Barrett食管(巴雷特)如何诊疗,一文囊括!
时间:2021-12-19 06:02:55 热度:37.1℃ 作者:网络
一、什么是巴雷特食管(BE)?
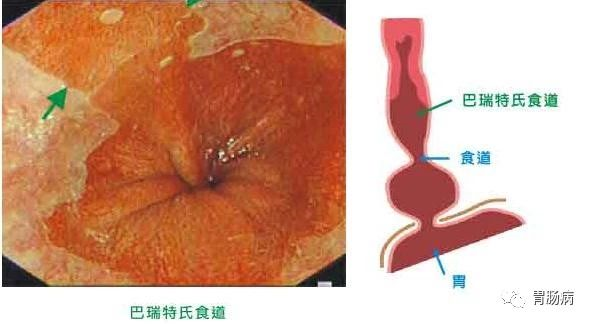
亦译为巴瑞特,是指食管下端有不正常的柱状上皮覆盖,称之为Barrett食管,又称barrett溃疡、慢性消化性溃疡和食管炎综合征。
普遍认为是获得性,并与反流性食管炎密切相关,并有发生腺癌的可能。1950年Norman Barrett首次提出,1957年确认,已渐为人们所关注。
Barrett食管是经内镜诊断,一般认为须距食管胃接合部至少有3cm以上处的柱状上皮覆盖,才能称Barrett食管。也有人认为Barrett食管是先天性的,因胎儿发育时期,食管的柱状上皮以后被鳞状上皮替代。异位柱状上皮残留于食管可在食管任何部位发生。
二、症状体征
Barrett食管本身并不产生症状,患者的症状主要由于反流性食管炎及其伴随病变引起。最常见的症状为反酸、胃灼热,其次为胸骨后疼痛和上腹痛。当出现食管狭窄时,突出的症状为咽下困难,吞咽困难的原因是:
1 鳞-柱状上皮交界处的狭窄;
2 慢性食管炎所致管壁纤维化,食管蠕动功能减退;
3 食管急性炎症引起的食管痉挛;
4 发生于柱状上皮的食管腺癌造成的管腔梗阻。
有些病人早期有烧心症状,经一段长时间的无症状期,直至并发症发生后才出现症状,原因是柱状上皮对消化液的刺激不如鳞状上皮敏感。Barrett食管出血可以大量,但常呈慢性缺铁性贫血。
少数穿孔或侵入胸膜腔引起瘘管或进入其他邻近器官出现症状。
三、Barrett食管的诊断
巴雷特食管的诊断标准如下:
内镜下可见食管鳞状上皮与胃柱状上皮的交界线(齿状线、Z线、SCJ)相对于胃食管结合部上移≥1cm(图3A),病理证实食管下段正常的复层鳞状上皮被化生的柱状上皮替代,可伴有或不伴有肠上皮化生;
内镜医师在诊断巴雷特食管时要应用Prague CM分型描述化生改变的范围,包括圆周范围及最大长度;
为明确有无肠化及异型增生(上皮内瘤变),对全周型病变建议纵向每间隔2cm的四壁分别活检1块,舌型病变每2cm最少活检1块;
对巴雷特食管但缺少肠上皮化生者,3~5年内应再次予以内镜检查并活检。
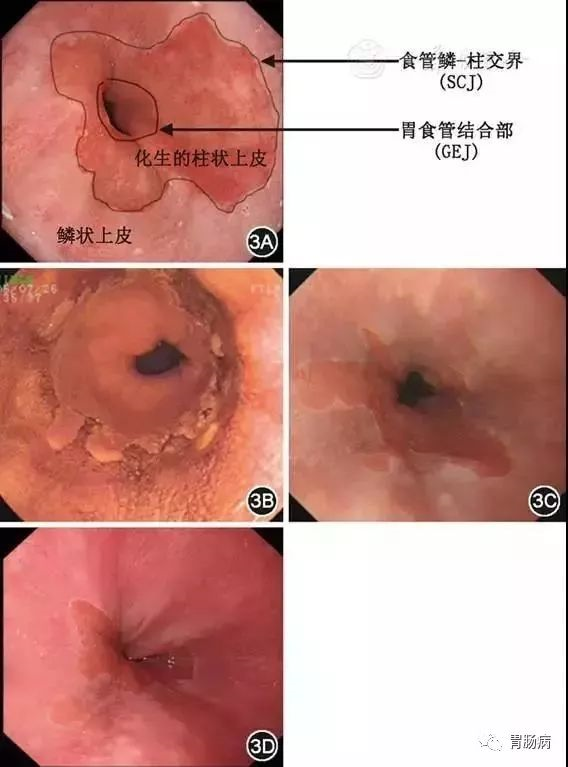
图3 巴雷特食管模式图及内镜下形态分型图
3A模式图 3B全周型巴雷特食管
3C舌型巴雷特食管 3D岛型巴雷特食管
由于巴雷特食管是食管腺癌唯一被公认的癌前病变,所以巴雷特食管的诊断很重要。对于巴雷特食管的诊断既要包括内镜下诊断也要包括病理诊断。诊断巴雷特食管首先要确定胃食管结合部。其次,诊断巴雷特食管还需要判断鳞-柱上皮交界,即食管下端鳞状上皮与胃柱状上皮交界构成的齿状线结构,亦称为Z线,当发生巴雷特食管时,齿状线上移,即发生了胃食管结合部与鳞-柱上皮交界的分离。
四、巴雷特食管内镜下分型
1、按化生的柱状上皮长度分型:
①长段巴雷特食管:化生的柱状上皮累及食管全周且长度≥3cm;
②短段巴雷特食管:化生的柱状上皮未累及食管全周或虽累及全周但长度为1~<3 cm。
2、按内镜下形态分型:全周型、舌型及岛型(见下图)。
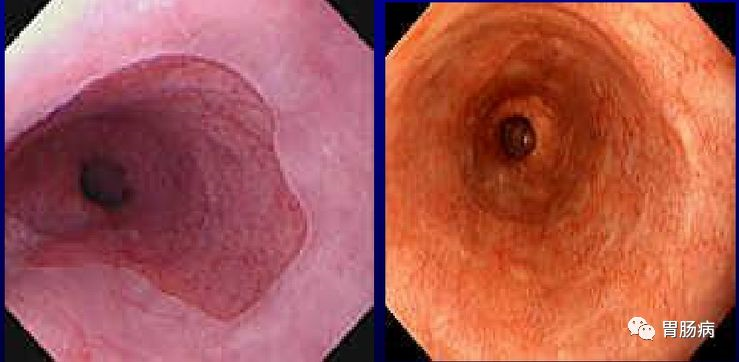
全周型
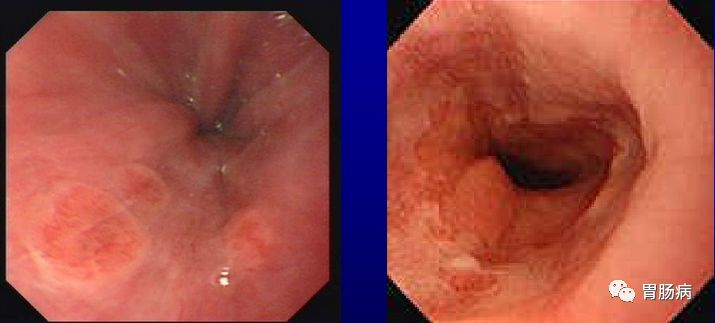
岛型
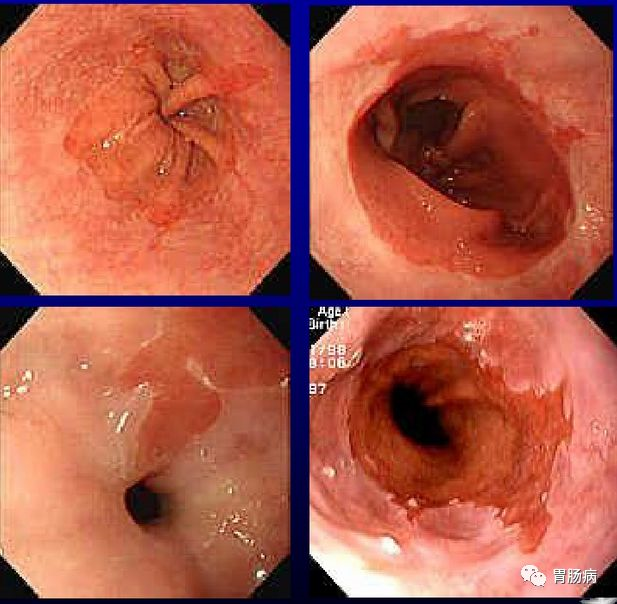
舌型
3、Prague CM分型:“C”代表全周型化生黏膜的长度,“M”代表非全周的化生黏膜的最大长度。如C2-M4表示食管全周柱状上皮长度为2cm,非全周的柱状上皮最大长度为4cm;C0-M4则表示无全周型柱状上皮化生,化生柱状上皮黏膜呈舌状伸展,长度为4cm。
由于80%食管腺癌发生在巴雷特食管基础上,而巴雷特食管黏膜瘤变的过程被认为是一个逐步发展的过程,从无异型增生(上皮内瘤变)到低级别异型增生(低级别上皮内瘤变),到高级别异型增生(高级别上皮内瘤变),最后发展为食管腺癌。
因此,巴雷特食管在组织病理学上可分为:
(1)无异型增生(上皮内瘤变)巴雷特食管
(2)不确定异型增生(不确定上皮内瘤变)巴雷特食管
(3)低级别异型增生(低级别上皮内瘤变)巴雷特食管
(4)高级别异型增生(高级别上皮内瘤变)巴雷特食管
(5)黏膜内癌。
有研究显示,伴肠上皮化生的巴雷特食管癌变风险比无肠上皮化生者高3倍以上;内镜诊断长度≥1cm巴雷特食管的可靠系数为0.72,而诊断长度<1cm者的可靠系数为0.22。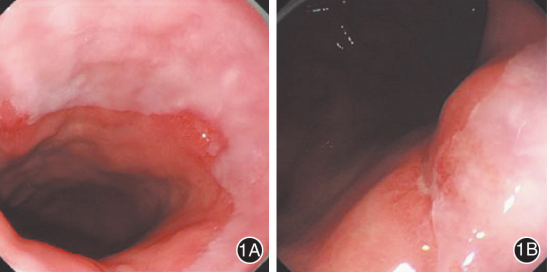
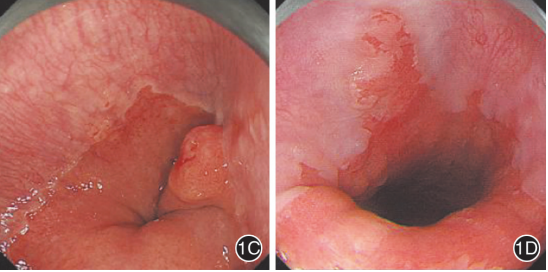 图4 早期巴雷特食管腺癌的白光内镜下形态
1A:三角形发红;1B:贲门糜烂型;1C:息肉样隆起型;1D:混合型
因此,在诊断巴雷特食管时一定要标注病变长度,以及是否有肠上皮化生和异型增生(上皮内瘤变)。
五、早期Barrett食管腺癌的诊断
图4 早期巴雷特食管腺癌的白光内镜下形态
1A:三角形发红;1B:贲门糜烂型;1C:息肉样隆起型;1D:混合型
因此,在诊断巴雷特食管时一定要标注病变长度,以及是否有肠上皮化生和异型增生(上皮内瘤变)。
五、早期Barrett食管腺癌的诊断
早食管癌患者临床上多无任何症状及体征,发生于巴雷特食管者可有长期胃食管反流症状,诊断上依赖于有资质医师的规范化胃镜检查,可疑病变的活检组织病理学为诊断的依据;
内镜下分型采用巴黎分型,主要分为隆起型、平坦型和凹陷型。
食管腺癌(包括巴雷特食管腺癌)表面黏膜在颜色、结构以及分布等方面会发生很大改变,以食管黏膜出现红色小结节或形态不规则为典型表现,如发现黏膜形态破坏或糜烂病灶则提示可疑肿瘤浸润。 早期食管腺癌内镜下主要分为以下几种类型(图4):
(1)0-Ⅰ型(隆起型):0-Ⅰp型,带蒂息肉型;0-Ⅰs型,无蒂息肉型;
(2)0-Ⅱ型(平坦型):0-Ⅱa型,平坦隆起型;0-Ⅱb型,完全平坦型;
(3)0-Ⅱc型,平坦凹陷型;
(4)0-Ⅲ型(凹陷型):病变凹陷较深,病变覆盖整个凹陷面。
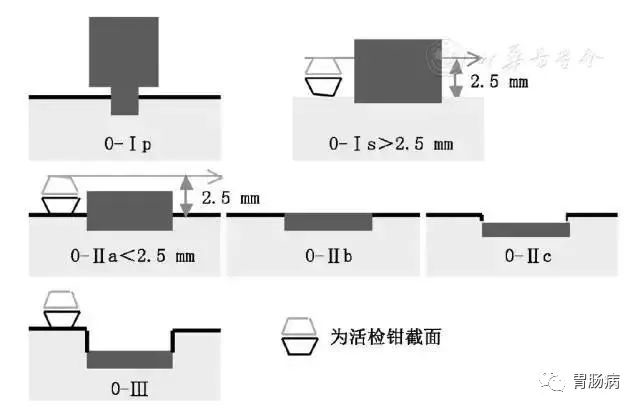 图5 早期巴雷特食管腺癌内镜下巴黎分型模式图
六、检查方法
图5 早期巴雷特食管腺癌内镜下巴黎分型模式图
六、检查方法
1、实验室检查:
食管动力检测BE患者食管下括约肌功能不全,食管下段压力减低,容易形成胃食管反流,且对反流性酸性物质的清除能力下降,因此通过对患者食管内压力及pH进行监测,对提示BE的存在有一定参考意义。一般认为食管下括约肌压力低于1.33kPa为功能不全。Ranson等经实验测定正常人食管下括约肌压力为2.6kPa±7kPa,而在广泛性BE患者为0.97kPa±3.46kPa,显著低于正常对照组。当内镜不能确定食管下段边界时,还可在测压指导下进行活检。
2、其他辅助检查:
(1)X线检查 较难发现Barrett食管,有食管裂孔疝及反流性食管炎的表现,不是此症的特异性。发现食管有消化性狭窄或体部有溃疡者应疑有Barrett食管。
(2)内镜检查 内镜下较易确认Barrett黏膜,正常食管黏膜为粉红带灰白,而柱状上皮似胃黏膜为橘红色,两者有显著差异。内镜下BE可分为三型:
全周型:红色黏膜向食管延伸累及全周,与胃黏膜无明显界限,其游离缘距食管下括约肌3cm以上。
岛型:齿状线1cm处以上出现斑片状红色黏膜。
舌型:与齿状线相连,伸向食管呈半岛状。在Barrett上皮可以出现充血、水肿、糜烂或溃疡,反复不愈的溃疡可引起食管狭窄。 (2)食管测压及pH监测 Barrett食管的病人食管与酸、碱反流物接触时间长可见到胃食管反流的测压表现,其食管下端括约肌压力较一般的反流病人为低。
七、并发症
Barrett食管可发生严重的并发症,良性并发症包括反流性食管炎、食管狭窄、溃疡、穿孔、出血和吸入性肺炎等。
(1)溃疡
Barrett食管引起溃疡的发病率为2%~54%,食管柱状上皮受酸性消化液腐蚀后可以发生溃疡,出现类似胃溃疡的症状,疼痛可放射至背部,并可引起穿孔、出血、浸润、溃疡愈合后发生狭窄,出现下咽不畅的症状。甚至可穿透主动脉导致大出血而迅速致死。
Barrett溃疡的病理分型有两种,最为常见的为发生在鳞状上皮段的浅表性溃疡,这种类型与因反流性食管炎引起的溃疡相似。另一种少见的为发生在柱状上皮段的深大溃疡,与消化性溃疡相似。
(2)狭窄 食管狭窄是Barrett食管最常见的并发症,发生率为15%~100%。狭窄部位多于食管中上段的鳞-柱状上皮交界处,而胃食管反流引起的狭窄多位于食管下段。反流性食管炎的发生率为29%~82%。病变可单独累及柱状上皮,也可同时累及鳞状和柱状上皮。
(3)恶变 Barrett食管中发生癌肿的发生率不甚确切,长期反流物进入Barrett食管可能起恶变作用。但有研究认为Barrett食管病病人施行了抗反流手术亦不能使这些柱状上皮消退,亦不减少恶变的危险性。
Barrett食管的柱状上皮区内可以发生异型增生,程度可自低度到高度,有时低度异型增生不易与正常柱状上皮区别,高度异型增生与原位癌有时难予区别,并可进展至浸润癌。这些恶变的肿瘤系腺癌。
需要指出的是内镜发现贲门腺癌伴有良性柱状上皮与柱状上皮异型增生为腺癌是有区别的。Barrett食管的异型增生是癌前期状况已为多数人公认。
(4)胃肠道出血 可表现为呕血或便血,并伴有缺铁性贫血,发生率约为45%,其出血来源为食管炎和食管溃疡。
八、治疗
(1)药物治疗
1)质子泵抑制剂(PPIs): 为内科治疗首选药物,剂量宜较大,如洛赛克20~40mg,每天2次口服,症状控制后以小剂量维持治疗,疗程半年以上。有证据表明,PPIs长期治疗后可缩短Barrett黏膜长度,部分病例BE黏膜上有鳞状上皮覆盖,提示PPIs能使BE部分逆转,但很难达到完全逆转。
PPIs治疗还可使BE中肠化生及异型增生消退,表明PPIs可阻止BE病情发展,增加鳞状上皮逆转的机会,减少恶性变的危险。
2)促动力药(多潘立酮,西沙必利等): 此类药物能减少胃食管反流,控制症状,但疗程较长。如多潘立酮10~20mg,每天3~4次,常与PPIs同时应用,以增加疗效。
3)其他: 如硫糖铝、思密达等黏膜保护剂亦有一定疗效,可改善症状,与PPIs合用效果更佳。
(2)内镜治疗
随着内镜治疗技术的发展,近年来内镜下消融治疗(endoSCopic ablation therapies,EATs)已应用于临床。
EATs可分为热消融、化学消融和机械消融三大类。热消融又包括多极电凝术(MPEC)、氩光凝固法(APC)和激光(KTP、YAG等)。化学消融主要指光动力学治疗(PDT),其基本原理为先将光敏剂如血紫质等静脉注射使其定位于食管的化生或异型增生或腺癌上皮,通过非热力的光化学反应而致局部组织坏死。
本方法的缺点是可引起皮肤光过敏反应。最近有报道应用特异性强的无皮肤光敏的5-氨基乙酰丙酸(ALA)治疗伴有异型增生或黏膜内癌的病例,可使不典型增生100%消失,黏膜内癌治愈率为72%。 机械消融则在内镜下运用萃吸、切除等方法。EATs加PPIs抑酸治疗是目前治疗BE及BE伴异型增生的有效方法,使BE上皮消失或逆转为鳞状上皮,疗效可达70%~100%,并发症发生率较低。 有明显食管狭窄者可进行食管探条或球囊扩张术,但其疗效较短暂,可能需多次扩张。
(3)外科治疗
手术适应证为:
(1)BE伴严重的症状性反流,内科治疗无效者。
(2)食管狭窄经扩张治疗无效者。
(3)难治性溃疡。
(4)重度异型增生或癌变者。
手术方式有多种,一般选择Nissen胃底折叠术,对重度异型增生或癌变者宜作食管切除术。对于抗反流手术的治疗效果目前尚存在争议。一些学者认为,虽然抗反流手术能够缓解反流症状,使溃疡愈合和改善狭窄,但不能逆转BE上皮,更不能逆转异型增生进展为腺癌。
(4)射频消融技术
射频治疗是一种热凝固治疗,是利用肿瘤细胞对热的耐受能力比正常细胞差这一特点实现治疗的。射频发生器产生的高频射频波通过插入肿瘤组织中的电极发出射频电流,再经过辅助电极形成回路,通过周围组织发生凝固性坏死。此方法安全,有效,简单。
有研究表明,巴瑞特食管合并不典型增生或是巴瑞特食管合并早期癌(即粘膜内癌)的患者中,经射频消融治疗后,巴瑞特食管复发的几率大约为 5%/ 年。患者的临床特点对疾病的复发并没有预测性。 所以,经射频消融治疗后的患者仍需长期进行定期内镜检查以实现对疾病复发的早期发现。
(5)非药物治疗的其他选择 1)腹腔镜下胃底折叠术 被证实可以有效减少所有酸性、弱酸性或非酸性的反流症状。 但有研究显示,利用内镜下缝合技术和内镜下射频消融技术进行治疗的胃食管反流患者与进行假手术治疗的患者比较,症状改善并无差别。 一项为期2年的非对照研究结果提出,在不存在食管裂孔疝的患者中,一种经口的折叠设备EsophyX可以促进胃食管反流症状缓解并减少对质子泵抑制剂的应用。 2)腹腔镜下抗反流技术 是在胃食管交界处放置一条磁珠组成的可动性束带,研究证实可以有效减少食管的酸暴露情况(由10.9%下降至3.3%),可以有效改善症状并减少质子泵抑制剂的使用。但该研究缺乏假手术对照组且随访时间只有1年。 3)食管下括约肌电刺激 利用腹腔镜植入电极对食管下括约肌电刺激,通过刺激食管下括约肌收缩来增加括约肌张力、减少反流、减轻症状。 九、预后 对不伴异型增生的巴雷特食管,因其癌变的概率低,治疗后一般都能逆转,有的甚至不需治疗,所以不必过度 担心,定期复查就可以了。 伴有异型增生者,必须要积极治疗,因为演变为食管腺癌的几率增大,但是预后也比较好,一般都能治愈。
但是,Barrett食管癌的预后较差,其主要原因是诊断时已属晚期,多数伴有淋巴结和局部转移。总体的5年生存率为21%~55%,淋巴结阴性组的5年生存率为91%,明显高于其他组。
Barrett食管癌的临床分期和肿瘤大小是影响远期生存率的重要因素,据报道,Ⅱ期肿瘤及肿瘤直径<6cm者的5年生存率分别为25%和21%,而Ⅲ期和Ⅳ期及肿瘤直径>6cm者的分别为4.5%和0。
预后与肿瘤的分化程度和外侵情况有关,而与肿瘤部位、患者年龄、性别以及手术方式无关。


