Lancet Neurol:无功无过——间充质干细胞与安慰剂治疗多发性硬化症(MESEMS)的安全性、耐受性和活性的研究
时间:2021-10-29 10:02:12 热度:37.1℃ 作者:网络
间充质干细胞(mesenchymal stem cells,MSCs),又称间充质基质细胞,是一种多能细胞,可以从包括骨髓在内的不同中胚层来源的组织中分离出来。自从Friedenstein首次对MSCs进行鉴定以来,MSCs因其迁移到中枢神经系统获得神经元表型的能力而引起了神经学家的兴趣。最近的研究表明,在移植后,MSCs迅速从宿主中清除出来,并经历了有限的转分化。多发性硬化症临床前模型的体外和体内研究显示了其他令人鼓舞的特征,即MSCs调节免疫反应的能力、抑制炎症的能力、保护神经细胞免受损伤的能力和促进再分化。这使得骨髓间充质干细胞成为治疗多发性硬化症等疾病的理想候选细胞,在这些疾病中,炎症和组织损伤并存。
在这些前提的基础上,已经通过静脉或鞘内输送骨髓来源的自体骨髓间充质干细胞治疗多发性硬化症进行了一些小型临床试验,证明了这项操作的安全性。2012年发表的一项小型2期研究显示了静脉注射治疗多发性硬化症的一些令人鼓舞的结果。然而,这些小型的、大多是非对照的研究并不足以证明骨髓间充质干细胞移植治疗多发性硬化症是否真的安全有效尚不能确定。近日,研究人员评价了自体骨髓间充质干细胞静脉输注治疗活动性多发性硬化症患者的安全性、耐受性和活性。

MESEMS是一项具有交叉设计的2期概念验证、多中心、随机、双盲、安慰剂对照试验。
该研究在9个国家的15个地点进行。年龄18-50岁的活动性复发-缓解型或进展型多发性硬化症患者,如果他们自多发性硬化症发病以来的病程为2-15年,扩展的残疾状态量表评分为2.5-6.5,则纳入其中。根据交叉设计,患者被随机分配(1:1),在第24周接受单次静脉注射自体骨髓来源的MSCs,然后接受安慰剂,或在第24周接受安慰剂,随后接受自体MSCs。主要目的是测试MSC治疗的安全性和活性。主要的安全终点是评估每个治疗臂内不良事件的数量和严重程度。主要疗效终点是治疗组之间在第4、12和24周内计算的钆增强病变(GELs)的数量。在所有参与者完成第24周的访问后,在完整的分析集合中评估主要疗效终点。疗效终点使用预定义的统计测试程序进行评估。在整个研究过程中,通过记录每次就诊时的生命体征和不良事件来监测安全性。
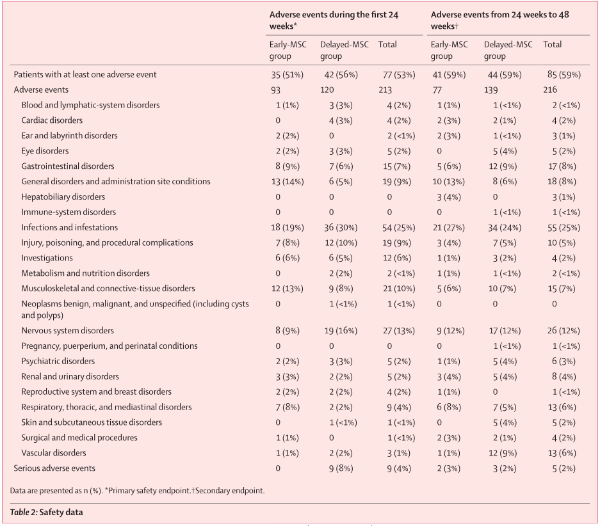
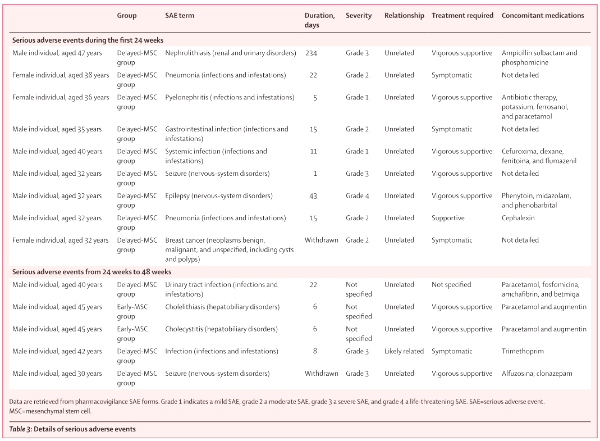
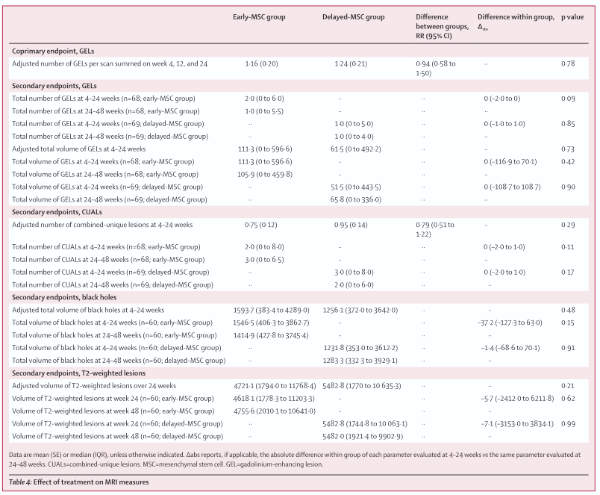
骨髓来源的MSC治疗是安全的,耐受性良好,但对活动性多发性硬化症患者第24周的GELs没有影响,GELs是急性炎症的MRI替代标记物。因此,本研究不支持使用骨髓间充质干细胞治疗活动性多发性硬化症。进一步的研究应该解决间充质干细胞对组织修复相关参数的影响。


