GUT:长期的饮食习惯影响肠道微生物群的促炎和抗炎特性
时间:2021-04-11 11:01:27 热度:37.1℃ 作者:网络
肠道微生物群直接影响肠道内促炎和抗炎反应的平衡。微生物对营养素的竞争在控制这种平衡中起着关键作用。炎症性肠病(IBD)是肠道微生物区系和肠道免疫系统之间失去平衡的典型疾病。除局部免疫反应外,肠道微生物区系还影响全身免疫成分,并与越来越多的免疫介导的炎症性疾病(IMID)有关,从糖尿病到关节炎和系统性红斑狼疮。肠道生态失调和相关炎症也与癌症和心脏代谢紊乱有关。流行病学研究揭示了与这些疾病的发病有关的几种饮食因素。然而,这种关系背后的机制在很大程度上仍不清楚。这项研究的目的是调查人类习惯性饮食、肠道微生物区系和肠道炎症之间的复杂关系。该文章发表在GUT杂志。

该研究调查了来自克罗恩病、溃疡性结肠炎、肠易激综合征和普通人群四个队列的1425名个体的173个饮食因素与微生物群的关系。用鸟枪式元基因组测序来分析肠道微生物的组成和功能。膳食摄入量通过食物频率问卷进行评估。进行了无监督的聚类,以确定饮食模式和微生物群。每个队列研究饮食和微生物特征之间的关联,然后进行荟萃分析和异质性评估,
以探索饮食-微生物组关联在不同疾病背景下的可复制性。该研究提出了促炎和抗炎机制,通过这些机制,特定的食物和饮食模式可以影响肠道内的炎症反应,作为设计饮食干预措施的合理基础。
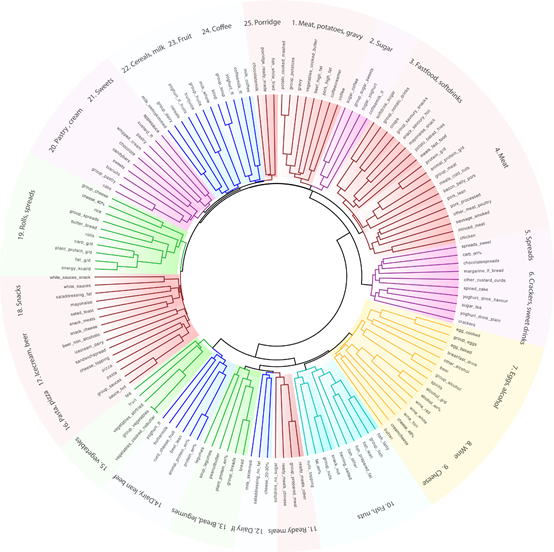
无监督饮食聚类分析揭示了常见的食物模式。分支图显示饮食摄入量分成25种类型。采用食物频率问卷调查了1425名健康对照者(n=871)、肠易激综合征(n=223)、克罗恩病(n=205)和溃疡性结肠炎(n=126)的饮食情况。使用平方欧几里德距离进行无监督的分层聚类。
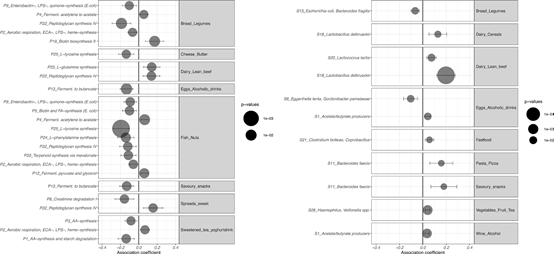
在跨疾病荟萃分析中,饮食模式与途径(A)和物种(B)簇的一致性关联。在对跨越四个队列的1425个个体进行的交叉疾病荟萃分析中,森林小区显示了饮食模式和微生物群之间的一致结果(FDRMeta<0.05,p-Cochran‘s-Q>0.05)。点表示荟萃分析的汇集结果;黑线表示顺式。点大小表示关联的重要性(FDR校正后的p值)。X轴表示系数。采用平方欧几里德距离和Bray-Curtis距离对膳食摄入量、物种和途径丰度进行无监督的系统聚类。在每个队列中,建立了食物集群与微生物集群的多变量线性模型,添加了年龄、性别、测序深度和卡路里摄入量作为协变量。对每个队列获得的结果进行逆方差荟萃分析,然后进行多重检验校正和Cochran‘s Q检验。
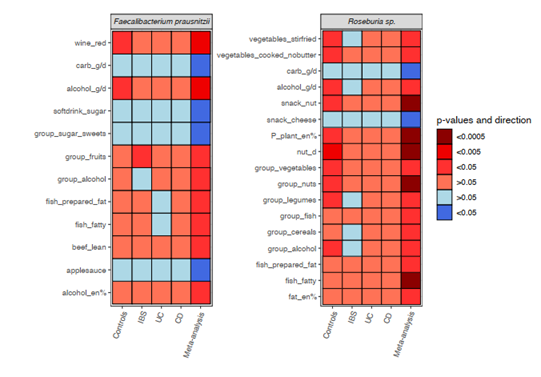
荟萃分析中与Faecalibacterium prausnitzii (A)和Roseburia (B)相对丰度相关的饮食因素。热图显示不同食物间的交叉荟萃分析结果与(A) Faecalibacterium prausnitzii和(B) Roseburia的相对丰度有显著的一致性(FDR<0.05,p-Cochran‘s-Q>0.05)。膳食摄入量通过食物频率问卷进行评估。能量调节采用营养密度法。对于每个食物项目,构建了食物摄入量与分类群和路径的多变量线性模型,添加了年龄、性别和测序深度作为协变量。对每个队列进行关联分析,然后进行逆方差荟萃分析、多重检验校正和Cochran‘s Q检验。红色,正关联;蓝色,负关联。颜色密度表示关联的重要性(FDR校正的p值)。
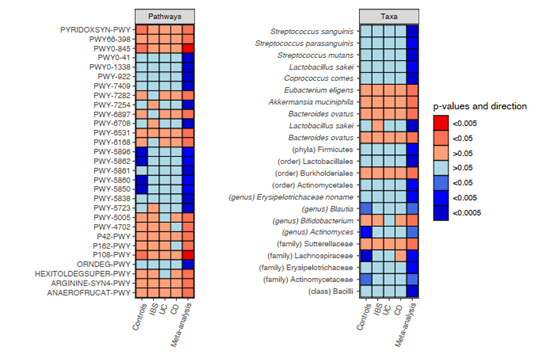
荟萃分析中与植物蛋白摄入相关的微生物代谢途径(A)和分类群(B)。热图显示,植物蛋白摄入量与肠道微生物群落(A)代谢途径和(B)分类丰度的相对丰度之间的交叉荟萃分析结果显著且一致(FDR<0.05,p-Cochran‘s-Q>0.05)。膳食摄入量通过食物频率问卷进行评估。对于每个食物项目,我们构建了食物摄入量与分类群和路径的多变量线性模型,添加了年龄、性别和测序深度作为协变量。对每个队列进行关联分析,然后进行逆方差荟萃分析、多重检验校正和Cochran‘s Q检验。红色,正关联;蓝色,负关联。颜色密度表示关联的重要性(FDR校正的p值)。
该研究确定了饮食模式和微生物群之间的38个关联。此外,在对健康人和IBS、克罗恩病和UC患者进行的荟萃分析中,61种食物和营养素与61种249种代谢途径相关(FDR<0.05)。加工食品和动物性食品一直与富含Firmicuts、该属物种和内毒素合成途径有关。植物性食物和鱼类则相反,它们与产生短链脂肪酸的共生体和营养新陈代谢途径呈正相关。
这项研究通过研究四个队列中无人监督的饮食模式、肠道炎症标志物和肠道微生物组成和功能之间的关系,展示了习惯性饮食选择如何影响人类肠道生态系统及其炎症潜能。确定了在克罗恩病、溃疡性结肠炎、肠易激综合征患者和普通人群中复制的重要关联,这意味着微生物组靶向饮食策略有可能缓解和预防肠道炎症。
该研究推断出与已知有粘膜保护和抗炎效果的细菌群和功能相一致的饮食模式。提供了饮食与微生物区系之间的联系是强有力的证据:结果在不同的队列中是一致的,在调整了额外的队列特定因素(如药物使用)后仍然显著。研究结果表明,CD、UC、IBS患者和普通人群对饮食的共同反应可能与炎症、肠道微生物变化和营养是共同主线的其他疾病背景有关。许多炎症性疾病(包括癌症、动脉粥样硬化、肥胖、非酒精性脂肪性肝炎、肝硬化和IBD)的细菌及其抗炎功能的减少。长期饮食富含豆类、蔬菜、水果和坚果,植物性食物的摄入量高于动物性食物,偏爱低脂发酵乳制品和鱼,同时避免烈性酒精饮料、加工高脂肪肉类和软饮料,有可能通过肠道微生物群防止肠道炎症过程。不遵守这些原则则IBD的风险增加。饮食可以通过调节肠道微生物群成为一种重要的补充治疗策略。食用植物性饮食可以增加肠道微生物区系的丰度,进一步增强治疗敏感度。
原文出处
Bolte Laura A,Vich Vila Arnau,Imhann Floris et al. Long-term dietary patterns are associated with pro-inflammatory and anti-inflammatory features of the gut microbiome.[J] .Gut, 2021, undefined: undefined.


