Cell子刊:西湖大学董晨等揭示了影响癌症免疫治疗效果的T细胞亚群!
时间:2025-02-01 12:08:54 热度:37.1℃ 作者:网络
抗PD-1与lenvatinib的组合在多种癌症中显示出临床疗效,但潜在的免疫学机制尚不清楚。
2025年1月30日,西湖大学董晨、深圳湾实验室张雷及中国解放军总医院卢实春共同通讯在Cancer Cell在线发表题为“Contrasting cytotoxic and regulatory T cell responses underlying distinct clinical outcomes to anti-PD-1 plus lenvatinib therapy in cancer”的研究论文,该研究表明细胞毒性和调节性T细胞反应的对比是抗PD-1联合lenvatinib治疗癌症的不同临床结果的基础。
在这里,研究人员使用单细胞转录组学和T细胞受体(scTCR)克隆型分析比较了联合治疗前后肝细胞癌(HCC)患者的T细胞。肿瘤浸润GZMK+ CD8+效应/效应记忆T (Teff/Tem)细胞对联合治疗表现出良好的反应,其包含祖细胞耗竭T (Tpex)细胞以及富含乙型肝炎病毒(HBV)特异性的不受欢迎的循环Tem (cTem)细胞。进一步的综合分析显示,cTem细胞与联合治疗的反应性特别相关,而Tpex细胞对联合治疗和抗PD-1单一治疗的反应都有贡献。值得注意的是,在联合治疗后,肿瘤中开发不足的KIR+ CD8+ T细胞亚群和FOXP3+ CD4+调节性T细胞在无应答者中特异性富集。因此,该研究阐明了T细胞亚群与癌症免疫治疗的临床益处和抗性相关。

免疫检查点阻断(ICB),特别是针对CD8+ T细胞上表达的抑制性受体程序性细胞死亡1 (PD-1),是一种针对各种癌症的高效免疫疗法。然而,大多数患者未能受益。在对抗PD-1单药治疗无反应的癌症中,联合其他治疗偶尔会改善结果。值得注意的是,联合ICB和抗血管生成治疗提高了对肝细胞癌(HCC)和胆道癌等癌症的疗效。抗PD-1和lenvatinib(一种针对血管内皮生长因子(VEGF)受体的多靶点酪氨酸激酶抑制剂)的联合使用,将HCC患者的反应率从单独使用抗PD-1的17%提高到45%。然而,反应和抵抗背后的免疫学机制仍然存在。
应用ICB和联合疗法作为新辅助治疗提供了一个机会,通过时间样本观察肿瘤微环境(TME)中的免疫细胞动力学。CD8+T细胞,PD-1阻断的主要靶点,显示出对各种癌症类型的良好反应,包括局部克隆扩增以及循环T细胞的募集。在HCC患者中,治疗前CD8+ T细胞的存在与对ICB和抗PD-1加lenvatinib的反应有关。在TME,长时间的抗原暴露导致T细胞衰竭,表现为失去效应子功能。单细胞测序已经确定了在癌症中具有不同衰竭水平的CD8+ T细胞亚群,包括晚期衰竭T (tTex)细胞。TCF7+祖细胞耗竭T (Tpex)细胞,GZMK+效应/效应记忆T (Teff/Tem)细胞,和CXCL13+ Tpex细胞。这些细胞亚群对抗PD(L)-1疗法表现出不同的反应,TCF7+Tpex细胞被证明对小鼠肿瘤模型和癌症中的ICB反应至关重要。
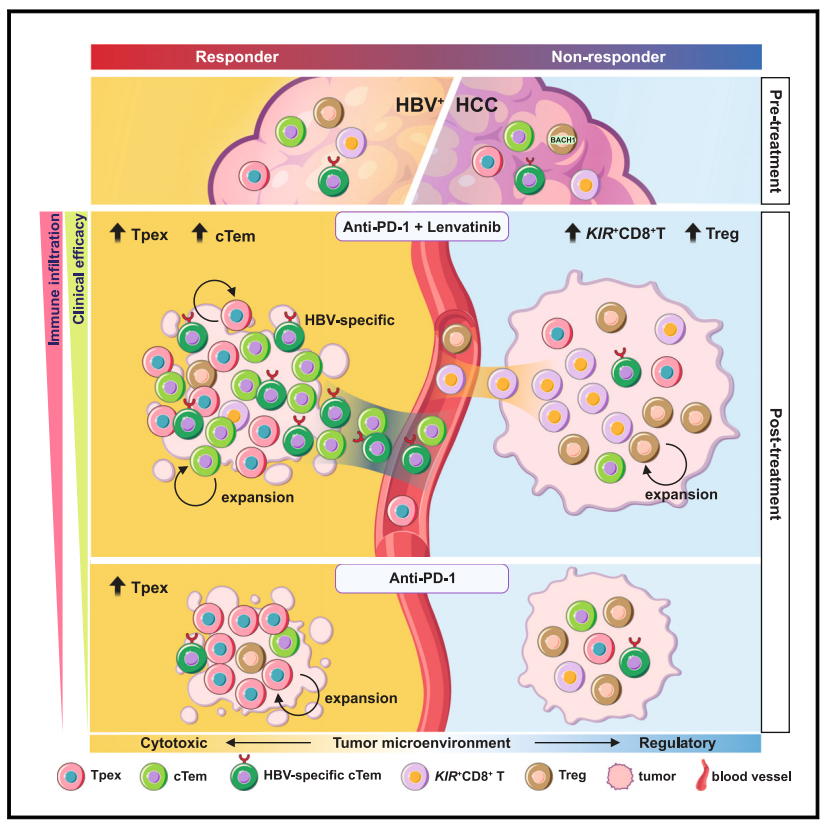
机理模式图(图源自Cancer Cell)
最近,在患有自身免疫性疾病和感染的患者中发现了KIR+ CD8+ Treg细胞亚群。这些细胞以抑制性杀伤细胞免疫球蛋白样受体(KIRs)为标志,并抑制致病性CD4+ T细胞。在癌症患者的外周血中也报道了CD8+ T细胞显示KIRs的高表达水平,但在TME仍未得到充分研究,特别是关于它们的特征、来源、分化和对ICB疗法的反应。
在这项研究中,为了了解对免疫疗法的反应性和抗性的免疫学机制,分析了接受新辅助抗PD-1加lenvatinib治疗的HBV+ HCC患者的T细胞动力学。总之,该研究阐明了HCC联合治疗和抗PD-1单一治疗期间的T细胞动力学,增强了人们对肿瘤免疫治疗应答和抵抗的免疫学机制的理解。这些见解可能有助于改善目前的疗法和发展未来的治疗策略。
参考消息:
https://www.cell.com/cancer-cell/abstract/S1535-6108(25)00019-4


