Adv Sci 中南大学湘雅三医院陆瑶/浙江大学徐清波教授团队发现内皮TRIM35泛素化调控搭桥动脉钙化的重要机制
时间:2025-01-30 12:08:17 热度:37.1℃ 作者:网络
搭桥动脉重构及狭窄始终是制约冠状动脉旁路移植术(Coronary Artery Bypass Grafting, CABG)血运重建的关键因素,冠脉搭桥后钙化与冠心病患者术后死亡率增加直接相关。尽管动脉钙化是反映CABG术后预后不良的重要指标,但由于其致病因素的多变性导致目前缺乏有效的逆转或预防钙化的药物治疗和靶点。寻找直接靶向血管钙化的调控因子,有望突破当前动脉搭桥慢性血管重构防治的瓶颈。
2025年1月27日,中南大学湘雅三医院陆瑶教授、浙江大学徐清波教授团队在Advanced Science上在线发表了题为“Endothelial TRIM35-regulated MMP10 Release Exacerbates Calcification of Vascular Grafts”的研究论文,该研究揭示了内皮TRIM35 (Tripartite Motif 35)通过K242/K327位点K63-多聚泛素化NF-κB非经典通路关键元件RelB并调节MMP10 (Matrix Metalloproteinase 10)的合成分泌,继而通过内皮旁分泌调控平滑肌细胞异常成骨转换和搭桥血管钙化。该研究首次发现抑制内皮-平滑肌细胞激活的MMP10可能是预防搭桥动脉粥样硬化及再狭窄的新方法,为靶向预防和改善血管重构提供了全新见解。

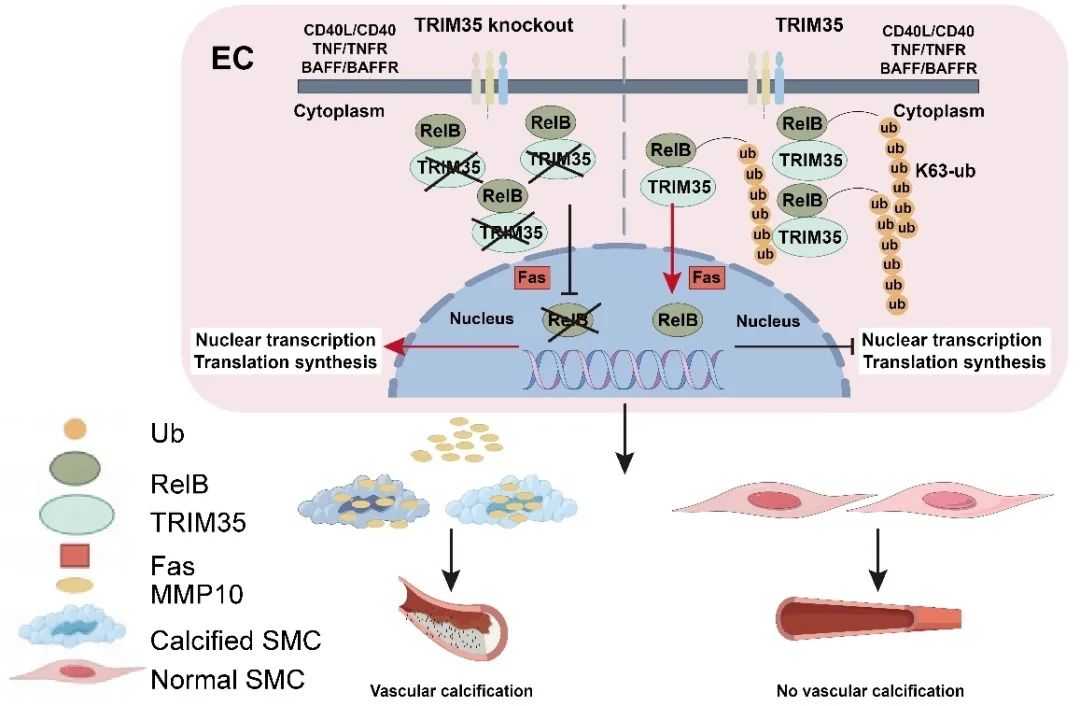
该研究中作者首次揭示了小鼠自体动脉搭桥后内皮TRIM35表达上调是保护搭桥动脉钙化的关键因素。TRIM35敲除驱动的MMP10分泌增多是导致平滑肌细胞异常成骨转换和搭桥动脉钙化的核心效应。进一步机制发现,内皮细胞TRIM35可以作为“分子刹车”,通过K63-多聚泛素化RelB的K242/K327位点并维持NF-κB非经典通路的稳定。内皮敲除TRIM35导致MMP10核转录异常活化和分泌增加,并诱导平滑肌细胞和动脉钙化。体外使用MMP10抑制剂和中和抗体均可有效逆转内皮TRIM35敲除诱导的搭桥动脉钙化。
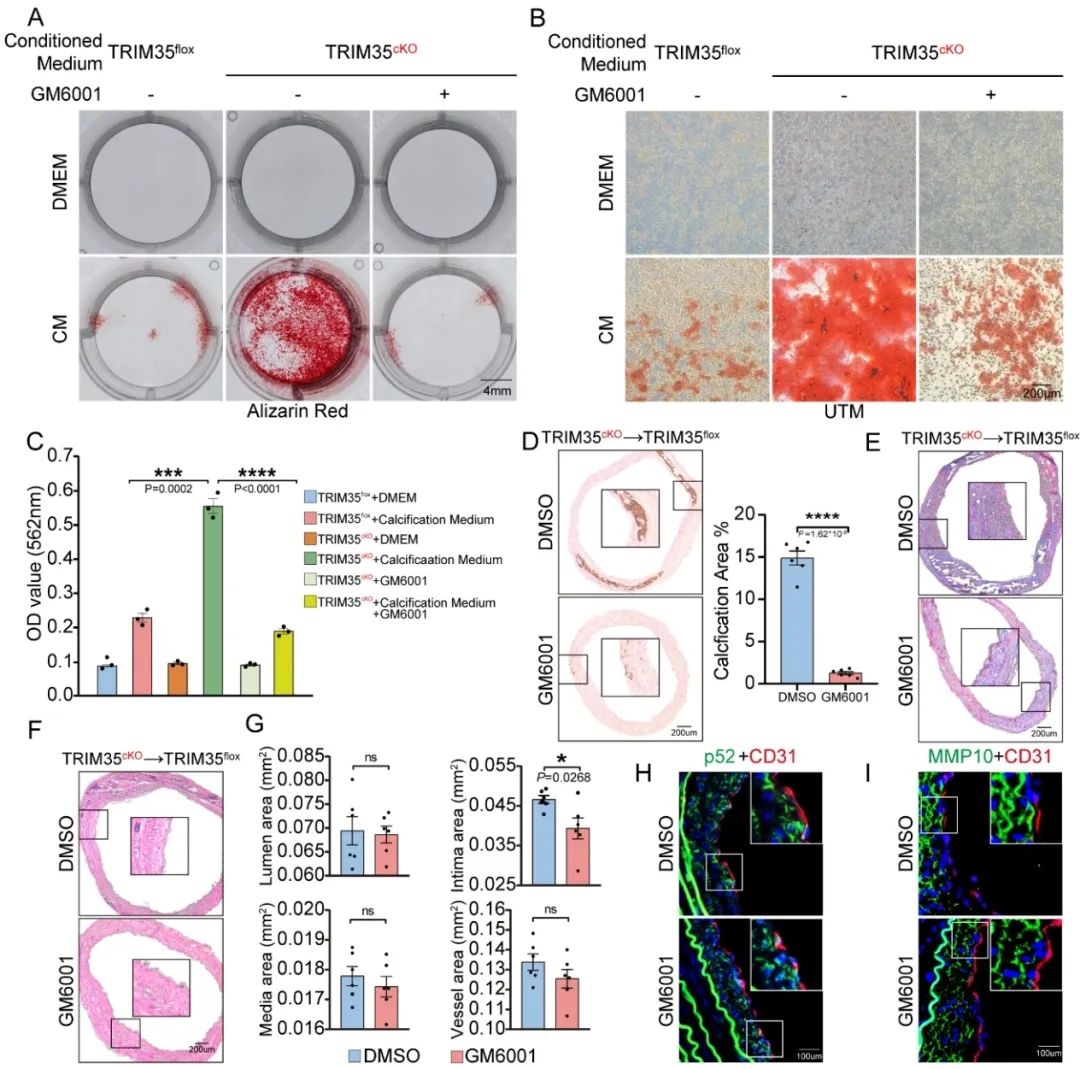
该研究鉴定了TRIM35调控的内皮-平滑肌细胞通讯在搭桥动脉钙化病理过程中的全新分子生物学机制,靶向MMP10介导的平滑肌钙化有望改善搭桥动脉重构,为CABG干预提供新策略。
陆瑶课题组冷一铭博士后、硕士生王炜、陆君为本研究的共同第一作者;陆瑶教授和徐清波教授为本文的共同通讯作者。该工作还得到了北京大学基础医学部翁良教授的支持和指导。该项研究获得国家自然科学基金项目、国家重点研发计划、中南大学创新驱动项目、国家博士后面上基金项目等资助。
原文链接:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202409641


