澳门大学王瑞兵教授Angew:室温合成的sp²C共价有机框架通过诱导脂滴融合实现工程化巨噬细胞治疗
时间:2025-01-19 12:16:47 热度:37.1℃ 作者:网络
免疫细胞,例如巨噬细胞、T淋巴细胞,可以通过基因工程或表面化学修饰进行工程化,从而识别和选择性地杀伤肿瘤细胞。这种工程化细胞疗法凭借其强大的靶向能力和疗效,已成功实现临床转化。然而,该疗法的长期应用仍然面临自体细胞异质性、成本高昂、制造复杂等挑战。因此,开发一种便捷的技术来快速生产用于癌症治疗的工程化免疫细胞至关重要。
对线粒体、溶酶体、微管、细胞膜等亚细胞结构的人工操控(例如解聚、聚集、融合)已被证明是调节细胞行为和功能的有效策略。脂滴是真核细胞中中性脂质的主要储存库,通过与内质网、线粒体、核膜等亚细胞结构动态相互作用,在细胞脂质代谢中发挥关键作用。据信,脂肪酸氧化是支持巨噬细胞抗炎和促肿瘤表型的关键代谢特征。诱导脂质滴融合,从而隔离脂肪酸并重编程能量代谢,可能为工程化巨噬细胞的抗肿瘤应用提供一种有前景的策略。
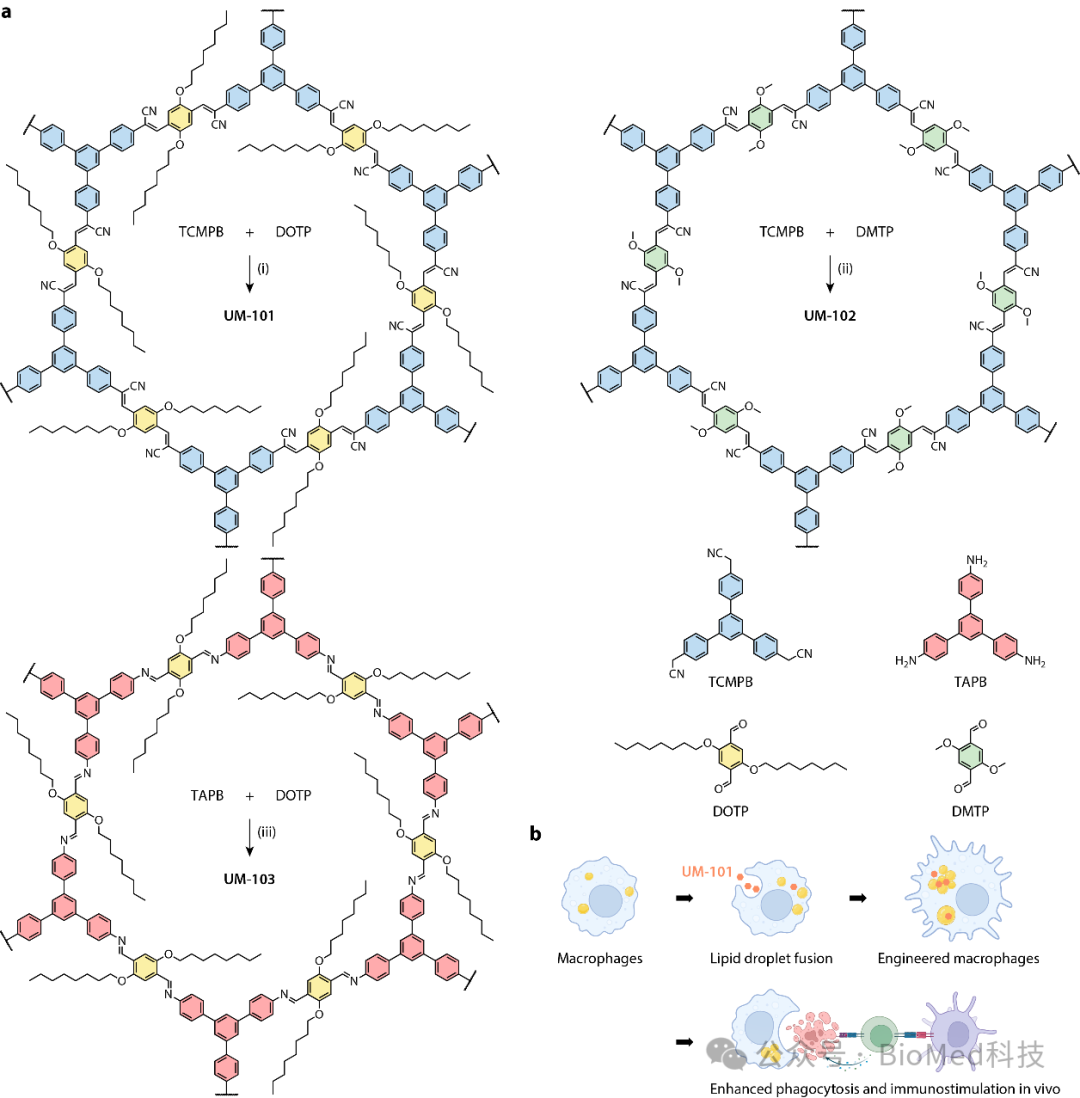
图1 COFs的结构与工程化巨噬细胞疗法示意图。
近日,澳门大学中华医药研究院王瑞兵教授课题组在Angew. Chem. Int. Ed.发表论文,提出了基于共价有机框架(COF)的脂滴融合策略来工程化巨噬细胞。澳门大学官群博士、山东第一医科大学周乐乐博士、澳门大学博士研究生杨植清为论文共同第一作者。澳门大学王瑞兵教授为论文通讯作者。
COF是通过有机构建块的动态共价聚合形成的多孔晶态聚合物。得益于高度有序的晶态框架,研究人员能够在合成之前预先设计COF框架和孔环境,以满足特定功能需求。合成的UM-101 COF集成了疏水性的烷基链和宽的π共轭结构,对中性脂质表现出高亲合力。UM-101在巨噬细胞中诱导脂滴聚集和融合,减少脂滴–线粒体接触,降低线粒体脂肪酸通量,促进巨噬细胞糖酵解和经典激活。静脉注射UM-101工程化的巨噬细胞不仅直接损伤肿瘤细胞,还触发了强烈的抗肿瘤免疫反应,有效抑制了CT26肿瘤的进展。
这是首次报告在室温下合成的sp2C-COF纳米颗粒,为通过细胞器操控开发工程化免疫细胞提供了新的视角。
参考文献:
Qun Guan, Le-Le Zhou, Zhiqing Yang, Beibei Xie, Yan-An Li, and Ruibing Wang*. An sp2 Carbon-Conjugated Covalent Organic Framework for Fusing Lipid Droplets and Engineered Macrophage Therapy. Angew. Chem. Int. Ed. 2025, e202421416. DOI: 10.1002/anie.202421416
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202421416


