2024 ASH丨泊马度胺破解多重难治性RRMM治疗困境
时间:2024-12-05 14:02:09 热度:37.1℃ 作者:网络
2024 ASH
2024年第66届美国血液学会(ASH)年会将于美国东部时间12月7日至10日在圣地亚哥举行。ASH作为全球血液学工作者的盛会,届时将汇集各个国家和地区知名血液病学专家,分享和探讨全球最前沿的研究进展和突破性临床研究及宝贵的临床实践经验。
近10余年靶向新药、造血干细胞移植及嵌合抗原受体T(CAR-T)细胞免疫治疗的应用,使骨髓瘤患者的疗效和预后取得了革命性进步,但MM至今仍无法治愈,患者终将面临疾病复发进展,进而难治,既往接受免疫调节剂(IMiDs)、蛋白酶体抑制剂(PIs)或抗CD38单克隆抗体(CD38)持续治疗的患者,双重难治或三重难治发生率大幅增加,预后不佳,且面临治疗选择有限的困境。泊马度胺具有直接杀伤肿瘤细胞及免疫调节的双重作用,与新型药物联用可协同增效,逆转耐药,为多重难治患者带来进一步获益。
随着近期大会摘要公布,泊马度胺在本次大会成果瞩目,多项国内外重磅研究入选。本期让我们聚焦泊马度胺联合方案在多重难治患者中的新进展与卓越疗效。
1996
Efficacy and Safety of Selinexor, Pomalidomide, and Dexamethasone (SPd) for Treatment of Patients with Relapsed or Refractory Multiple Myeloma (RRMM)
塞利尼索、泊马度胺和地塞米松(SPd)治疗复发性/难治性多发性骨髓瘤(RRMM)患者的疗效和安全性
Muhamed Baljevic
研究背景
多发性骨髓瘤(MM)目前仍无法治愈,尽管CAR-T疗法具有前景,但对既往接受免疫调节剂(IMiDs)、蛋白酶体抑制剂(PIs)或抗CD38单克隆抗体(CD38)治疗的RRMM患者,目前仍尚无标准治疗方案。LocoMMotion等大型观察性研究显示,接受常用抗MM药物治疗的三药暴露(TCE) RRMM的中位PFS较短,约为4.5个月。在此报告1b/2期STOMP试验(NCT02343042)每周1次40mg或60mg (QW)塞利尼索联合泊马度胺和地塞米松治疗RRMM的最新临床和安全性数据。
研究设计
塞利尼索多种剂量方案(40mg或60mg,每周1次) 联合Pd(泊马度胺给药剂量包括2mg、3mg或4mg,每日1次)旨在确定SPd方案的最大耐受剂量和2期推荐剂量,并评估其在RRMM患者中的疗效和安全性。
研究结果
截至2024年3月25日,共纳入了81例患者接受SPd治疗,其中SPd(60mg)组20例, SPd(40mg)组16例。在接受SPd治疗的所有患者中,53.1%为男性,中位年龄为65岁,既往中位治疗线数为3线。IMiDs既往暴露/难治的患者为100%/86.4%;PI为100%/80.2%;CD38单抗为33.3%/30.9%;TCE为33.3%/25.9%。
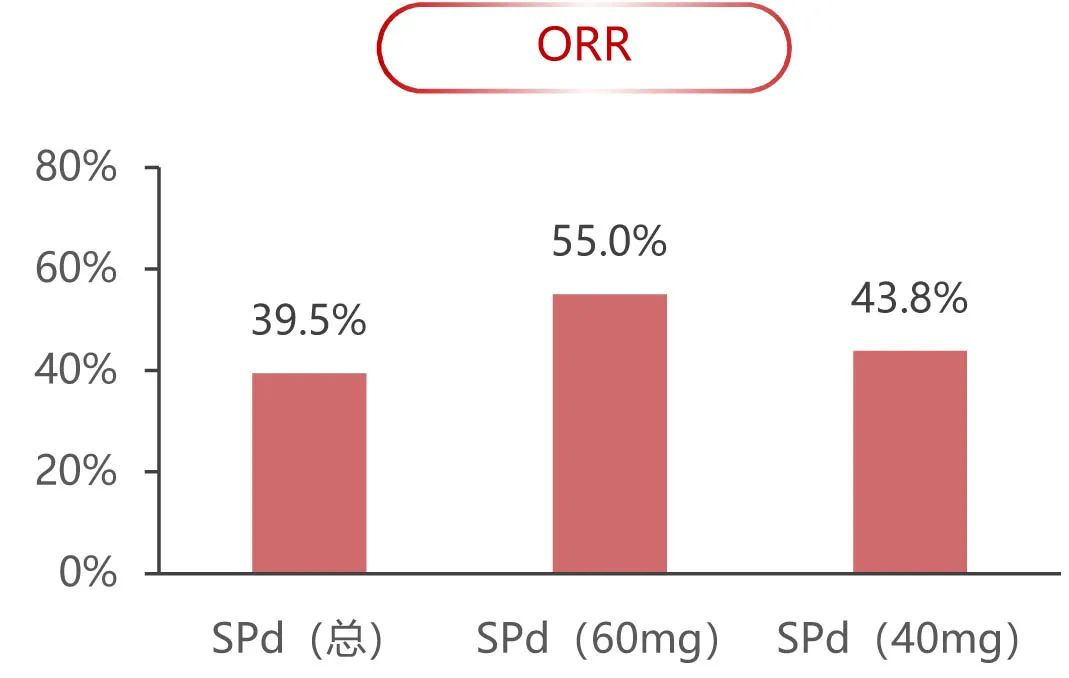
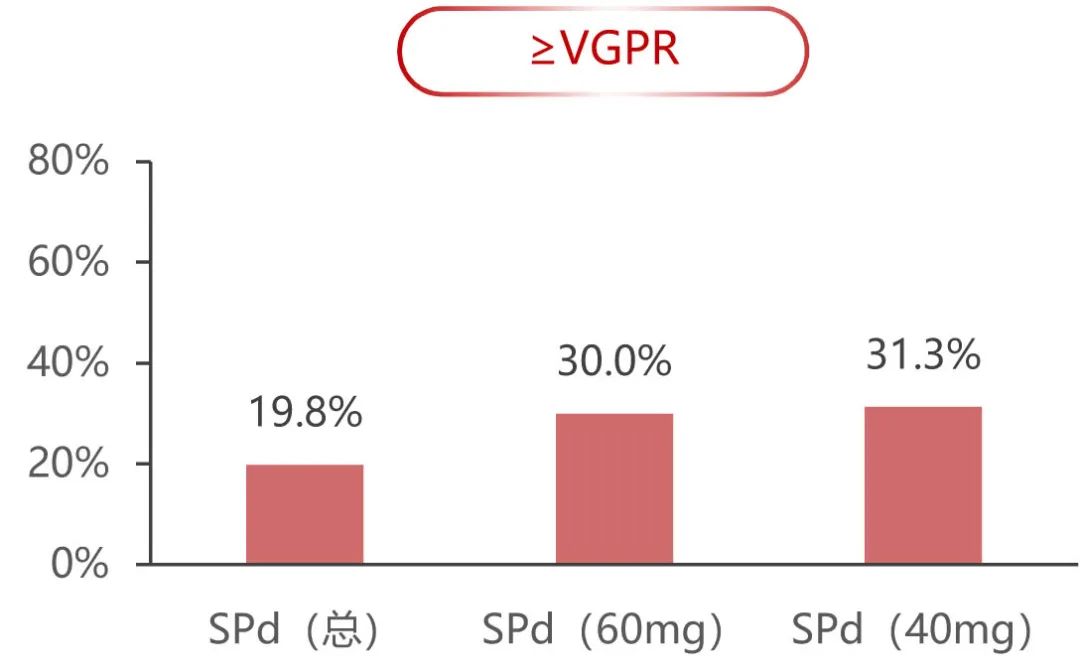
在整个队列中,研究者评估的ORR为39.5%, SPd(60mg)组为55.0%, SPd(40mg)组为43.8%。19.8%患者≥VGPR, SPd(60mg)组和SPd(40mg)分别为30.0%和31.3% 。2例患者达到严格的完全缓解(均为TCE患者), 1例患者达到CR。
在整个队列中,中位至缓解时间为1.1个月。中位治疗持续时间为19.0周, SPd(60mg)组和SPd(40mg)分别22.0周和28.0周。
在整个队列中,塞利尼索的中位相对剂量强度为86.4%(57.5mg/周), SPd(60mg)组为77.5%(46.5mg/周) ;SPd(40mg)组为93.2% (37.3mg/周)。
研究结论
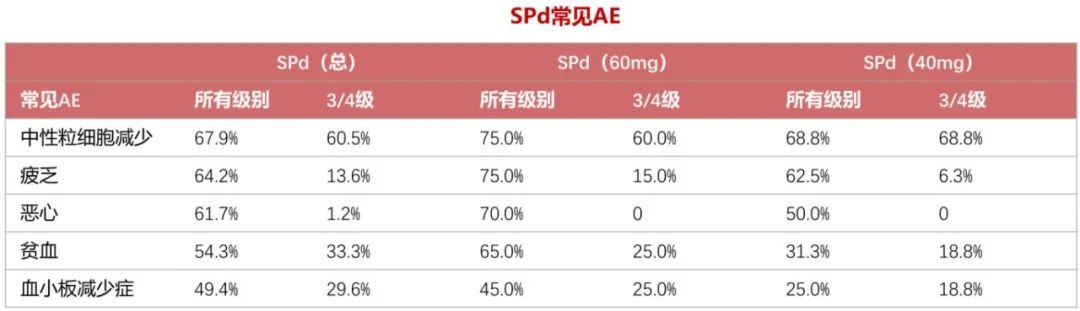
SPd全口服联合方案对RRMM患者展示了初步疗效,总体耐受性良好。SPd(60mg)组的ORR较高,达55.0%,但在SPd(40mg)组AE的发生率较低,暴露持续时间较长,并且达到了较高的剂量强度。
4699
Isatuximab, Pomalidomide, and Dexamethasone (IsaPd) As Salvage Therapy for Patients with Multiple Myeloma: Multicenter, Retrospective Clinical Experience with 262 Cases Outside of Controlled Clinical Trials
Isatuximab联合泊马度胺和地塞米松(IsaPd)作为多发性骨髓瘤患者的挽救治疗:262例对照临床试验之外的多中心、回顾性临床经验
Enrica Antonia Martino
研究目的
在真实世界中,初步探讨Isatuximab 联合泊马度胺和地塞米松(IsaPd)作为挽救性治疗RRMM患者的疗效和安全性。
研究设计
2021年1月至2024年6月,纳入意大利50家医疗中心的262例RRMM患者,至少接受1个周期的IsaPd挽救治疗。患者至少达到部分缓解(PR)为符合缓解标准。
研究结果
IsaPd开始治疗时,143例(54.6%)患者为男性,国际分期系统(ISS) Ⅲ期患者占14.1%。既往中位治疗线数为2线,24.8%的患者为难治。此外,38.9%的患者接受过自体干细胞移植(ASCT), 16.8%既往接受达雷妥尤单抗治疗。高危细胞遗传学异常的患者[ t(4;14), t(14;16), del(17p)、t(14;16)]占30.3%。
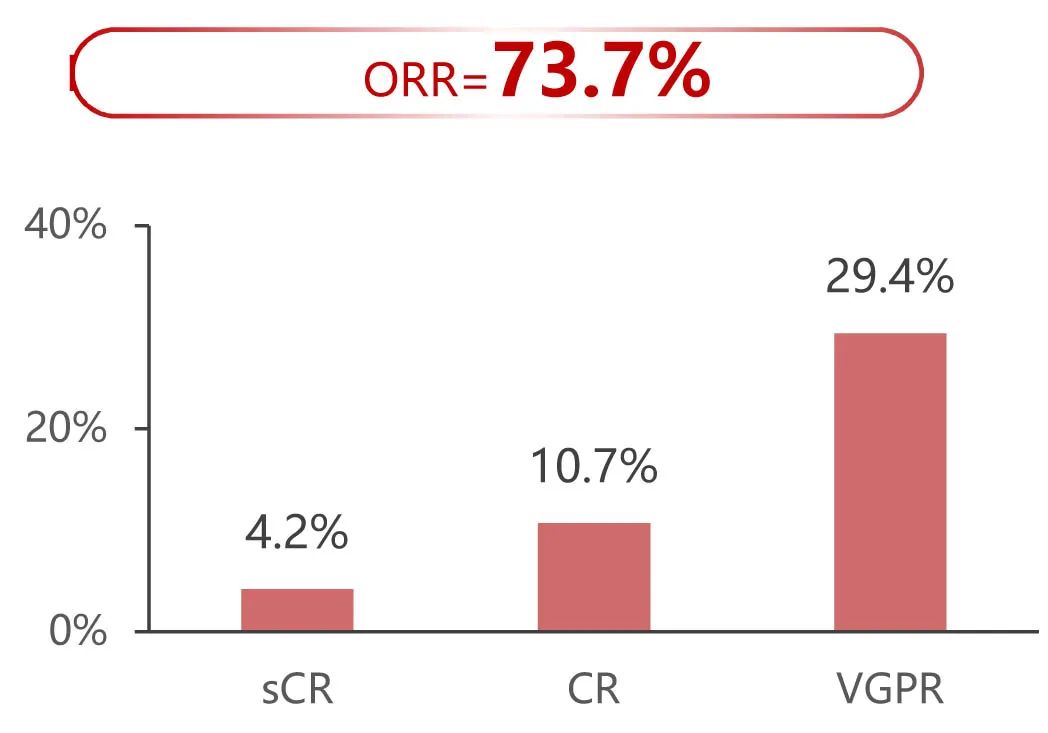
截至2024年6月,所有患者均可评估缓解情况。IsaPd中位治疗周期为11(1-37)。ORR为73.7%,4.2%患者达sCR、10.7%达CR,29.4%达VGPR。
中位随访23.5个月,中位PFS为15.4个月。Cox多变量分析发现高危细胞遗传学异常(HR=2.87;P<0.0001)、乳酸脱氢酶升高(HR=2.35;P=0.003)以及既往达雷妥尤单抗暴露史(HR=2.44;P=0.003)是PFS的独立预后因素。
2年OS率为66.3%。Cox多因素分析显示,高危细胞遗传学异常(HR=2.12,P=0.023)、乳酸脱氢酶升高(HR=3.3;P=0.001)和肌酐清除率<60ml/min (HR=2.48;P=0.007)是OS的独立预后因素。既往达雷妥尤单抗暴露与OS呈趋势相关(HR=2.48;P=0.07)。

研究结论
在真实世界中,证实了IsaPd是既往接受过至少两种方案治疗的RRMM患者可行的挽救治疗方案,具有良好的安全性和有效性,73.7%患者达到缓解。
3782
Efficacy of Isa-Pom-Dex Therapy in Double Refractory Multiple Myeloma (MM) Patients in Real Clinical Practice
IsaPd治疗双重难治多发性骨髓瘤患者的真实世界研究
Maxim Soloviev
研究目的
在真实世界中,评估IsaPd三药联合方案在MM患者中的有效性。
研究设计和人群
2021-2024年,这项前瞻性研究,纳入来自26个中心,接受IsaPd三药联合方案治疗的RRMM患者,共83例。IsaPd开治疗时,17例(18%)患者肾小球滤过率<60ml/min,其中2例接受了血液透析。
既往中位治疗线数为2线,多数患者接受了硼替佐米(99%)和来那度胺(94%)治疗,28%的患者接受过达雷妥尤单抗治疗,18%的患者接受过卡非佐米治疗,10%的患者接受过泊马度胺治疗,8%的患者接受过伊沙佐米治疗,8%的患者接受过elotuzumab治疗,43%的患者接受过自体造血干细胞移植(ASCT)。
从诊断到IsaPd治疗的中位时间为47个月。分析其疗效、结局(复发、进展、死亡)和不良事件。
研究结果
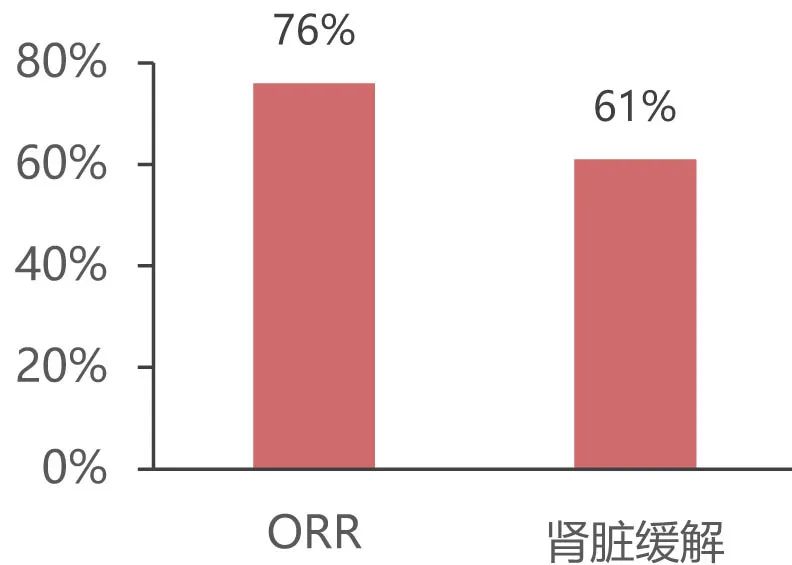
ORR为76%,肾脏缓解率为61%。中位PFS为13.5个月,IsaPd二线治疗中位PFS未达到,三线治疗的中位PFS为14.3个月。既往未经雷妥尤单抗治疗的患者中位PFS显著高于既往达雷妥尤单抗经治患者,分别为28个月和8个月(p<0.05)。3年OS为81%。
IsaPd方案的耐受性良好,最常见的血液学AE为中性粒细胞减少(70%)。2例(2%)患者因AE停用Isatuximab。2例正在接受肾脏替代治疗的CKD 5期患者接受IsaPd治疗;未观察到AE发生率显著增加。
在伴骨事件患者(n=46)中,67%达到一般缓解,12个月PFS为48%,1年O率S为76%。

研究结论
IsaPd三联疗法治疗复发性MM的真实世界研究结果显示,患者缓解、PFS和OS结果与ICARIA注册研究相当,ORR达76%,61%的患者达肾脏缓解,在既往未经达雷妥尤单抗治疗的患者中位PFS为28个月。同时, IsaPd在高龄、体弱、晚期和接受肾脏替代治疗的患者中显示出了有效性。
5153
Pomalidomide, Bortezomib and Dexamethasone in Multiple Myeloma Patients Double Refractory to Lenalidomide and Anti-CD38 Monoclonal Antibodies: A Multicentric Italian Retrospective Study
泊马度胺联合硼替佐米和地塞米松治疗来那度胺和抗CD38单抗双重难治多发性骨髓瘤患者:一项意大利多中心回顾性研究
Carmine Liberatore
研究背景
难治对复发性多发性骨髓瘤患者的预后产生不利影响。自1线治疗以来,持续使用来那度胺和抗CD38单克隆抗体,将导致在1线或2线治疗后,患者对这两药双重难治的比例增加。对于这些患者,尤其是治疗开始后出现早期进展(<12个月)的患者,临床实践中可用的挽救性治疗方案有限。此外,获批药物的大多数临床试验并不包括抗CD38单抗和来那度胺双重难治的患者。
本研究旨在探讨在1线或2线治疗后对IMIDs和抗CD38单克隆抗体双重难治的MM患者中,PVd方案在真实世界中的疗效。
研究设计
一项回顾性研究,纳入意大利20个研究中心,经1线或2线治疗后对来那度胺和抗CD38单抗双重难治的患者,共74例,接受PVd方案治疗。
研究结果
患者发病时中位年龄74岁,高危细胞遗传学异常[t(4;14), t(14;16), del(17p) , gain/ampl(1q21)]患者31例(42%)。9例(12.2%)伴髓外病变。
77%(57例)的患者因症状复发而开始PVd治疗,23%(17例)的患者因生化复发而开始PVd治疗。从诊断到PVd开始治疗的中位时间为21个月,36例(48.6%)处于DRd病程早期进展(<12个月)。中位随访5.7个月,PVd治疗中位周期数为6周期。至最佳缓解中位时间为2.9个月。
ORR为75% (CR:20%, VGPR:27%, PR:28%),PVd治疗后中位PFS为8个月,中位OS为17.8个月。
单因素分析未发现PFS与从诊断到开始接受PVd治疗的时间或获得双难治状态前的治疗线数(1线vs2线)之间存在显著相关性(所有P值>0.7)。PVd治疗缓解率与预后呈正相关(P=0.021),与<VGPR的患者相比,≥VGPR的患者的PFS更长(HR=3.1;P=0.008)。安全特征与OPTISMM数据一致。

研究结论
本研究是首个在真实世界中探索PVd治疗IMIDs和抗CD38单抗双重难治MM患者疗效的研究。PVd治疗来那度胺和抗CD38单抗双重难治MM安全性良好,并获得了显著的缓解率,ORR达75%,20%的患者达到完全缓解。
495
Teclistamab, Daratumumab, and Pomalidomide in Patients with Relapsed/Refractory Multiple Myeloma: Results from the Majestec-2 Cohort a and Trimm‑2 Studies
特立妥单抗联合泊马度胺和达雷妥尤单抗治疗RRMM:Majestec-2队列a和Trimm-2研究结果
Anita D'Souza
研究背景
达雷妥尤单抗(D)和泊马度胺(P)均具有免疫调节作用,可增强特立妥单抗(Tec)的作用,从而提高抗骨髓瘤活性。在此报告了2项关于Tec-DP治疗MM的Ib期研究(MajesTEC-2,NCT04722146;TRIMM‑2,NCT04108195)的安全性和有效性。
研究设计
MajesTEC-2队列的符合条件患者既往接受过1-3线治疗,包括PIs和来那度胺;TRIMM-2队列的符合条件患者既往接受过≥3线治疗(包括PI和IMiDs,或者PI和IMiD双重难治)。患者接受每周1次的Tec(0.72、0.75或1.5mg/kg,采用剂量递增给药[SUD])联合D(1800mg)和泊马度胺(2或4mg)治疗。泊马度胺在完成SUD后开始使用。
研究结果
共纳入27例患者接受Tec-DP治疗(TRIMM-2研究,n=10;MajesTEC-2研究,n=17)。数据截止时,中位随访时间为25.8个月,Tec-DP的中位持续治疗时间为12.0个月。既往中位治疗线数为2,其中33%的患者既往治疗线数超过3线;40.7%的患者曾接受过达雷妥尤单抗治疗。
25例(92.6%;3/4级:63.0%)患者报告感染。所有致死性感染均发生在实施加强感染预防计划之前,该计划强调补充静脉注射用免疫球蛋白( IVIg )。自该计划实施以来,未再发生致死性感染。
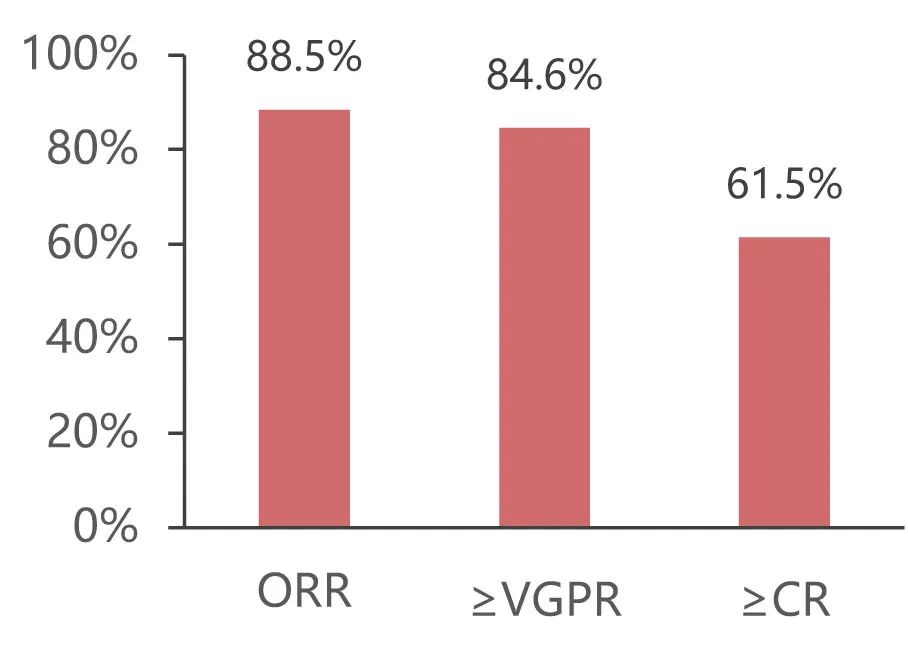
ORR为88.5%,达到≥VGPR为84.6%,达到≥CR为61.5%。中位至首次缓解时间为0.95个月。中位缓解持续时间无法估计(NE;12.2个月-NE)。中位PFS为26.5个月。初步数据显示,Tec的血清浓度通常与MajesTEC-1研究中Tec单药治疗观察值处于同一范围内。

研究结论
Tec-DP方案在RRMM(包括双重难治)患者中具有可行性,具有高缓解率,89%的患者达到缓解,61.5%的患者达到完全缓解,中位PFS达26.5个月。
594
Pharmacodynamic Signatures and Correlatives of Response in Patients with Relapsed/Refractory Multiple Myeloma (RRMM) Treated with Talquetamab or Teclistamab Plus Daratumumab and Pomalidomide
Tec-DP或Tal-DP治疗的RRMM的药效学特征和相关反应
Deeksha Vishwamitra
研究背景
旨在深入了解Talquetamab联合达雷妥尤单抗和泊马度胺(Tal-DP)治疗方案的潜力,评估TRIMM-2(NCT04108195)研究中接受tal-DP方案治疗患者的免疫药效学特征、疗效相关指标以及与临床结局的相关性。
研究设计
既往接受过≥3线治疗的RRMM患者接受tal 0.4mg/kg 每周一次(QW)或0.8mg/kg 每两周一次(Q2W)治疗,并逐步递增剂量,并联合达雷妥尤单抗1800mg和泊马度胺2mg治疗。通过流式细胞术分析基线时和治疗期间采集的外周血样本,分析了其与PFS、DOR和最佳缓解(完全缓解[CR]/严格完全缓解[sCR]、部分缓解[PR]/非常好的部分缓解[VGPR]以及疾病稳定[SD]/疾病进展[PD])的相关性。
研究结果
纳入77例患者(tal QW,n=18;tal Q2W,n=59;CR/sCR,n=37;VGPR/PR,n=24;SD/PD,n=6)。
Tal-D显示出互补的药理作用,包括在第1周期中T细胞边缘化、绝对T细胞恢复增加、效应记忆细胞扩增以及初始CD8 T细胞减少,这些作用在第2周期加入泊马度胺后得到增强。
虽然达雷妥尤单抗治疗导致CD38+ CD8 T细胞减少,但加用tal可诱导这一亚群的激活。泊马度胺给药后,CD8 T细胞上的CD38再次诱导,表明T细胞被重新刺激。达雷妥尤单抗减少了免疫抑制性CD38+调节性T细胞(Tregs),而加入泊马度胺恢复了达雷妥尤单抗减少的自然杀伤细胞(NK细胞)。
亚组分析显示,tal-DP对既往接受过双特异性抗体(BsAb)治疗的患者有显著影响。尽管这些患者在基线时表现出T细胞功能更差、更衰竭的表型,但与未接受过BsAb治疗的患者相比,tal-DP导致的CD8 T细胞扩增、NK细胞恢复、CD38+T细胞活化、CD38+调节性T细胞(Tregs)下调更为显著。
tal-DP深度缓解者的绝对CD8 T细胞恢复更早、程度更大,与更长的PFS和DOR相关,尤其是在加入泊马度胺后。tal-D后,所有缓解组的NK细胞减少程度相当;然而,深度缓解患者在加入泊马度胺后出现NK细胞恢复。虽然加入达雷妥尤单抗后CD38+ CD8 T细胞最初减少,但深度缓解患者在加入tal后CD38+ CD8 T细胞激活程度更高,且在给予泊马度胺后持续存在。
NK细胞绝对计数和CD38+ CD8 T细胞的最大倍率变化越高,PFS和DOR改善的趋势越明显,尤其是第2周期加入泊马度胺后。
最后,在获得深度缓解的患者中观察到CD8 T细胞上共抑制受体的持续表达减少,而在所有接受tal-DP治疗的患者中绝对CD38+调节性T细胞(Tregs)均减少。
tec-DP的初步结果与tal-DP的结果具有相似性,进一步的分析正在进行中。
研究结论
Tal-DP通过互补的作用机制产生深度、持久疗效,对于既往接受过双特异性抗体(BsAb)治疗的患者可能尤其有益。
总结
基于泊马度胺联合方案对于多重难治患者提高缓解率,延长生存,进一步提升患者获益。
-
SPd全口服方案在IMiDs,PI,抗CD38单抗双重或三重难治患者中可快速达到缓解,中位至缓解时间为1.1个月,ORR达55%(60mg组)。
-
IsaPd 作为RRMM挽救治疗,73.7%的患者达到缓解,其中4.2%患者达到sCR,10.7%的患者达到CR,中位PFS为15.4个月,2年OS率为66.3%。
-
IsaPd治疗双重难治患者ORR达76%,肾脏缓解率达61%,中位PFS为13.5个月,3年OS率达81%。在未经Dara治疗的亚组患者中PFS达28个月。
-
PVd治疗来那度胺和抗CD38单抗双重难治患者ORR达75%,其中20%的患者达到完全缓解,中位OS达17.8个月。
-
泊马度胺可增强双特异性抗体和抗CD38单抗抗MM作用,逆转达雷妥尤单抗的NK细胞减少,恢复CD8 T细胞功能,泊马度胺可显著改善双特异性抗体和达雷妥尤单抗的PFS和DOR。
-
特立妥单抗联合泊马度胺和达雷妥尤单抗治疗PI和IMiDs双重难治患者可快速达到缓解,中位至首次缓解时间仅为0.95个月,88.5%患者达到缓解,其中61.5%的患者≥CR。中位PFS达26.5个月。
参考文献
1.Baljevic M, et al. 2024ASH. abstract 1996.
2.Martino EA, et al. 2024ASH.abstract 4699.
3.Soloviev M, et al. 2024ASH.abstract 3782
4.Liberatore C, et al. 2024ASH. Abstract 5153.
5.D'Souza A, et al. 2024ASH. Abstract 495.
6.Vishwamitra D, et al. 2024ASH. Abstract 594.


