中国学者领衔!最新Nature Biotechnology,偶联物,跨越血脑屏障!
时间:2024-11-27 15:01:05 热度:37.1℃ 作者:网络
静脉注射可跨越血脑屏障偶联物促进生物大分子向中枢神经系统的转运
生物大分子的脑部递送与血脑屏障
寡核苷酸等生物大分子已被用于多种治疗应用。然而,由于血脑屏障(BBB)的存在,高效安全地将这些生物大分子输送到脑组织仍然是一个巨大的挑战。在过去的几十年里,研究人员探索了各种将寡聚物输送到大脑的策略。例如,开发了一种二价小干扰RNA(siRNA)结构,用于通过脑脊液注射有效沉默动物体内的亨廷顿基因。胆固醇或α-生育酚结合可增强DNA/RNA异源双链体向脑组织的运输。siRNA与棕榈基修饰的结合也被证明可以通过鞘内或侧脑室注射有效地沉默中枢神经系统(CNS)中的基因。最近,在动物模型中,与人转铁蛋白受体1(TfR1)结合的Fc片段被证明可以穿过血脑屏障并递送反义寡核苷酸(ASO)。尽管取得了这些重要进展,但仍然迫切需要开发技术来克服血脑屏障,并通过全身给药加强生物大分子疗法向中枢神经系统的输送。
可跨越血脑屏障的缀合物
在最新的研究中,西奈山伊坎医学院Yizhou Dong和Eric J. Nestler等人开发了一种可跨越BBB的偶联物(BCC)系统,该系统可通过γ-分泌酶介导的转胞吞作用促进向中枢神经系统的递送。在野生型小鼠、人脑组织和肌萎缩侧索硬化症小鼠模型中,静脉注射BCC10-寡核苷酸偶联物证明了寡核苷酸可跨越血脑屏障上进行有效运输和基因沉默。相关工作以“Intravenous administration of blood–brain barrier-crossing conjugates facilitate biomacromolecule transport into central nervous system”为题发表在Nature Biotechnology。

【文章要点】
先前的研究已经证明,各种活性受体介导的跨细胞摄取方法通过全身给药可促进药物跨越血脑屏障,其中的典型例子包括位于血脑屏障管腔膜上的TfR、低密度蛋白受体和胰岛素受体。这些受体可以启动内吞过程,形成进入大脑的转胞小泡。受此启发,作者设计一个模块化系统,该系统能够通过使用各种跨细胞途径经血脑屏障静脉注射(i.v.)到中枢神经系统来增强生物大分子疗法的递送。为了实现这一目标,作者概念化了一个系统,即将特定的小分子跨BBB试剂与生物大分子共价偶联(图1)。

图1 BCC的设计和特性
具体而言,基于能够穿越血脑屏障的小分子配体的结构和功能,作者设计并合成了四类BCCs,包括肉桂酸衍生物、色胺衍生物、MK-0752衍生物和SR-57227衍生物。其中,肉桂酸衍生物可以穿过血脑屏障,与淀粉样β(Aβ)的β-折叠相互作用。胰蛋白酶衍生物依靠Mg2+和三磷酸腺苷积极转运到大脑中。MK-0752是一种γ分泌酶抑制剂,能有效穿过血脑屏障并减少aβ的产生。SR-57227可以与5-HT3受体相互作用,促进其转运到大脑中。每一类合成的BCC都由与Cy5荧光成像探针连接的双天线和三天线小分子试剂组成。以BCC10-Cy5分子的合成为例,经过三(羟甲基)-氨基甲烷与丙烯酸叔丁酯的反应,然后与Fmoc-GABA缩合并随后脱保护,缩合再进行Fmoc脱保护,得到BCC10。BCC10与Cy5-NHS发生偶联反应,得到BCC10-Cy5。为了测试这一缀合物概念,作者将这些BCC–Cy5化合物静脉注射到小鼠体内,并量化了所给BCC–Cy5在大脑中的积累。与游离Cy5相比,大多数BCC-Cy5化合物导致每克脑注射剂量百分比(%ID/g)增加。特别是,三天线肉桂酸衍生物、色胺衍生物和SR-57227衍生物的百分比分别比游离Cy5高62.5倍、97.0倍和141.8倍。总的来说,与双天线BCC相比,三天线BCC显示出更优的BBB穿透率。来源于三天线MK-0752的BCC10在小鼠大脑中的积累比游离Cy5高220.5倍(图2)。
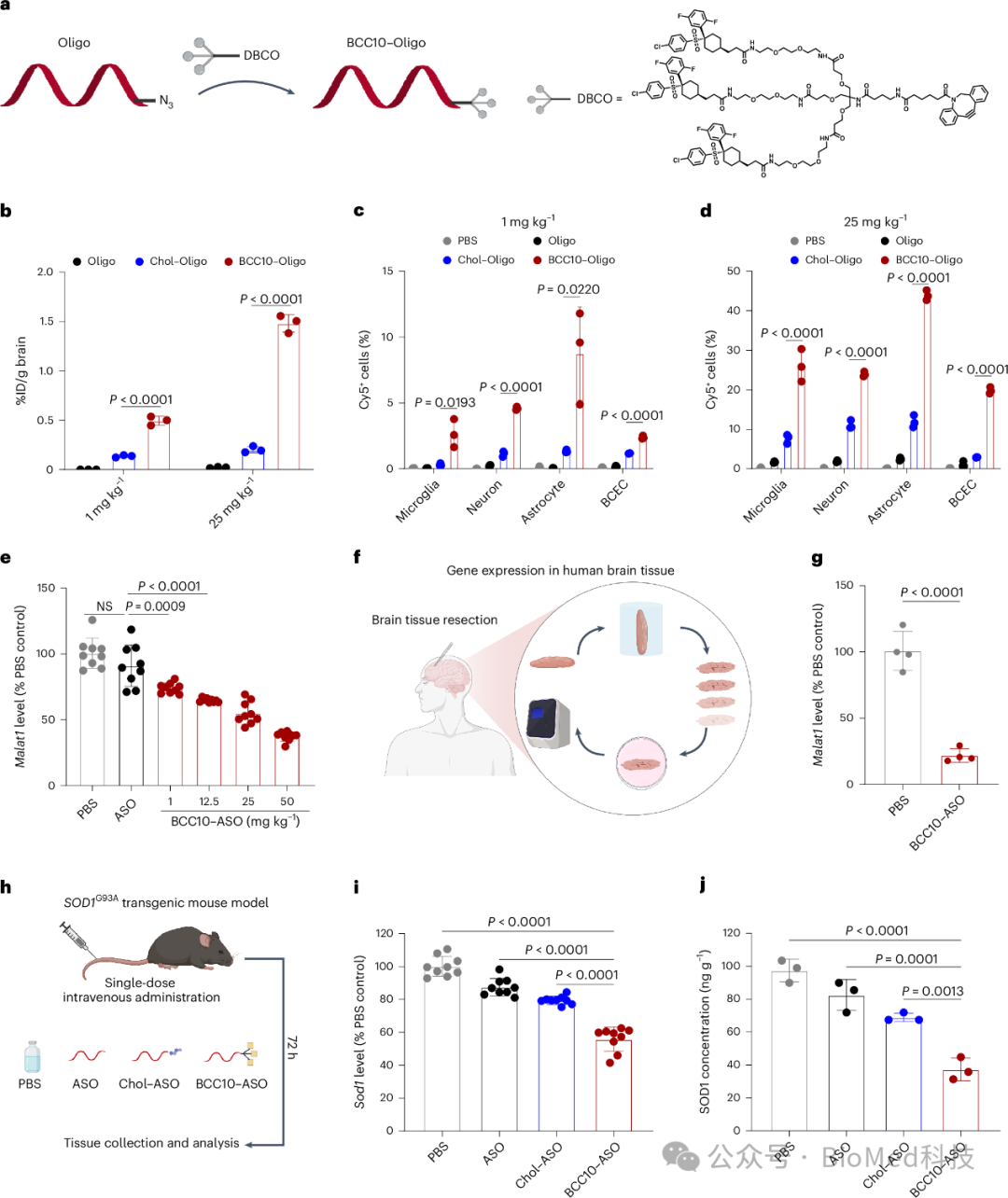
图2 BCC10在小鼠体内增强寡核苷酸的血脑屏障渗透
特别是,作者揭示BCC10是通过γ-分泌酶介导的转胞作用而成功穿过血脑屏障并递送功能性生物大分子的。更重要的是,BCC10不仅安全地将不同类型的反义寡核苷酸(ASO)递送到大脑中,而且增强了多种小鼠模型和离体人脑组织中基因沉默的功效。此外,作者还进行了试点研究,以探索BCC系统用于蛋白质递送的可能性。在实验中,作者分别将BCC10与mCherry和TAT-Cre重组酶(Cre)结合。结果表明,BCC10-mHerry显著增强了mCherry向大脑的运输(相对于mCherry增加3.9倍)。根据流式细胞术分析,在Ai14小鼠模型中,BCC10-Cre比游离Cre在多种脑细胞类型上产生了更有效的编辑。根据所提供的数据,BCC系统是一种高效的系统,可用于在大脑中全身递送生物大分子。
结论与展望
作者最后指出,为了实现上述BCC系统在临床转化中的潜力,详细的研究是必不可少的。这应该包括对大脑和细胞运输的机制研究实验,以及对其安全性和有效性的全面评估。此类研究对于探索这种递送系统在治疗一系列中枢神经系统疾病(如ALS、AD、缺血性卒中、多发性硬化症和药物成瘾)方面的特征和治疗潜力至关重要。总体而言,BCC系统为克服生物大分子输送到大脑的挑战提供了巨大的希望,并为未来治疗中枢神经系统疾病提供了策略。
文献链接:
https://www.nature.com/articles/s41587-024-02487-7


