涨知“食”,这几种吃法是阿尔兹海默病的克星还是救星?
时间:2022-10-30 20:37:12 热度:37.1℃ 作者:网络
中国有句古话“民以食为天”,饮食在百姓心中的地位十分深厚。孔子曾说过:“君子食无求饱”,我国自古便十分重视饮食有度、有节。随着生活水平的提高,除了吃得开心、吃得幸福外,人们也越来越重视饮食健康。
阿尔茨海默病(Alzheimer’sdisease,AD)是一种起病隐匿、呈进行性发展的神经系统退行性疾病,号称威胁老年人健康的“第四大杀手”,是无数家庭的“不能承受之重”。令人心痛的是,病因迄今未明。
越来越多的研究表明,健康的生活方式或能降低罹患AD的风险。“进食”作为人体获取能量的途径,也是最受自身控制的生活方式行为,引起国内外学者极大关注,研究者们试图从中找到打开阿尔兹海默症宝盒的“神奇密码”。近日,发表在iScience杂志上的一篇研究显示,低进食频率可能通过减少脑淀粉样蛋白沉积而降低AD风险,这一发现为通过调整进食频率来预防AD的相关策略提供了线索。

Doi:https://doi.org/10.1016/j.isci.2022.105422
该研究将411名非痴呆老年人根据饮食频率分为2组,低饮食频率组139人(Low Meal Frequency,LMF,每天进食次数小于3次)和高饮食频率组272人(High Meal Frequency,HMF,每天进食次数为3次)。对Aβ蛋白的沉积情况以及Aβ蛋白阳性率分析表明,LMF组老年人大脑中Aβ蛋白沉积和Aβ蛋白阳性率显著低于HMF组。
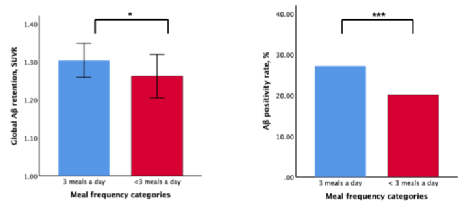
LMF组和HMF组大脑Aβ蛋白沉积和Aβ蛋白阳性率
然而,影响进食频率和AD之间关系的潜在影响因素有很多,包括终身体力活动(lifetime physical activity, LPA)、终身认知活动、职业复杂性、年收入、体重指数(BMI)等。通过对参与者的调查问卷的分析发现 LPA与进食频率密切相关,而其他变量与进食频率之间无显著相关性,提示LPA可调节进食频率和总体Aβ蛋白沉积之间的关系。进一步的分析显示,只有在低LPA的老年人中LMF与Aβ蛋白沉积之间具有显著相关性,在高LPA的老年人中二者没有显著关系。我们可以理解为增加体力活动后,即使吃的多可能也不会导致Aβ蛋白沉积增加。而对于体力活动较少的人群,推荐LMF饮食。
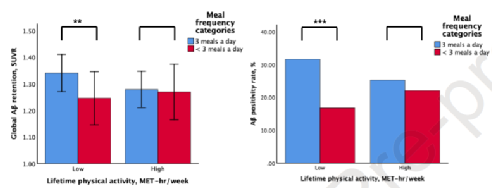
不同LPA水平分组中LMF和HMF对Aβ蛋白沉积和Aβ蛋白阳性率的影响
那么LMF是通过什么方式降低了大脑中Aβ沉积呢?血清饥饿素(ghrelin)是一种促食欲激素,通过与生长激素促分泌受体(GHS-R)结合调节进食。已有的动物实验结果表明血清饥饿素升高在AD中具有保护作用,但是在人体中的作用还不清楚。进一步分析结果显示,LMF组血清饥饿素的水平显著高于HMF组,该激素与大脑Aβ蛋白沉积呈负相关关系。如果将血清饥饿素作为一个协变量,再去评估进食频率和Aβ蛋白沉积之间的关系时,二者无显著性关系。这说明LMF可能是通过上调血清饥饿素的水平,减少大脑Aβ蛋白沉积。
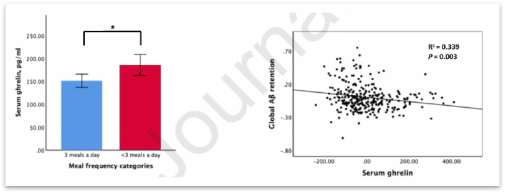
LMF组和HMF组血清饥饿素水平及血清饥饿素水平与Aβ蛋白沉积的相关性
这项研究结果向我们发出警告,有时候能吃不一定是“福”!看来以后加餐之前要好好想一想了。在科研届亦或养生圈,有一种饮食模式有着异曲同工之妙,那便是禁食。2022年9月发表在Cell Reports的一篇研究报告,题为“Fasting-mimicking diet cycles reduce neuroinflammation to attenuate cognitive decline in Alzheimer's models”,选用两种AD转基因小鼠模型,给予每月两次为期5天的模仿禁食饮食(Fasting-mimicking diet,FMD)周期,以探究FMD对阿尔兹海默症的影响。需要指出的是,FMD是一种低卡路里/低蛋白质但高不饱和脂肪的饮食,与长时间禁食(只能喝水)相比,整体更加安全可控。
结果不出所料,研究者发现FMD周期可以改善小鼠的视觉注意力、工作记忆和空间记忆,缓解焦虑行为,并增加探索活动。那么具体机制又是什么呢?进一步研究发现,FMD周期降低了AD关键病理标志物的水平,包括Aβ和过度磷酸化的tau蛋白,以及小胶质细胞密度和神经炎症标志物,以改善小鼠认知功能,延缓病情进展。科学需要时间验证,FMD的饮食周期在人类患者身上是否安全有效仍需大型的临床研究和数据来支撑。关于这篇报告的详细解读已于10月4日在本公众号发布,感兴趣的伙伴可以移步阅读哦!
“吃饭减三口,活到九十九”,老祖宗传下来的话果然充满大智慧。健康需要节制,很多小伙伴可能要说,美食实在太多了,我忍不了啊!尤其是炸鸡汉堡红烧肉,一口咬下去香的流油……在梦里都在向我招手。不要急,下面这篇报告可能会让你管住自己的“口腹食欲”。
随着生活水平的提高,高热、高脂食物成为人们日常饮食中必不可少的一部分,三高发病率逐年攀升。研究表明,糖尿病是阿尔茨海默病(AD)的危险因素,但是糖尿病引起AD发病的分子机制尚不完全清楚。2型糖尿病表现为高血糖、胰岛素抵抗和外周炎症,而慢性炎症已被证实在AD的发病中起关键作用。2022年5月发表在Molecular Psychiatry杂志的题为“High-fat diet-induced diabetes couples to Alzheimer’s disease through inflammation-activated C/EBPβ/AEP pathway”的研究报告,发现高脂肪饮食(High-Fat Diet,HFD)引起的肥胖和糖尿病相关的炎症激活了神经元C/EBPβ/AEP信号,伴随显著的Aβ蛋白和过度磷酸化的Tau蛋白在大脑中积累,驱动AD的发生和认知障碍。该研究为通过管理糖尿病改善一般人群AD的发生及进展提供了新的理论依据,也告诫我们高脂食物可以吃,但不要贪多哦。
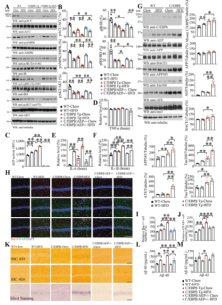
敲除Thy1-C/EBPβ转基因小鼠的AEP可缓解HFD诱导的神经炎症和AD病理
正如上文所叙述的那样,有些食物吃多了可能会慢慢毁掉我们的大脑,与此同时,有些东西吃少了也会对大脑造成不利影响。大脑作为人体最重要的器官之一,营养物质的补充对其健康举足轻重。
胆碱是与大脑发育密切相关的一种营养素,其与认知的积极关联在动物和人类研究中都有报道。动物实验表明饮食中补充胆碱可改善小鼠大脑中β淀粉样蛋白沉积、小胶质细胞活化及认知功能。然而胆碱与人类阿尔茨海默病(AD)之间的关系尚不清楚。
2022年8月,一篇刊登在Am J Clin Nutr杂志的研究报告,题为“Is dietary choline intake related to dementia and Alzheimer’s disease risks? Results from the Framingham Heart Study”,通过对来自Framingham心脏研究参与者进行长期随访及评估,以探究胆碱摄入量与痴呆和AD的发生之间是否存在关系。结果发现,中等程度的胆碱摄入量的参与者患痴呆和AD的风险最低,低胆碱摄入量与痴呆和AD发病风险增加相关,但并未阐明高胆碱饮食与AD之间的关系,有待进一步探索。
除了上述提到的进食模式外,MIND饮食、地中海饮食、生酮饮食等也是热门的研究方向,有兴趣的小伙伴可以查阅起来!虽然战胜阿尔兹海默病的路途道阻且长,但是我们始终要相信:行则将至!
最后,希望能够早日破解阿尔兹海默病的难题,也愿所有的老人都能安享晚年。
参考文献:
[1] Kim, J.W., Byun, M.S., Yi, D., et al. Association of low meal frequency with decreased in vivo Alzheimer’s pathology, ISCIENCE (2022).
[2] Rangan P, Lobo F, Parrella E, et al. Fasting-mimicking diet cycles reduce neuroinflammation to attenuate cognitive decline in Alzheimer's models. Cell Rep(2022).
[3] Liu, P., Wang, ZH., Kang, S.S. et al. High-fat diet-induced diabetes couples to Alzheimer’s disease through inflammation-activated C/EBPβ/AEP pathway. Mol Psychiatry (2022).
[4] Yuan J., Liu X, Liu CY., et al. Is dietary choline intake related to dementia and Alzheimer's disease risks? Results from the Framingham Heart Study, The American Journal of Clinical Nutrition(2022).


