羟氯喹阻断SARS-CoV-2进入哺乳动物细胞培养中的内吞途径
时间:2022-10-26 08:59:26 热度:37.1℃ 作者:网络
目前,全世界已有数百万人感染了SARS-CoV-2。针对严重症状的拟议治疗方法包括众所周知的FDA批准的抗疟和抗炎药氯喹(CQ)及其衍生物羟氯喹(HCQ),但它们的作用机制在人类细胞中知之甚少。
HCQ在SARS-CoV-2感染性中的作用机制模型:

在针对COVID-19重症患者的多项研究中,血液中的胆固醇似乎很低。然而,在同一患者的单核细胞中测量的细胞胆固醇浓度升高,表明在疾病的晚期阶段血液和组织出现相反的结果。重要的是,胆固醇的合成和对免疫细胞的摄取是炎症的关键影响因素。胆固醇转运蛋白载脂蛋白E(apoE)将胆固醇装载和卸载到细胞膜和从细胞膜卸载胆固醇,使我们能够在体外和体内操纵胆固醇水平。
胆固醇决定了羟氯喹在肺细胞中的作用:
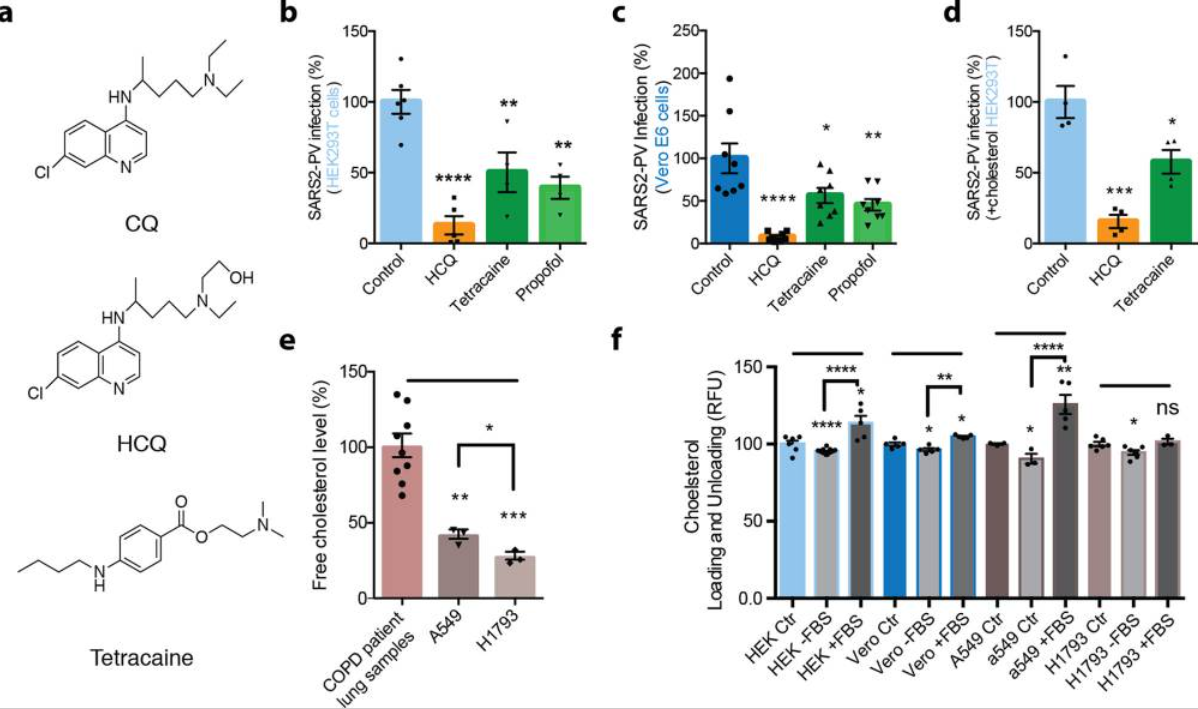
有趣的是,CQ是一种麻醉剂 - 皮下注射CQ产生足以执行外科手术的即时局部麻醉。此外,CQ和局部麻醉剂丁卡因都是疏水性的,并且含有叔胺。由于CQ和局部麻醉剂(如丁卡因)是弱碱,它们的摄取会改变膜内的酸碱平衡。此外,常见的局部麻醉剂(如甲哌卡因、布比卡因和丁卡因)和其他GM1簇干扰化合物(如甾醇和环糊精)可以发挥抗病毒或抗菌活性。萜类化合物也可以破坏病毒的进入;这个过程是胆固醇依赖性的。
麻醉剂和羟氯喹抑制SARS2-PV进入培养细胞:
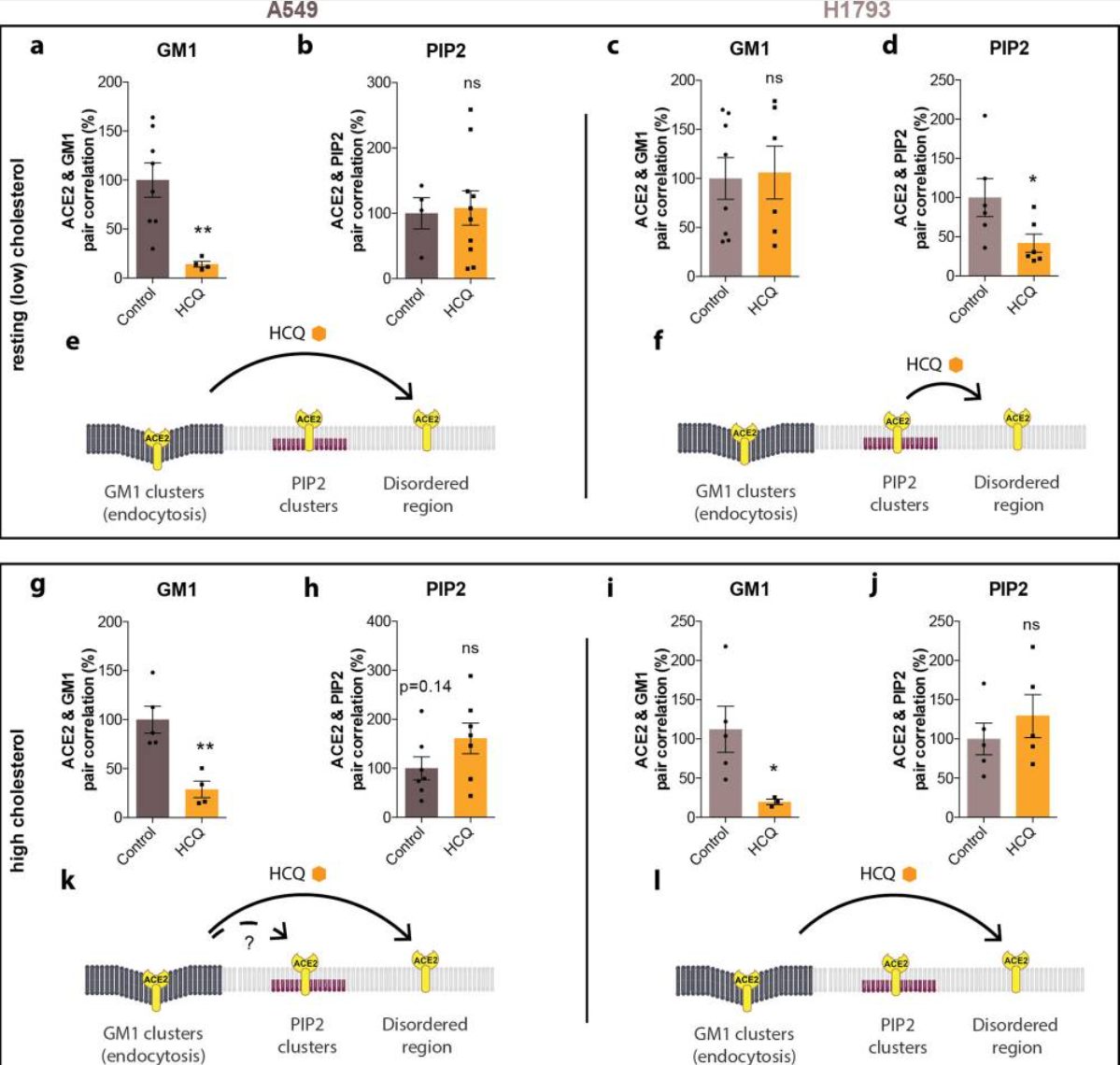
在体外,HCQ有效地抑制病毒进入,但其在临床中的使用受到相互矛盾的结果的阻碍。最近,麻醉剂被证明可以破坏单唾液四十六烷基神经节苷脂1(GM1)脂质的有序簇。这些相同的脂质簇将SARS-CoV-2表面受体血管紧张素转换酶2(ACE2)招募为内吞脂质,远离磷脂酰肌醇4,5双磷酸(PIP2) 群集。在这里,研究者采用培养的哺乳动物细胞(VeroE6,A549,H1793和HEK293T)的超分辨率成像来显示HCQ直接扰动ACE2受体与内吞细胞脂质和PIP的2集群。在升高(高)胆固醇时,HCQ使ACE2纳米镜距离远离内吞脂质。在静息(低)胆固醇的细胞中,ACE2主要与PIP相关2群集和 HCQ 使 ACE2 远离 PIP2簇—红霉素具有类似的作用。
羟氯喹从肾细胞中的GM1和PIP2簇中取代ACE2:
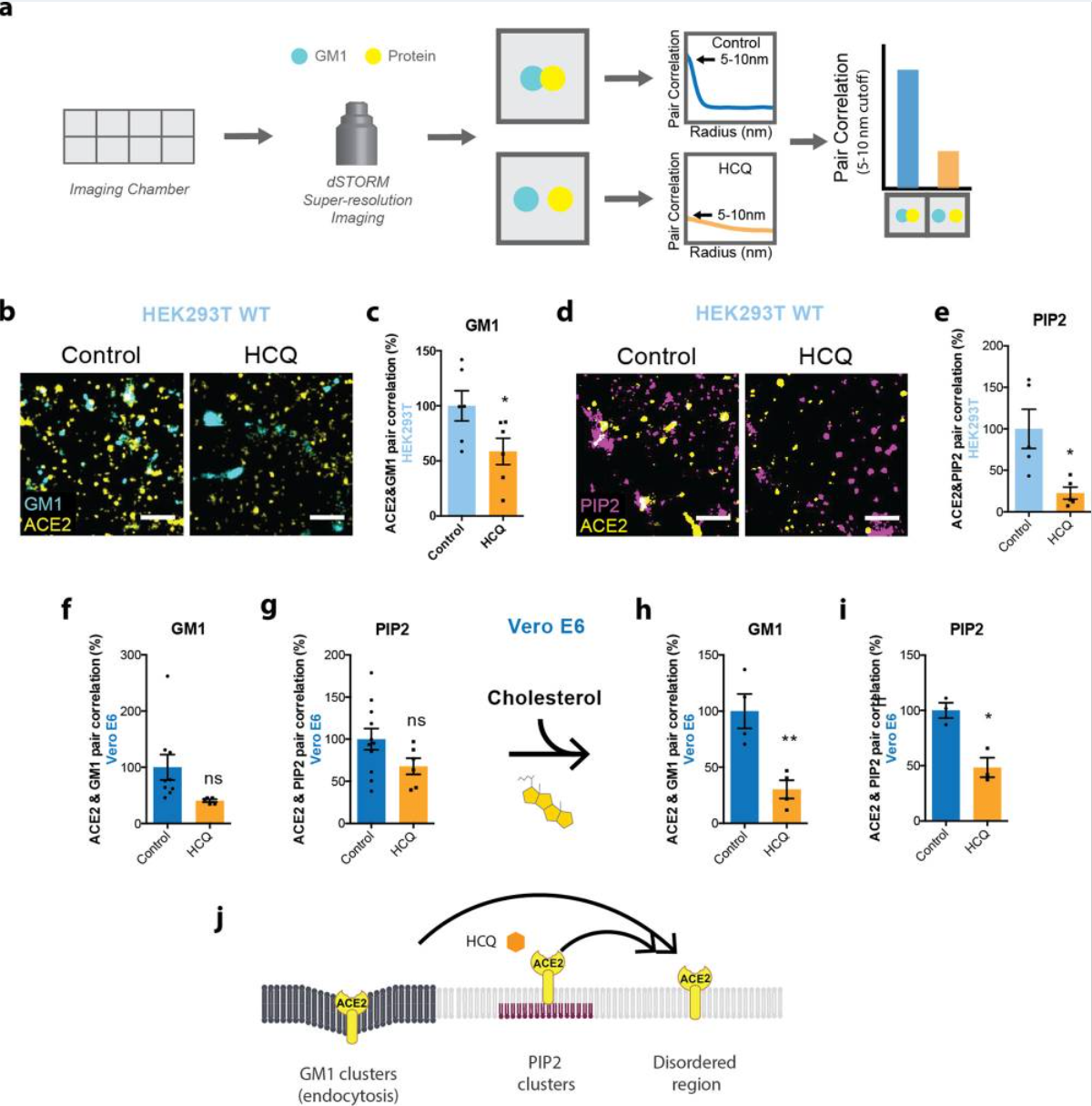
因此,研究者得出结论,HCQ通过高和低组织胆固醇中的两种不同机制抑制病毒进入,并且在抑制组织蛋白酶-L之前这样做。HCQ临床试验和动物研究在评估剂量和疗效时需要考虑组织胆固醇水平。
参考文献:Yuan Z, Pavel MA, Wang H, Kwachukwu JC, Mediouni S, Jablonski JA, Nettles KW, Reddy CB, Valente ST, Hansen SB. Hydroxychloroquine blocks SARS-CoV-2 entry into the endocytic pathway in mammalian cell culture. Commun Biol. 2022 Sep 14;5(1):958. doi: 10.1038/s42003-022-03841-8. PMID: 36104427; PMCID: PMC9472185.



