来那度胺联合奥妥珠单抗和CHOP治疗初治DLBCL的初步探索
时间:2022-11-18 20:54:20 热度:37.1℃ 作者:网络
LO-CHOP方案
R-CHOP方案是弥漫大B细胞淋巴瘤(DLBCL)的标准一线治疗方案,在其基础上加入其他药物(R-CHOP+X)已有多次尝试,但来那度胺、伊布替尼或硼替佐米等均未优于R-CHOP,包括用奥妥珠单抗(O)代替R的方案也告失败。
奥妥珠单抗是一种靶向 CD20 的糖工程化 II 型抗体,与利妥昔单抗相比可提高抗体依赖性细胞毒性、吞噬作用和直接细胞死亡,来那度胺是免疫调节剂,可激活干扰素信号、抑制NF-κβ通路并提高NK细胞活性。来那度胺和奥妥珠单抗均未纳入DLBCL的一线治疗,但它们联合给药可产生协同作用,可能的机制在于联合给药时活化NK 细胞逆转和未成熟 NK 细胞表型。
MD安德森癌症中心Jason Westin教授等假设,来那度胺和奥妥珠单抗联合 CHOP 化疗将表现出较高的疗效和可耐受的毒性特征,并开展了一项LO-CHOP 治疗新诊断 DLBCL 患者的 Ib/II 期单中心临床试验 (NCT02529852),其中还包括循环肿瘤 DNA (ctDNA) 分析,以测量基线肿瘤负荷、分子学缓解和分子亚型。该研究结果近日发表于《Blood Advance》。

研究设计
本研究为研究者发起、单臂、Ib/II 期研究,Ib期部分主要考察安全性,II期部分主要在LO-CHOP治疗后评估疗效(Lugano 2014根据PET/CT评估的ORR和CR)。
纳入患者为≥18岁的新诊断、未经治疗的CD20 + DLBCL患者、影像学最长直径≥1.5 cm的可测量疾病,ECOG PS评分≤2(或既往 PS 为0-1但因淋巴瘤导致恶化,且可通过治疗逆转),器官和骨髓功能充足。
21天/周期,第1-14天每日口服来那度胺15mg,第1周期的第1、8和15天以及后续周期的第1天静脉注射 (IV)奥妥珠单抗1000 mg,联合标准CHOP(所有周期的第1天开始,环磷酰胺750 mg/m2、多柔比星50 mg/m2、长春新碱1.4 mg/m2[最高2.0 mg]、和泼尼松100 mg口服第1-5天每日一次)。计划所有患者共接受6个周期的治疗。要求所有患者接受粒细胞集落刺激因子、阿司匹林81 mg(如果尚未接受抗凝治疗)和耶氏肺孢子虫肺炎预防治疗。如果患者因标危因素存在 CNS 受累风险,则允许进行鞘内化疗。
本研究还评估了循环肿瘤DNA (ctDNA,PhasED-Seq 检测),包括基线、治疗2周期后和治疗结束时。
研究结果
患者
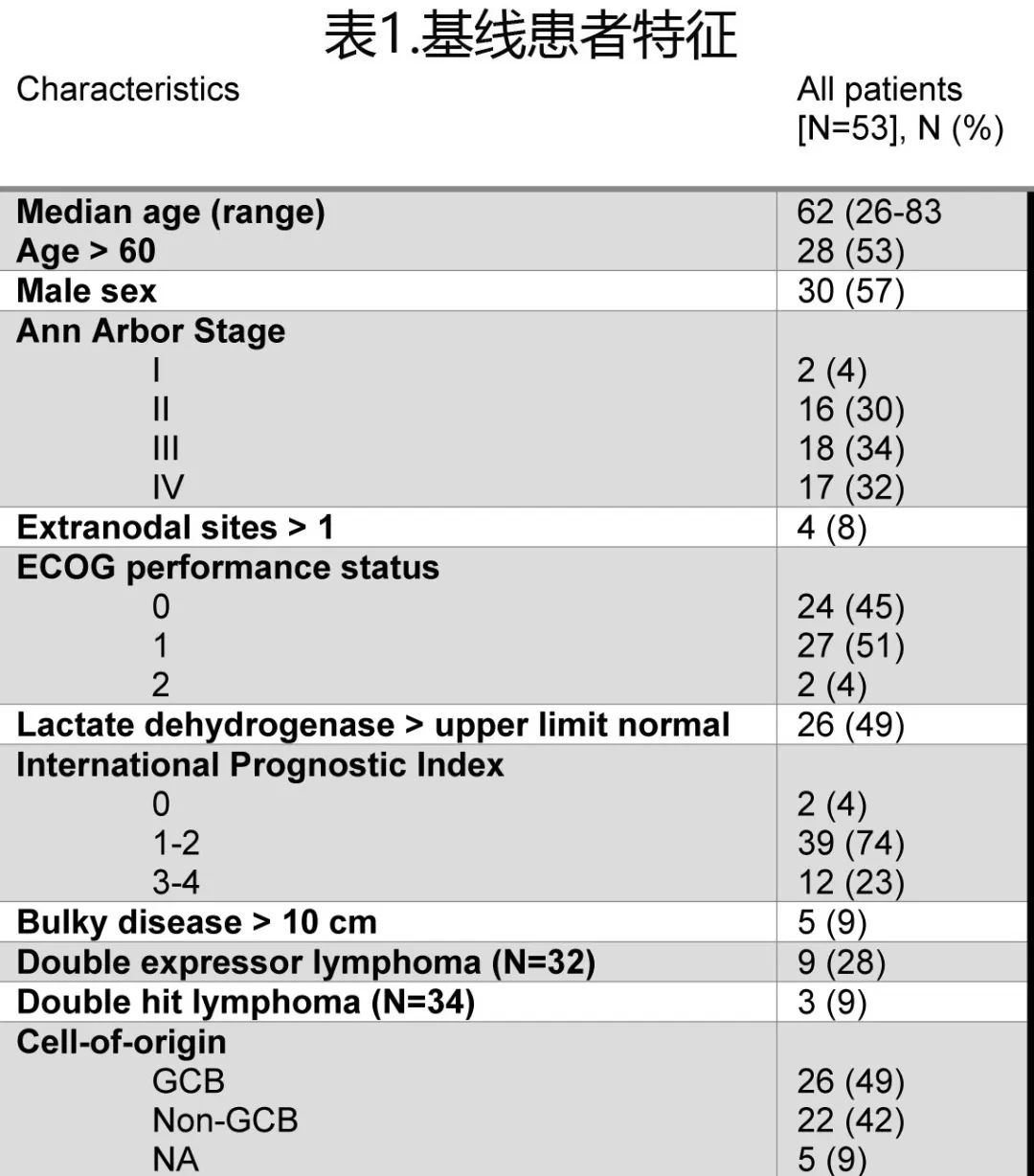
共入组53例患者,其中Ib期部分6例、II期部分47例。中位年龄为62岁,35例 (66%) 患者为 III/IV 期,26例 (49%) 乳酸脱氢酶 (LDH) 升高,12例 (23%) 国际预后指数 (IPI) > 2,26例 (49%) 为生发中心 (GC),22例 (42%) 为非 GC 亚型,5例无法进行亚型分型。详细的基线特征总结见表1。
安全性
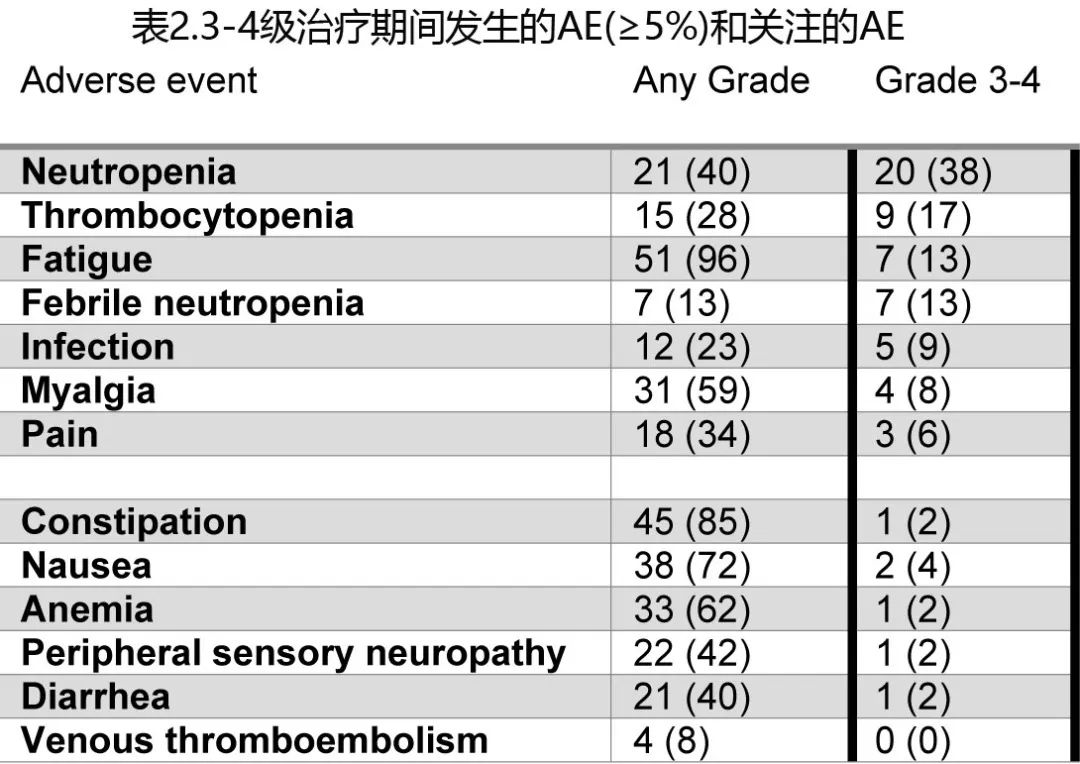
所有患者均发生治疗相关不良事件,其中37例(70%)发生了≥1次3-4级治疗相关不良事件,无致死性AE。Ib期的6例患者未发生剂量限制性毒性。常见的任何级别 AE 包括疲乏 (96%)、便秘 (85%)、恶心 (72%)、贫血 (62%)、肌痛 (59%) 和头晕 (57%)。常见的3-4级 AE 包括中性粒细胞减少 (38%)、血小板减少 (17%)、疲乏 (13%)、发热性中性粒细胞减少 (13%) 和感染 (9%)。3-4级感染包括蜂窝织炎、尿路感染、感染性肺炎和艰难梭菌性结肠炎。4例 (8%) 患者发生血栓栓塞。AE见表2。
23例 (43%) 患者因 AE 中断来那度胺(L)治疗(主要因周期中期中性粒细胞减少或血小板减少),11例 (21%) 需要降低剂量,3例 (6%) 停药。1例患者需要延迟下一周期的 LO-CHOP 治疗7天以上。
疗效
51例患者在2个 LO-CHOP 周期后接受中期 PET/CT 评估(2例患者退出研究而无法评估,其中1例因 AE、 1例因患者选择)。中期评估的 ORR 为100% (51/51),CRR为84% (43/51),而PR为16% (8/51);LO-CHOP 治疗6个周期后,50例患者 PET/CT 可评估(另有1例患者因 AE 退出研究),治疗结束时的 ORR 为98% (49/50),CR、PR和PD分别为90% (45/50)、8% (n=4) 和2% (n=1) 。
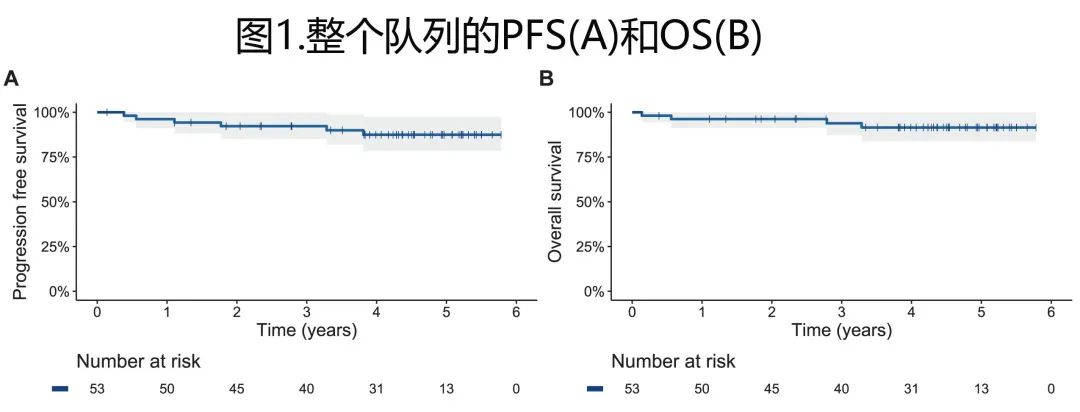
中位随访4.5年,6例患者出现疾病进展或复发,4例患者死亡(原因:淋巴瘤进展、转化型MDS、脑血管意外和未知),中位 PFS 和OS未达到,4年 PFS 和 OS 率分别为87.4%和91.3%(图1A-B)。
循环肿瘤DNA
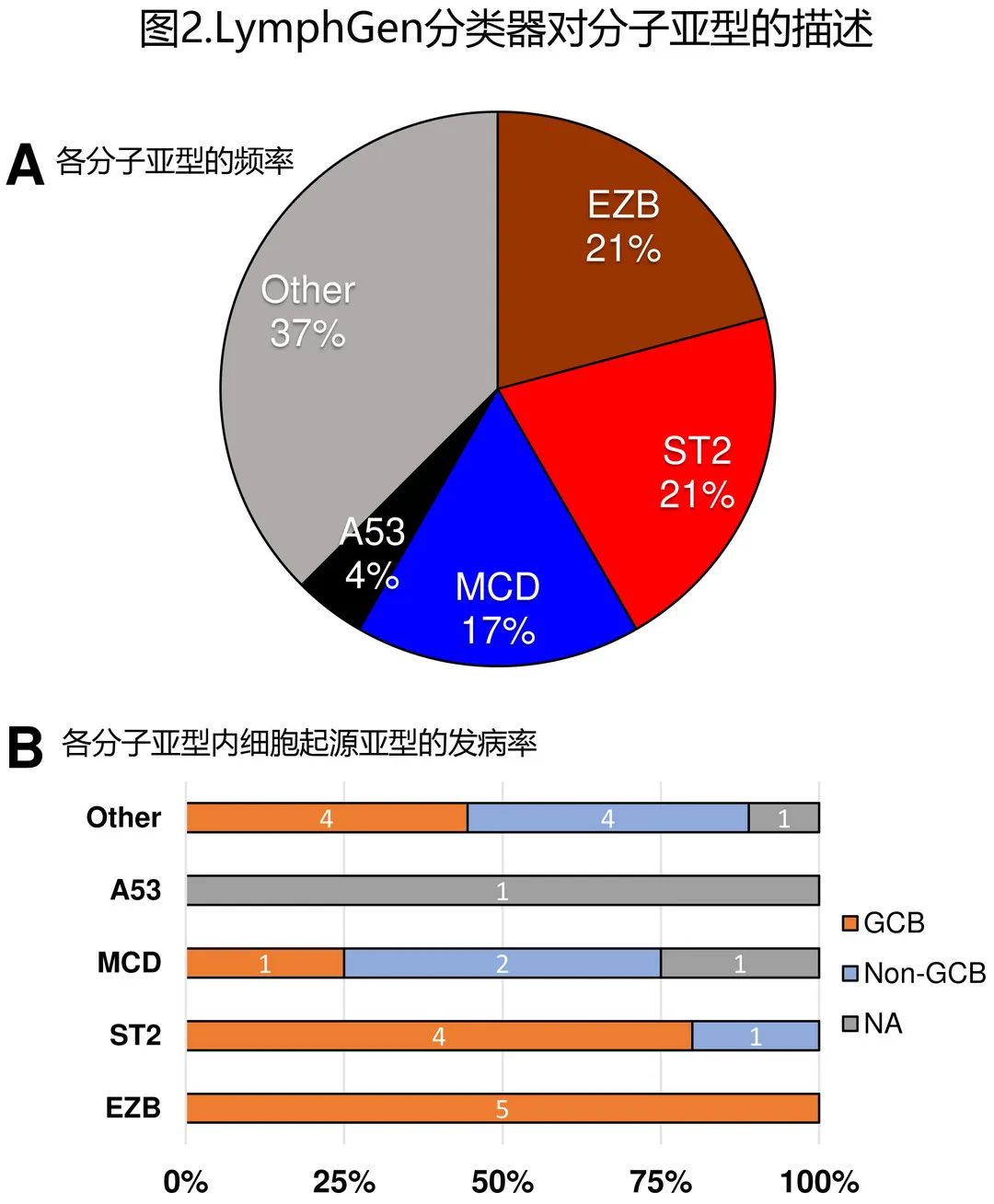
成功评估了总计24/33例 (73%) 患者的ctDNA,分子亚型包括其他 (9,38%)、EZB(5,21%)、ST2(5,21%)、MCD(4,17%) 和A53(1,4%)(图2A);2例患者具有复合亚型(EZB/ST2和EZB/A53),在此被归类为EZB。正如预期,所有5例 EZB 和4/5例 ST2 患者均归类为 GC 亚型,而仅2/4例 MCD 患者为非GC,人工审查其余2例 MCD 患者的基因型,根据存在典型热点突变(提示这些病例可能 IHC 错误分类为COO),认为将其分类为 MCD 是适当的。每个基因亚型内 COO 亚组的发病率如图 2B 所示。
上述24例合格患者中分别有20例和17例可评估EMR(早期分子学缓解,定义为1个治疗周期后 ctDNA 下降 2个对数)和 MMR (主要分子学缓解,定义为治疗2个周期后 ctDNA 下降2.5个对数)的样本。EMR 和 MMR 率分别为75% (15/20) 和71% (12/17)(图3A-B)。
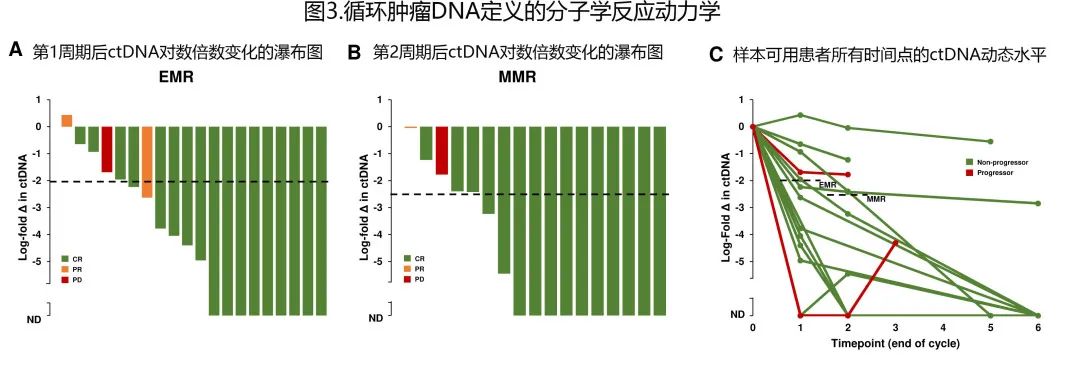
在 EMR 和 MMR 均可评估的15例患者中,2个终点之间的一致性为87% (13/15)。所有时间点 ctDNA 水平的倍数变化如图 3C 所示。共18例患者在至少5个治疗周期后可进行 ctDNA 评估,其中16例 (89%) ctDNA无法检测,而2例患者在该晚期时间点检测到ctDNA。
未发现ctDNA 特征(包括分子学亚型、EMR、MMR或 PhasED-Seq 的晚期时间点MRD),与患者的缓解率、PFS或 OS 的显著差异有相关性。
结论
在这项 Ib/II 期研究中,来那度胺和奥妥珠单抗联合 CHOP 化疗(LO-CHOP)治疗新诊断 DLBCL 高度有效,治疗结束时的ORR和 CR 分别为98%和90%,4年 PFS 和 OS 率分别为87%和91%。LO-CHOP 在高危患者亚群中同样有效,包括 高IPI、非GCB COO、治疗前高 ctDNA 水平以及 MCD 和 EZB 分子亚型。LO-CHOP 治疗1个或2个周期后的早期和主要分子学缓解率分别为75%和71%,且两个终点之间具有高度一致性。此外令人鼓舞的是,治疗结束时PhasED-Seq评估的MRD阴性率高达89%;本研究也证明了ctDNA 测序可以在前瞻性临床试验中,对接受基因亚型分型治疗的患者进行非侵入性分子学分类。
LO-CHOP 的安全性特征未显示任何非预期毒性;且在强制性生长因子支持下,3-4级AE(如中性粒细胞减少、血小板减少和发热性中性粒细胞减少)的发生率优于 LR-CHOP 和 O-CHOP 的报道。此外任何级别血栓栓塞的发生率可能高于 ROBUST 研究,但患者数量较少很难得出结论。任何级别AE(如疲乏、恶心和便秘)的发生率均高于预期,但无剂量限制性毒性,治疗中止或延迟的发生率较低,与其他研究相比血细胞减少的发生率相似,表明这种差异可能与报告差异有关,而非毒性高于R-CHOP 或 LR-CHOP。
总的来说,作为该单臂 Ib/II 期研究中 DLBCL 的改良一线治疗方案,LO-CHOP具有较高的放射影像学和分子学缓解率、长期随访的持久缓解和预期的安全性特征,但本研究无法和R-CHOP直接对比。此外本研究纳入的研究设计方法,包括新型组合和基于 ctDNA 的评估,也可能对进一步改善 DLBCL 的一线治疗至关重要。
参考文献
Chern HJ,et al.A phase I/II study of lenalidomide and obinutuzumab with CHOP for newly diagnosed diffuse large B-cell lymphoma.Blood Adv . 2022 Nov 14;bloodadvances.2022008174. doi: 10.1182/bloodadvances.2022008174
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


