J Immunother Cancer:CheckMate 920研究评估nivolumab(那武利尤单抗)+ ipilimumab (伊匹木单抗)治疗晚期非透明细胞肾癌患者的疗效和安全性
时间:2022-02-28 14:20:43 热度:37.1℃ 作者:网络
CheckMate 920 (NCT02982954)是一项多队列、3b/4期临床试验,主要是评估nivolumab + ipilimumab治疗未治晚期肾细胞癌(RCC)患者的疗效和安全性。近期,Journal for ImmunoTherapy of Cancer杂志上报告了CheckMate 920研究中晚期非透明细胞RCC (nccRcc)队列的安全性和有效性。

研究纳入既往未治疗的晚期/转移性nccRCC患者,KPS≧70%,接受4周期nivolumab 3mg /kg加ipilimumab 1mg /kg,每3周一次,随后是nivolumab 480mg维持,每4周一次,≦2年或直到疾病进展/不可接受的毒性。主要终点是最后一次给药100天内≧3级免疫介导不良事件(AEs)的发生率。主要次要终点包括客观缓解率(ORR)、无进展生存期(PFS;研究者评估),反应时间(TTR)和反应持续时间(DOR)。总生存期(OS)为探索性。
研究纳入52例ncRcc患者接受治疗,中位年龄为64岁(范围23-86),69.2%为男性,KPS均≧70%,82.7%为IMDC中低风险,28.8%有肉瘤样特征。
最常见的任何级别免疫介导的AEs为皮疹(23.1%)、腹泻/结肠炎(13.5%)和甲状腺功能减退/甲状腺炎(9.6%;表2)。未报道5级免疫介导的AEs。3 - 4级免疫介导的AEs分别为腹泻/结肠炎(7.7%)、皮疹(5.8%)、肾炎和肾功能不全(3.8%)、肾上腺功能不全、肝炎和垂体炎(各1.9%)。

92.3%的患者报告了任何级别治疗相关的AEs,最常见的是疲劳(48.1%)、腹泻(30.8%)和恶心(26.9%)。

研究者评估的ORR (n=46)为19.6% (95% CI 9.4-33.9)。其中2例患者获得完全缓解(乳头状,n=1;未分类,n=1), 7例达到部分缓解(乳头状,n=4;未分类,n=3), 17例病情稳定。PD- L1 <1%和 ≥1%患者的ORR分别为14.3% (95% CI 3.0%-36.3%)和30.8% (95% CI 9.1%-61.4%)。存在或不存在肉瘤样特征患者的ORR分别为35.7% (95% CI 12.8%-64.9%)和12.5%(95%CI 3.5%-29.0%)。IMDC低风险,中风险,和高风险患者的ORR分别为12.5% (95% CI 0.3%-52.7%),20.0% (95% CI 6.8%-40.7%),和23.1%(95%CI 5.0%-53.8%)。

中位TTR为2.8个月(范围2.1 - 14.8个月)。中位DOR未达到(范围0.0+-27.8+);9例出现应答者中仍有8例患者未报告病情进展。
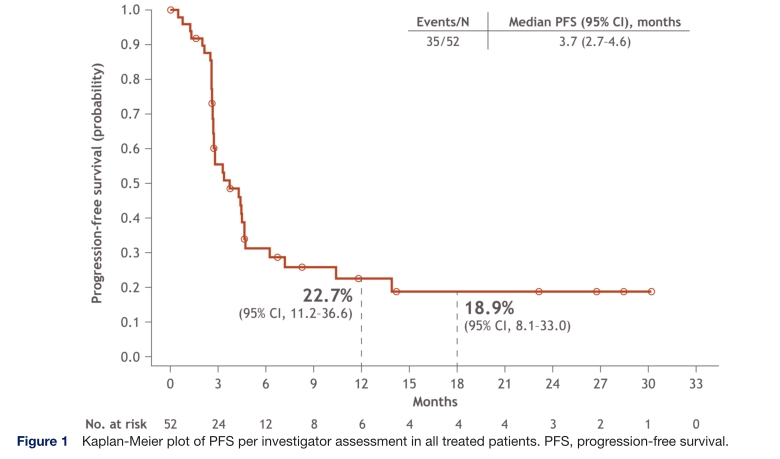
中位无进展生存期(n=52)为3.7个月(95% CI 2.7-4.6)。IMDC低风险,中风险,和高风险患者中位PFS分别为3.6 (95% CI 2.6 to NE; n=9) 个月, 4.3 (95% CI 2.6 to 10.4; n=27)个月, 和2.8 (95% CI 1.3 to 4.7; n=16)个月。
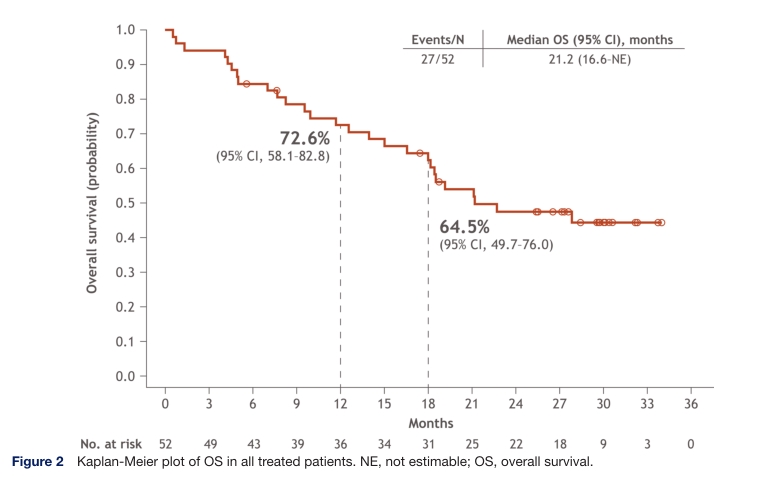
中位OS (n=52)为21.2个月(95% CI 16.6至不可估计)。12个月和18个月的生存率分别为72.6% (95% CI 58.1%-82.8%)和64.5% (95% CI 49.7%-76.0%)。IMDC低风险,中风险,和高风险患者中位OS分别为未达到(95% CI 4.1至NE;n=9), 22.7 (95% CI 16.6 ~ NE;n=27)个月,和16.6个月(95% CI 4.5 ~ 27.9;n = 16)个月。
综上,研究表明,nivolumab(那武利尤单抗)+ ipilimumab (伊匹木单抗)治疗晚期非透明细胞肾癌患者具有令人鼓舞的抗肿瘤活性,并且未出现新的安全信号。
原始出处:
Tykodi SS, Gordan LN, Alter RS, Arrowsmith E, Harrison MR, Percent I, Singal R, Van Veldhuizen P, George DJ, Hutson T, Zhang J, Zoco J, Johansen JL, Rezazadeh Kalebasty A. Safety and efficacy of nivolumab plus ipilimumab in patients with advanced non-clear cell renal cell carcinoma: results from the phase 3b/4 CheckMate 920 trial. J Immunother Cancer. 2022 Feb;10(2):e003844. doi: 10.1136/jitc-2021-003844. PMID: 35210307.


