Nature Neuroscience:新型AAV变体,突破血脑屏障,且不在肝脏富集
时间:2021-12-16 14:01:35 热度:37.1℃ 作者:网络
血脑屏障(BBB)是指脑毛细血管壁与神经胶质细胞形成的血浆与脑细胞之间的屏障,和由脉络丛形成的血浆和脑脊液之间的屏障,仅允许特定类型的分子从血流进入大脑神经元和其他周围细胞。
血脑屏障的存在,对于阻止有害物质由血液进入大脑具有重要意义,然而,血脑屏障同时也阻止了绝大部分小分子和大分子(例如多肽,蛋白质和核酸)的转移,严重限制了神经中枢系统疾病(例如神经退行性疾病、脑肿瘤,脑部感染和中风等)的治疗。
随着日益严重的人口老龄化问题,阿尔茨海默病、亨廷顿症、帕金森病等神经退行性疾病正在快速增长,脑部疾病的治疗面临严峻挑战,因此,迫切需要有效突破血脑屏障的药物递送策略。
近日,美国加州理工学院 Viviana Gradinaru 团队在 Nature Neuroscience 期刊发表了题为:AAV capsid variants with brain-wide transgene expression and decreased liver targeting after intravenous delivery in mouse and marmoset 的研究论文。
该研究开发了一种新型腺相关病毒(AAV)变体——AAV.CAP-B10,该载体能够通过血液注射突破血脑屏障,靶向神经细胞,同时不会在肝脏富集,避免了可能引起的肝脏毒性副作用,为脑部疾病提供了一种更安全、更有效的治疗选择。该AAV变体在小鼠和狨猴模型中均得到了验证,这为向临床转化铺平了道路。

腺相关病毒(AAV)长期以来被认为是最有前景的基因治疗递送载体,而且已经在临床中得到了验证。
AAV由两个主要部分组成:蛋白质构成的衣壳;以及包裹在衣壳内的遗传物质。将其中的遗传物质替换成治疗所需的DNA片段,构成重组AAV,然后将其靶向特定组织,就能实现基因治疗的目的。早在2017年,FDA就批准了Spark Therapeutics的AAV基因疗法上市,该疗法就是通过AAV将RPE65基因递送到视网膜,治疗先天性黑蒙症。
加州理工学院的 Viviana Gradinaru 团队近十年来一直致力于开发和设计能够穿越血脑屏障的AAV衣壳,并使其可以特异性靶向大脑内的特定细胞类型。此前,该团队就开发出了AAV-PHP.eB,它能够通过静脉注射高效穿越血脑屏障,但同时也会在肝脏富集。
在这项新研究中,该团队通过对AAV9型进行衣壳改造,开发了一系列AAV变体,其中AAV.CAP-B10,不仅能够高效穿越血脑屏障进入大脑细胞,特别是神经元,同时还能包括肝脏在内的全身性目标。这种穿越血脑屏障的神经元特异性靶向和肝脏低靶向,不仅在小鼠上得到了证实,在非人灵长类动物狨猴上也得到了证实。
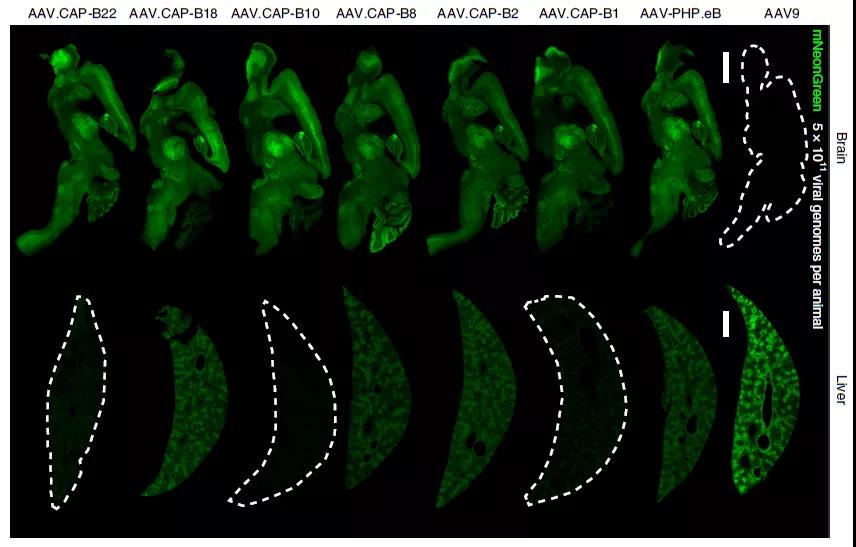
在此之前,该团队开发的AAV-PHP.eB等载体在非人灵长类动物实验中未获成功,而这项新研究找那个开发的AAV.CAP-B10,在非人灵长类动物中同样效果显着,相比AAV9和AAV-PHP.eB,AAV.CAP-B10能够特异性靶向神经元,而且不会在肝脏富集。
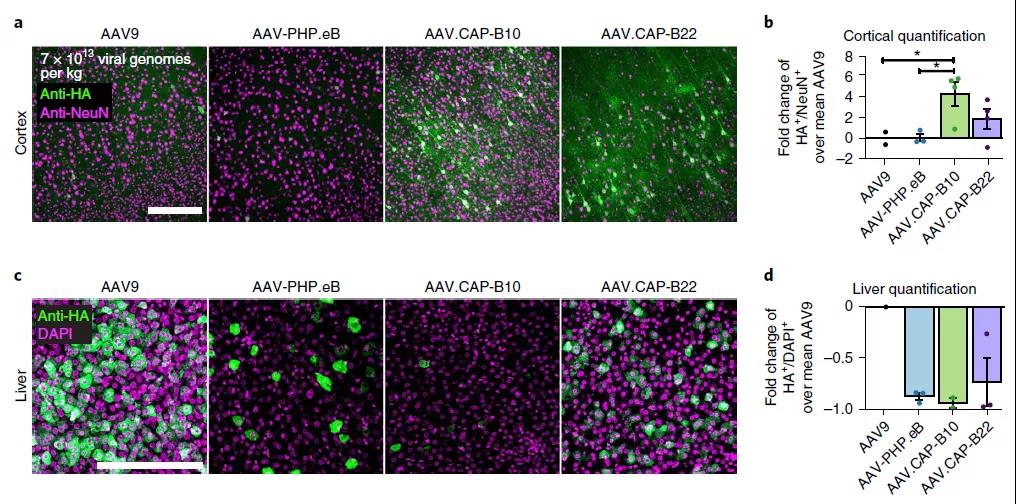
Viviana Gradinaru 团队通过定向进化,在多个位点修改AAV衣壳,从中产生了多种可以在小鼠和猴子中穿越血脑屏障的AAV变体。这些研究结果也说明了针对AAV衣壳的修改能够提高基因治疗的递送效率、增加神经元靶向特异性。这一新的AAV载体也为脑部疾病提供了一种更安全、更有效的治疗选择。

Viviana Gradinaru
Viviana Gradinaru 是张锋的师妹,二人均博士毕业于光遗传学之父 Karl Deisseroth 教授的实验室,博士期间,Viviana 与张锋一起发表了多篇光遗传领域重要论文。
原始出处:
Goertsen, D., Flytzanis, N.C., Goeden, N. et al. AAV capsid variants with brain-wide transgene expression and decreased liver targeting after intravenous delivery in mouse and marmoset. Nat Neurosci (2021). https://doi.org/10.1038/s41593-021-00969-4.


