Nat Nanotech:我国学者开发出高效装载砒霜的仿生递送载体,显著抑制多种白血病
时间:2021-10-28 12:03:01 热度:37.1℃ 作者:网络
白血病是严重危害人类健康的血液系统恶性肿瘤,在儿童及35岁以下成人中死亡率居恶性肿瘤首位。目前,化疗仍然为白血病治疗的重要手段,主要临床用药包括烷化剂、抗代谢类药物、生物碱类药物以及由中国学者提出的砒霜治癌(三氧化二砷,ATO)。针对各种类型白血病,临床已建立了不同的标准化疗方案,但总体治疗效果仍有待提升。
基于体内天然颗粒创建药物载体,可以借助体内固有路径靶向递送药物,克服体内复杂环境和多重屏障,提高已批准药物的疗效并扩展适应症,并且具有较高的成药性。
2021年10月25日,中科院过程工程所生化工程国家重点实验室马光辉研究员、魏炜研究员、北京大学化学与分子工程学院马丁教授、南方医科大学珠江医院李玉华教授团队合作,在 Nature 子刊 Nature Nanotechnology 上 发表了题为:Ferritin-based targeted delivery of arsenic to diverse leukaemia types confers strong anti-leukaemia therapeutic effects 的研究论文。
该研究发现多种白血病细胞具有特异性高表达CD71的广谱特点,提出利用CD71配体铁蛋白颗粒(Fn)作为药物载体,解决了Fn高效装载白血病治疗药物三氧化二砷(ATO)的难题并实现了靶向递送,显着抑制了多种白血病的进展。

中科院过程工程所生化工程国家重点实验室基于体内天然组分的铁蛋白颗粒(Fn)和已批准的药物三氧化二砷(ATO),提出了仿生递送的新策略,并联合北京大学和珠江医院交叉合作,面向临床应用的实际需求,进行了白血病靶向治疗创新制剂的研发。
研究团队首先收集大量临床外周血和骨髓样本,发现健康样本中的红细胞、淋巴细胞、单核细胞和粒细胞的CD71表达水平较低(平均阳性率<10%),而患者样本中白血病细胞的CD71表达水平显着升高(平均阳性率>90%)。CD71的特异性高表达不受限于白血病的类型和进程,证明了其作为白血病细胞广谱靶点的可行性。
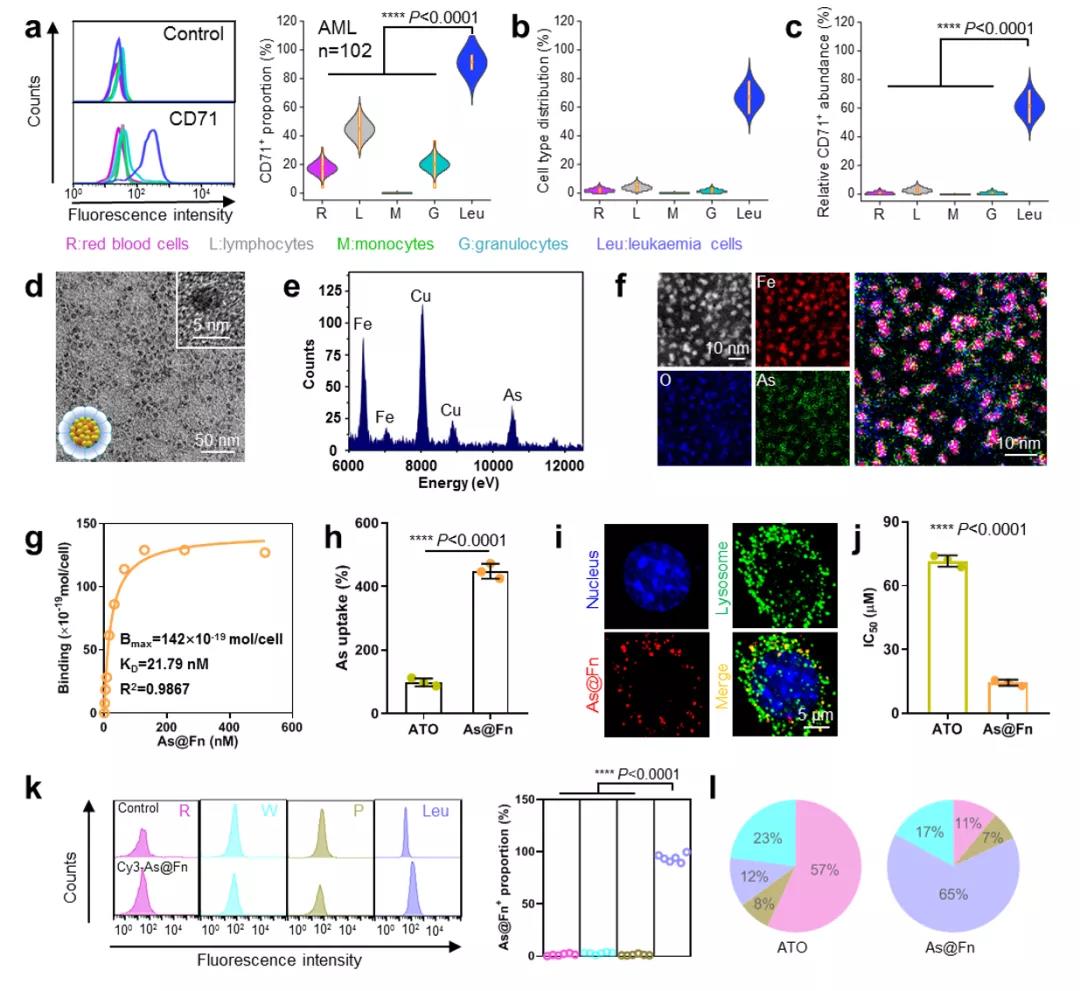
图1:白血病细胞CD71表达、As@Fn的构建和靶向性分析:(a)白血病患者骨髓中各细胞群CD71表达阳性率;(b)各细胞群比例;(c)各细胞群C71表达丰度;(d)As@Fn透射电镜图;(e)As@Fn能谱图;(f)As@Fn球差电镜图;(g)As@Fn和白血病细胞特异性结合曲线;(h)As@Fn和ATO的白血病细胞内吞比较;(i)As@Fn的胞内定位;(j)As@Fn和ATO对于白血病细胞的IC50比较;(k)As@Fn体内靶向白血病细胞分析;(l)As@Fn和ATO的体内分布比较
在此基础上,研究团队提出利用CD71配体Fn作为载体靶向递送ATO,以此提高治疗效果并降低副作用。然而,Fn的内腔十分有限(直径~8 nm),对小分子ATO的高效装载和可控释放提出了挑战。
研究团队基于Fn的耐热性能、铁对Fn内腔的亲和性以及砷与铁的相互作用,巧妙地设计铁预成核的策略并高效锚定了三价砷(Fn:As=1:200)。静脉注射后,砷基铁蛋白(As@Fn)可以借助CD71的识别,靶向富集于白血病细胞,并在胞内酸性溶酶体中选择性释放活性三价砷,高效杀伤白血病细胞。
上述仿生靶向递送策略显着提高了临床砷制剂的耐受剂量,并且将适应症从急性早幼粒细胞性白血病扩展至急性髓系、急性淋系和慢性髓系等多种白血病类型。研究团队在临床样本和患者来源的异种移植模型上证明,As@Fn可显着抑制多种白血病的进展,效果显着优于现有的单独ATO和联合化疗策略。
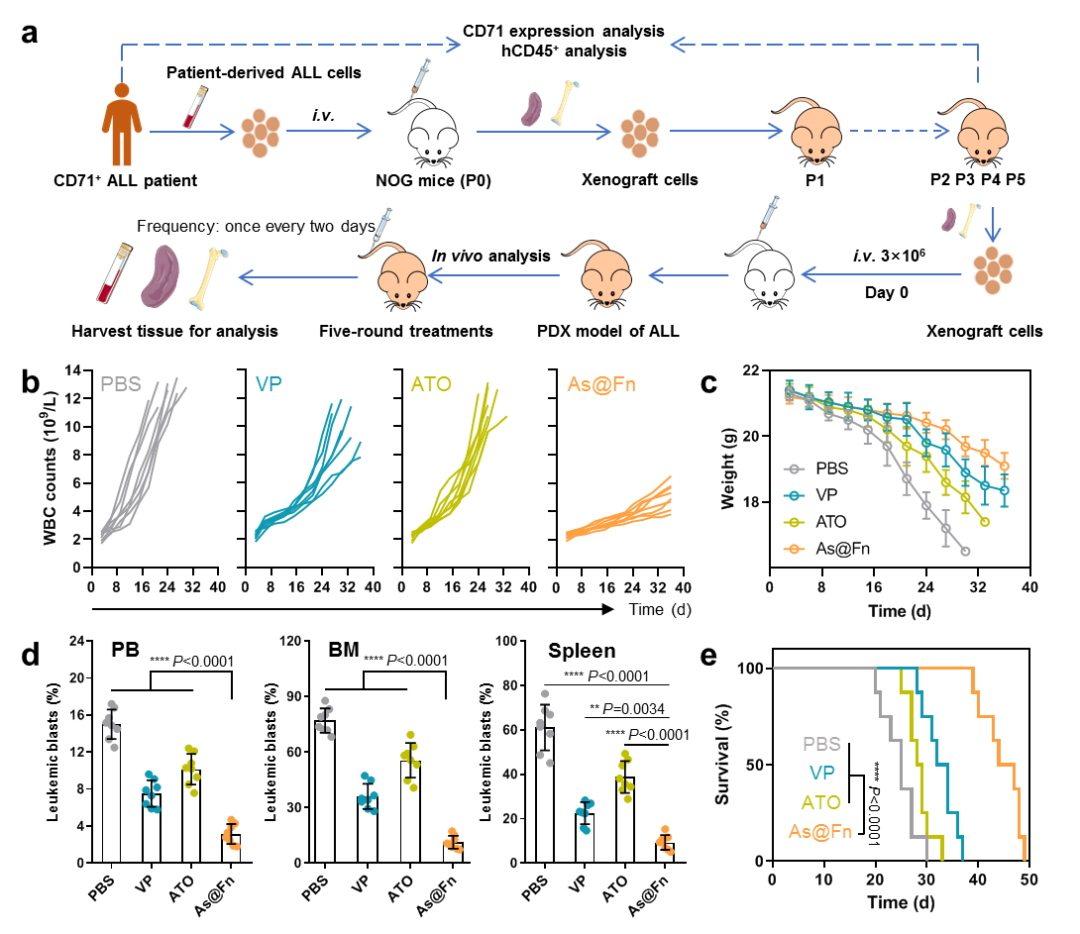
图2:As@Fn在病人来源白血病异种移植模型上的疗效:(a)白血病PDX模型构建及药效分析示意图;(b)不同治疗组小鼠白细胞变化曲线;(c)不同治疗组小鼠体重变化曲线;(d)不同治疗组小鼠外周血(PB)、骨髓(BM)和脾脏中白血病细胞的比例;(e)不同治疗组小鼠的生存曲线
研究团队表示,上述成果仍属于临床前研究,实际临床疗效仍有待进一步验证。鉴于Fn为人体内源组分并且ATO为已批准用药,该制剂具有较好临床转化潜力。研究团队正在按照相关要求合作推进后续的研发和转化。
该研究是研究团队基于以往的研究基础,历经十一年的潜心研究和交叉合作,根据白血病新靶点发展的又一个具备转化潜力的靶向递送剂型。王昌龙博士研究生(中科院过程工程所)、章伟博士(北京大学)、贺艳杰副主任医师(珠江医院)为该论文的共同第一作者。马光辉研究员(过程工程所)、马丁教授(北京大学)、魏炜研究员(过程工程所)、李玉华教授(珠江医院)为共同通讯作者。相关工作得到了国家自然科学基金、国家重点研发计划项目、中科院战略性先导科技专项、广州再生医学与健康广东省实验室项目等支持。
原始出处:
Wang, C., Zhang, W., He, Y. et al. Ferritin-based targeted delivery of arsenic to diverse leukaemia types confers strong anti-leukaemia therapeutic effects. Nat. Nanotechnol. (2021). https://doi.org/10.1038/s41565-021-00980-7.


