LANCET ONCOL:围手术期或术后辅助奥沙利铂联合S-1 vs术后辅助奥沙利铂联合卡培他滨在接受D2胃切除术的局部进展期胃或胃食管结合部腺癌患者的疗效和安全性(RESOLVE): 一项开放标签、优效性和非劣效的3期随机对照研究
时间:2021-07-11 21:01:51 热度:37.1℃ 作者:网络
局部进展期胃癌(LAGC)标准治疗方案为D2胃切除术结合围术期治疗。目前指南推荐术后治疗采用卡培他滨联合奥沙利铂方案(CapOx)。但是,围手术期最佳治疗方案是手术后辅助化疗,还是新辅助化疗后手术加辅助化疗,目前尚存争议。而且,新辅助化疗对于有明显局部肿瘤浸润或淋巴结转移患者的效益不明确。氟尿嘧啶为基础的化疗方案是胃癌治疗的基础,包括S-1和卡培他滨。基于S-1的方案在胃癌治疗中均表现出较好的耐受性以及疗效, 而CapOx辅助化疗则出现较高的不良事件。目前尚无大规模随机试验比较围手术期SOX和标准术后CapOx方案的优劣性,SOX辅助化疗的疗效和安全性同样需要前瞻性试验进一步研究。因此,我国研究者针对接受D2根治术的LAGC患者开展了RESOLVE研究, 评估围手术期或术后辅助SOX 对比术后辅助CapOx在接受D2胃切除术的局部进展期胃或胃食管结合部腺癌患者的疗效和安全性。相关研究成果发表在LANCET ONCOL杂志上。

RESOLVE是在中国27个医院中心开展一项随机对照、开放标签、多中心、优效性/非劣效III期试验。纳入年龄≥18岁,经组织学证实的胃腺癌患者(cT4aN+M0或cT4bNanyM0),KPS≥70。所有患者均接受标准D2淋巴结切除术。入组患者1:1:1随机分配至三组:Adj-CapOx组:D2根治术后CapOx辅助化疗共8周期,Adj-SOX组:D2根治术后SOX辅助化疗共8周期、Peri-SOX组:D2根治术前使用SOX3周期,术后辅助SOX5周期。主要研究终点是3年无病生存期(DFS),次要研究终点是总生存期(OS)、客观缓解率(ORR)、病理完全缓解(pCR)和安全性。
共1022例 (mITT人群)接受了研究治疗。Adj-CapOx组、Adj-SOX组、Peri-SOX组分别有342例、338例、295例患者接受了手术。中位随访时间为40.6个月。Peri-SOX组和Adj-CapOx组的R0切除率分别为93%和87%(P <0.01); Peri-SOX和Adj-CapOx组的D2淋巴清扫率分别为96%和91%(P <0.01);Peri-SOX组病理性T分期和N分期患者比例明显低于其余两组(P <0.01)。
mITT人群的主要终点结果显示,Adj-CapOx组和Peri-SOX组的3年DFS率分别为51.1%和59.4%(HR=0.77,95%CI=0.61-0.97, P=0.027),而Adj-CapOx组(51.1%)与Adj-SOX组(56.5%)的3年DFS率相当(HR=0.86,95%CI=0.68-1.07, P=0.170),满足非劣效性条件。Peri-SOX组在六个亚组中的四个亚组中的DFS明显优于Adj-CapOx组:女性患者(P=0.006)、胃部肿瘤(P=0.047)、非肠型(P=0.016)和N+(P=0.032)。而Adj-CapOx组与Adj-SOX组相比,在六个亚组分析中均无显著差异。
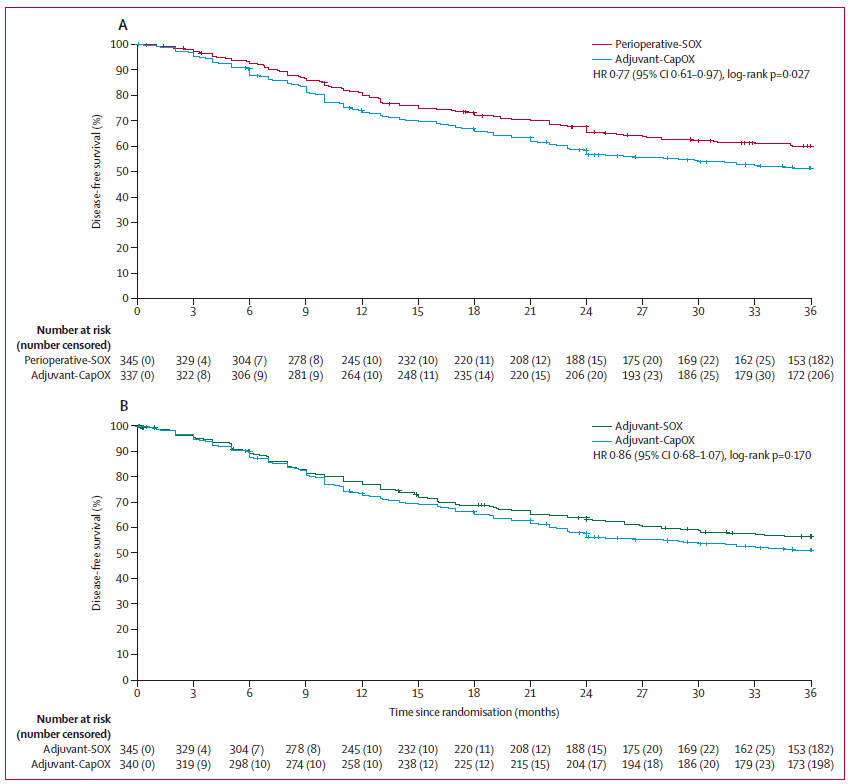
DFS
安全性方面,Adj-CapOx组、Adj-SOX组和Peri-SOX组30天围术期死亡率均为1%,三组手术相关并发症发生率相似。Adj-CapOx组、Adj-SOX组和Peri-SOX组3-4级不良反应发生率分别为17%、19%、21%,Peri-SOX组的3-4级血小板减少(P=0.013)和贫血(P=0.0048)发生率显著高于Adj-CapOx组。严重不良事件包括Adj-CapOx组的低白蛋白血症(n=1)和中性粒细胞减少症(n=1),以及Peri-SOX组的恶心(n=1)、血小板减少症(n=2)和中性粒细胞减少症(n=2)。
综上,与CapOx辅助化疗相比,围术期使用SOX方案能显著改善LAGC胃切除患者的3年DFS,而SOX辅助化疗非劣于CapOx辅助化疗。
原始出处:
Xiaotian Zhang,Han Liang, Ziyu Li, et al. Perioperative or postoperative adjuvant oxaliplatin with S-1 versus adjuvant oxaliplatin with capecitabine in patients with locally advanced gastric or gastro-oesophageal junction adenocarcinoma undergoing D2 gastrectomy (RESOLVE): an open-label, superiority and non-inferiority, phase 3 randomised controlled trial. Published:July 09, 2021DOI:https://doi.org/10.1016/S1470-2045(21)00297-7.


