Sci Trans Med:Tau抗体semorinemab I期临床安全
时间:2021-05-17 22:01:37 热度:37.1℃ 作者:网络
阿尔茨海默病(AD)是痴呆症最常见的原因,估计在美国有580万患者,全世界有5000万患者。现在,已获批准的AD医疗疗法(如乙酰胆碱酯酶抑制剂和N-甲基-D-天门冬氨酸受体拮抗剂)可能暂时缓解AD的症状,但它们不能改变疾病的进展。鉴于这一庞大且不断增长的未得到满足的医疗和社会挑战,人们迫切需要减缓或阻止这一疾病的认知和功能衰退的治疗方法。
AD的特点是细胞外含β-淀粉样肽(Aβ)的斑块(淀粉样斑块)和细胞内tau聚集物[神经纤维缠结(NFTs)]在大脑中的积累。治疗性药物的开发主要集中在阻断Aβ肽的形成,去除Aβ的聚集形式,或减轻其神经毒性,目前为止,针对Aβ肽的疗法结果喜忧参半。

最近的药物开发工作以Tau为目标,Tau是一种微管结合蛋白,会过度磷酸化,并聚集形成NFTs的主要成分。Tau是一个有吸引力的药物目标,因为tau病理的解剖分布和程度与疾病过程和严重程度密切相关,特别是与认知缺陷的范围和皮质萎缩的程度相关。此外,在AD转基因(Tg)小鼠模型中,敲除编码tau的基因(MAPT)可以防止认知障碍,表明tau可能在疾病的进展中发挥核心作用。
最近,研究人员描述了semorinemab抗体的产生、临床前特征和1期临床特征。Semorinemab抗体是一种以免疫球蛋白G4(igG4)为骨架的人源化抗tau单克隆抗体。Semorinemab与所有六种人类tau异构体结合,并在神经元和小胶质细胞的培养基中保护神经元免受tau低聚物的神经毒性。
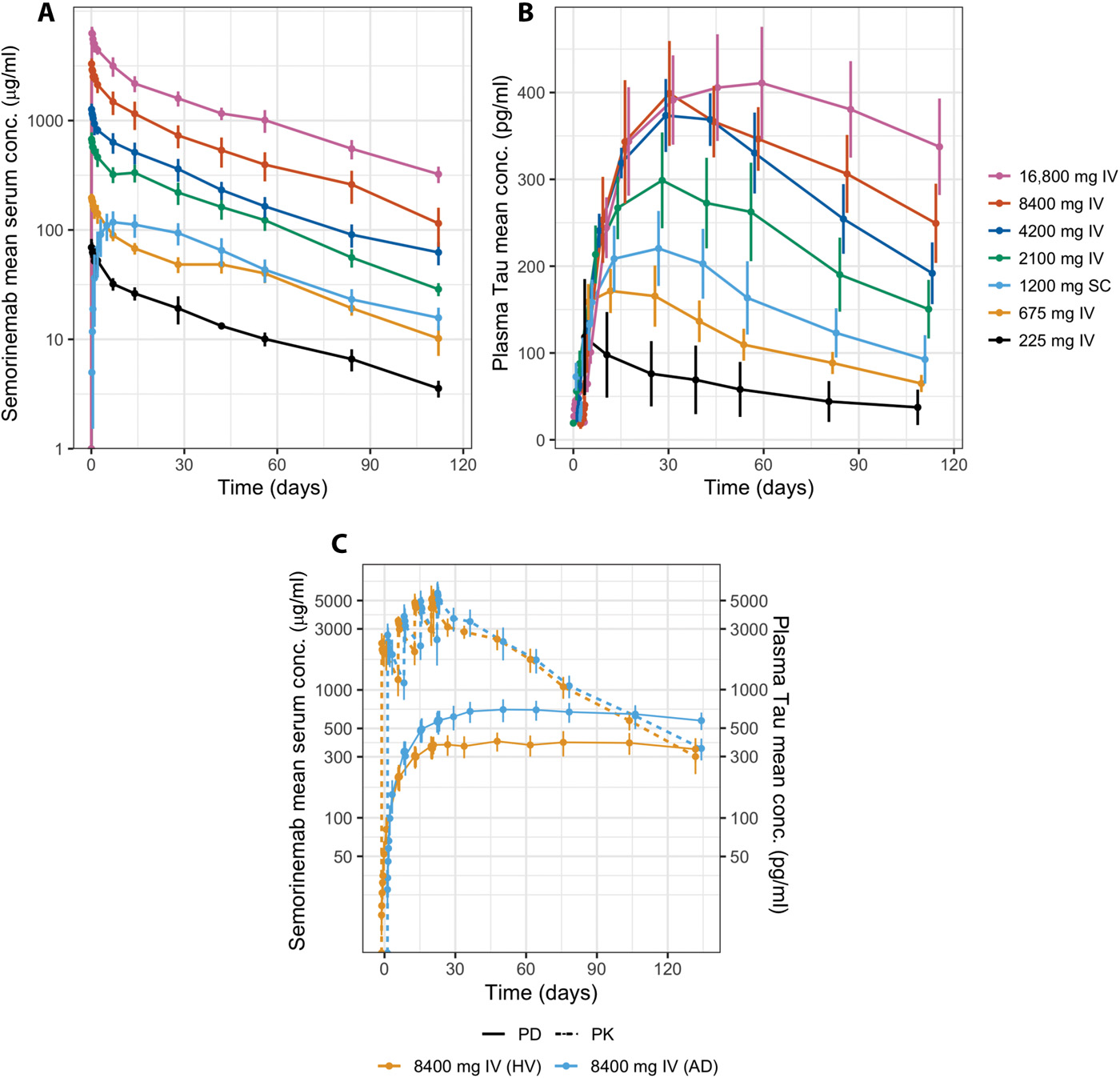
Semorinemab抗体在人体血清和血浆的PK/PD结果
此外,当每周腹腔注射一次,持续13周时,针对小鼠的semorinemab可以减少tau病的转基因小鼠模型中tau病理的积累,与抗体效应功能状态无关。
Semorinemab还显示了体内靶点参与的明确证据,在tau转基因小鼠、非人灵长类动物和人类中观察到全身tau浓度的增加。与健康对照组相比,AD参与者用药后观察到更高的全身tau浓度。
在1期临床试验中,在单次剂量达16,800毫克和一个月内多剂量共33,600毫克时,没有观察到令人担忧的安全问题。
原始出处:
Gai Ayalon et al. Antibody semorinemab reduces tau pathology in a transgenic mouse model and engages tau in patients with Alzheimer’s disease. Science Translational Medicine (2021).


