新英格兰:孕妇mRNA Covid-19疫苗安全性仍是未知
时间:2021-04-23 12:02:10 热度:37.1℃ 作者:网络

美国许多孕妇正在接种mRNA Covid-19疫苗,但有关其对孕妇的安全性的数据有限。在美国获得的第一批Covid-19疫苗是mRNA疫苗:BNT162b2(辉瑞-生物科技)和mRNA-1273 (Moderna)。2020年12月,该疫苗获得了食品和药物管理局(FDA)的紧急使用授权(EUA),作为两剂系列疫苗,辉瑞- biontech间隔3周,Moderna间隔1个月,并被免疫实践咨询委员会(ACIP)推荐使用。1-4名孕妇被排除在预先授权的临床试验之外,在授权时只有有限的关于妊娠期安全性的人类数据。然而,与未怀孕的育龄者相比,患有Covid-19的孕妇罹患严重疾病(如入院重症监护室、体外膜氧合或机械通气)和死亡的风险更高。此外,与未感染Covid-19的孕妇相比,感染Covid-19的孕妇可能面临更大的不良妊娠结局风险,如早产。
与美国妇产科医师学会和美国儿科学会合作,发布了指导意见,指出不应向孕妇拒绝接种Covid-19疫苗,需要对孕妇进行授权后监测,以确定这些新型Covid-19疫苗的安全性,这些疫苗使用mRNA、脂质纳米颗粒和最先进的制造工艺。此外,建立安全档案对于为孕产妇接种Covid-19疫苗提供信息至关重要。CDC v-safe COVID-19 Pregnancy Registry Team报告了美国三种疫苗安全监测系统对孕妇Covid-19疫苗mRNA安全性的初步发现:“v-safe预防接种后健康检查”监测系统,v-safe怀孕登记系统,和疫苗不良事件报告系统(VAERS)。

从2020年12月14日到2021年2月28日,该研究团队使用“ v-safe预防接种后健康检查”监视系统,v-safe怀孕登记册和疫苗不良事件报告系统(VAERS)的数据来表征初始Covid-19 mRNA孕妇疫苗的安全性。
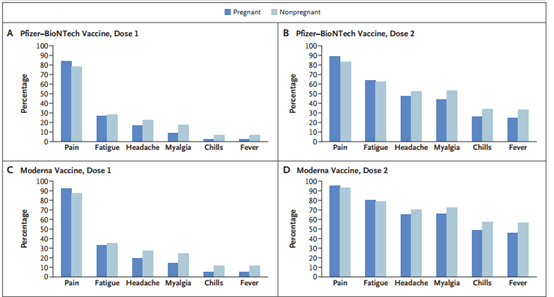
共有35691名16至54岁的v型安全参与者被确认为怀孕。据报道,与非孕妇相比,孕妇中注射部位疼痛的发生频率更高,而头痛,肌痛,发冷和发烧的报道频率较低。在参加v型安全怀孕登记系统的3958名参与者中,有827名完全怀孕,其中115名(13.9%)导致了流产,而712名(86.1%)的妇女活了分娩(大多数是在第三次接种疫苗的参与者中)三个月)。不良的新生儿结局包括早产(占9.4%)和小胎龄(占3.2%);没有新生儿死亡的报道。虽然不能直接比较,在完成Covid-19预防接种的Covid-19疫苗接种者中,不良妊娠和新生儿结局的计算比例与在Covid-19大流行之前进行的涉及孕妇的研究中报道的发生率相似。向VAERS报告的221个与妊娠相关的不良事件中,最频繁报告的事件是自然流产(46例)。
美国对妊娠期和围产期Covid-19 mRNA疫苗安全性的监测综述表明,美国一些孕妇选择在妊娠期接种Covid-19疫苗。不良妊娠和新生儿结局(如胎儿丢失、早产、胎龄小、先天性畸形、v-safe怀孕登记中已完成妊娠的参与者的数据似乎与Covid-19大流行前研究的怀孕人群中公布的发病率类似。v-safe怀孕登记的许多参与者由于作为卫生保健人员的工作,被纳入1a期(最高)Covid-19疫苗接种优先组。v-safe的参与是自愿的,并不是所有接种地点都统一提供登记信息,尽管EUA对卫生保健提供者和患者的情况介绍中包含了监测系统的信息。因此,由于这些人群在年龄、种族和其他已知与妊娠和新生儿结局相关的社会、人口和临床特征方面可能存在差异,因此,将这些结果的接种妇女比例与以前公布的估计结果进行比较受到限制。然而,这样的比较有助于提供一个粗略的感觉,即这些早期数据中是否有任何意外的安全信号。在分析的时候,在v-safe监测系统中被确认为怀孕的人中,只有14.7%的人被联系到提供怀孕登记。
还应注意其他限制。与所有参与者报告的监测系统一样,v-safe健康调查的错误完成可能导致参与者被错误分类为怀孕;因此,参与者向v-safe平台报告的局部和全身反应数据可能包括一些来自非孕妇的报告。参与者不需要每天在同一时间完成调查,我们评估不良事件(如发烧)发生或持续时间的能力有限。登记数据是初步的,来自一个小样本,并描述了晚期妊娠疫苗接种的新生儿结果;随着额外妊娠结果的报告和样本量的增加,结果可能会改变,这可能有助于发现罕见的结果。无法评估可能与妊娠早期暴露相关的不良后果,如先天性异常,因为迄今为止,在妊娠早期接种疫苗的孕妇中没有活产被纳入v-safe妊娠登记;此外,报告自然流产的孕妇比例可能不能反映疫苗接种后的真实比例,因为参与者可能是在前三个月风险最大的时期之后接种的疫苗,而且很早期的妊娠损失可能无法被确认。虽然在妊娠的前三个月和中期早期接种疫苗的妊娠已经完成,但大多数仍在进行中,需要在接种疫苗时间的基础上对结果进行直接比较,以确定该队列中自然流产的比例。由于样本量的限制,妊娠和新生儿的结果都是按比例而不是按比例计算的。
该研究的初步分析使用了参与者报告的数据,对不良妊娠和新生儿结局的其他潜在危险因素的信息有限。VAERS受到被动监视的限制,尽管EUA强制报告要求和CDC对VAERS报告的指导,但可能存在大量妊娠和新生儿特异性不良事件的漏报。也不知道孕妇接种Covid-19疫苗的总剂量,这进一步限制了我们从VAERS数据估算不良事件报告率的能力。在Covid-19疫苗接种后报告给VAERS的妊娠特异性疾病中,流产是最常见的。这与2009年甲型H1N1流感大流行期间在引入2009年甲型H1N1流感灭活疫苗后观察到的情况类似,在那里,流产是接种该疫苗的孕妇报告的最常见不良事件。除了接种疫苗保护妇女在妊娠期间预防Covid-19及其并发症外,新出现的证据显示,孕产妇接种Covid-19疫苗后,经胎盘转移SARS-CoV-2抗体,这表明孕妇接种疫苗可能对新生儿提供某种程度的保护。然而,这篇文章没有关于抗体转移和与接种时间相关的保护水平的数据。
CDC和FDA正在继续监测和传播有关mRNA和其它类型Covid-19疫苗在孕妇中的安全性的信息。来自v-safe监测系统、v-safe怀孕登记和VAERS的早期数据未显示与妊娠晚期Covid-19疫苗接种相关的妊娠或新生儿结局有任何明显的安全信号。需要继续监测,以进一步评估与孕产妇Covid-19疫苗接种相关的孕产妇、妊娠、新生儿和儿童结局,包括在妊娠早期和孕前阶段。同时,目前的数据可以帮助孕妇及其卫生保健提供者作出有关接种疫苗的决策。
原文出处
Shimabukuro TT, Kim SY, Myers TR, et al. Preliminary Findings of mRNA Covid-19 Vaccine Safety in Pregnant Persons [published online ahead of print, 2021 Apr 21]. N Engl J Med. 2021;10.1056/NEJMoa2104983. doi:10.1056/NEJMoa2104983


