Int J Mol Sci:COVID-19疫情期间及疫情后的粪菌移植
时间:2021-04-10 17:01:23 热度:37.1℃ 作者:网络
COVID-19是当今世界面临的重大流行病,这对当前基于微生物群的治疗有影响,为了提高粪便微生物群移植(FMT)的安全性和有效性,必须阐明人类肠道微生物群与COVID-19发病机制之间的双向关系以及相关的潜在机制。Kazemian N 等在Int J Mol Sci杂志发表了综述文章,讨论了COVID-19感染期间肠道微生物群和肺之间的关键交叉作用,即肠-肺轴,以及这些微生物及其功能活性(即短链脂肪酸和胆胆汁酸)对FMT治疗的可能影响。

此外,该文强调目前迫切需要调查COVID-19对FMT安全性和有效性可能产生的影响,以及COVID-19大流行期间和疫情后制定严格的捐助者、受助者筛选协议的以产生最优化FMT治疗计划。
COVID-19大流行期间和COVID-19大流行后的FMT有四种可能的组合和情况:(1) 无症状COVID-19供体和无症状COVID-19受体;(二)无症状COVID-19供体和COVID-19阴性受体;(三)COVID-19阴性供体和无症状受体;(四) COVID-19阴性供体和COVID-19阴性受体。此外,COVID-19阴性的捐赠者和接受者可能从未感染COVID-19,也可能已经从COVID-19中恢复。

FMT捐赠者应该是健康的,没有已知的胃肠道疾病或最近进行抗生素治疗(90天内)。如果捐赠者有可能与肠道微生物群改变相关的病史(如自身免疫性疾病、代谢综合征、肥胖等),也应排除他们。在COVID-19大流行期间和之后,制定更加一致和基于证据的FMT筛查方案比以往任何时候都更加重要。SARS-CoV-2主要通过肺泡上皮细胞上存在的血管紧张素转换酶2 (ACE2)受体引起肺部感染。ACE2受体也存在于身体的其他部位,包括肾脏、心脏、肝脏、眼睛、口腔粘膜的上皮细胞和肠道。虽然SARS-CoV-2的传播被认为主要通过呼吸道飞沫,但肠道也可能参与COVID-19的发病机制,因为肠道上皮细胞,特别是小肠的肠上皮细胞也表达ACE2受体。过去的研究也报道了感染者的胃肠道症状和粪便样本中存在SARS-CoV-2病毒颗粒。有研究表明,一些患者在呼吸样本阴性后,粪便中仍有可检测到的病毒RNA。
此外,有研究表明,在SARS-CoV-2感染过程中,肠道ACE2表达下调,导致抗菌肽(AMPs)分泌减少,提高病原体的生存。因此,随着COVID-19大流行在全球蔓延,迫切需要采取预防措施,对FMT捐赠者进行SARS-CoV-2筛查,以预防COVID-19传播的潜在风险。COVID-19可能通过FMT从无症状供体传播给受者,特别是那些通过呼吸道样本检测COVID-19阴性但粪便样本检测呈阳性的人。
为了解决这一问题,FMT捐献者筛查应该严格,并遵循每个司法管辖区的指导方针。目前,FDA建议只有从2019年12月1日之前捐赠的粪便中产生的FMT产品才能使用,直到获得适当的检测和筛查方案。因此,OpenBiome一直在遵循这一指导方针,并在该日期之后对所有捐赠者的粪便进行测试。如果捐赠者的检测呈阳性,所有材料将在检测日期前28天销毁。此外,捐赠者将被搁置,并被排除在至少八周内提供捐赠。香港中文大学的FMT中心是亚洲最大的FMT提供者之一,作为预防措施,该中心也隔离了自2019年11月1日以来捐赠的所有捐赠材料。如果在FDA推荐的时间表之前没有捐赠的粪便,使用粪便样本对捐赠者进行新冠肺炎筛查是至关重要的。粪便的单一阴性检测不足以排除SARS-CoV-2的存在。因此,可能需要在不同时间点进行多次测试。捐赠者的同意将需要修改,以接受在检测和捐赠过程中感染新冠肺炎的潜在风险。此外,最初的面谈可以虚拟地进行,以保护候选捐赠者和医疗保健提供者。医生应筛查:(1)捐赠者在过去30天内有无典型的新冠肺炎症状;(2)捐赠者在之前30天内曾去过新冠肺炎疫区或与确诊或疑似感染的个人有过密切接触。因此,在临床评估过程中,如果潜在捐赠者有任何新冠肺炎症状,应该将他们排除在下一阶段的实验室筛查和捐献过程之外。如果捐赠者通过问卷调查,他们将接受包括SARS-CoV-2在内的实验室检测。虽然SARS-CoV-2的检测可以通过鼻咽拭子进行,但如果有有效的检测,最好是直接检查粪便样本。在“自然”杂志最近的一项民意调查中,89%的科学家认为SARS-CoV-2很有可能或很可能成为一种地方性病毒。因此,在流行国家,应该考虑对所有捐赠者进行实时RT-PCR检测。同样值得一提的是,在新冠肺炎之前,相当大比例的潜在捐献者(60%-90%)可能无法通过筛查方案,其中大多数是在健康面谈和体检期间。在新冠肺炎期间和新冠肺炎之后,这一失败率可能会上升,这将使捐赠者的招募和留住变得更加具有挑战性。随着新出现的病原体可以通过粪便传播,捐赠者筛查将需要不断进步;然而,这仍然不能完全消除疾病传播的风险。因此,迫切需要更精细的生物疗法。这导致了对无菌粪便滤液转化及其对rCDI疗效的探索。在Ott及其同事的初步研究中,无菌粪便滤液转化预防了5名患者的rCDI复发。在对89名rCDI患者进行的2期临床试验中,早期植入SER-109已被证明可以减少CDI的复发。微生物生态系统疗法(MET-2)是第一个被定义的、不依赖供体的生物疗法,是一种由40种冻干共生细菌组成的口服胶囊制剂。它们最初是从健康捐赠者的粪便中分离出来的,后来可无需粪便制造。有研究发现MET-2有与FMT类似的预防CDI复发的效果,为已定义的生物疗法提供了原则证据。
COVID-19和FMT功效
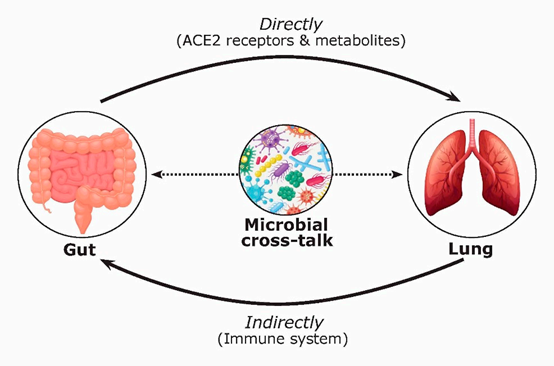
众所周知,肠道微生物区系在人体新陈代谢、免疫和疾病中起着至关重要的作用。到目前为止,FMT的疗效被归因于通过植入恢复了正常的肠道微生物群组成和功能,以及供体和受体细菌菌株的持续共存。此外,肺部和肠道微生物区系(称为肠-肺轴)之间的相互作用是双向的;肠道微生物区系可以直接(通过代谢物)或间接(通过免疫系统)影响肺部,肺部的不同微生物及其炎症也可以影响肠道微生物区系。
自大流行开始以来,肠肺轴已经产生了大量的报道。例如,De Oliveira及其同事的一篇综述强调了肠肺轴及其生物失调,以及新冠肺炎常见的胃肠道表现。然而,关于微生物的功能活性和代谢产物的讨论,以及它们对FMT治疗的影响,都被忽视了。聚焦于新冠肺炎,我们假设新冠肺炎感染期间的双向肠肺轴可以直接(通过ACE2受体和肠道微生物代谢产物,如短链脂肪酸和胆汁酸)和间接(通过免疫系统)影响肠道和肺。
先前的研究表明,超过60%的新冠肺炎患者有胃肠道症状,并报告有胃肠道症状的证据,如腹泻、恶心和呕吐。与健康参与者相比,新冠肺炎患者也有更多的条件致病菌、曲霉和念珠菌等机会性真菌。相反,有益的共生菌与新冠肺炎严重程度呈负相关。
单链脂肪酸的形成是由于复杂碳水化合物的发酵影响了一系列宿主过程,包括宿主-微生物信号、能量利用和结肠pH的控制,从而影响微生物区系组成和肠道动力。最丰富的短链脂肪酸是醋酸、丙酸和丁酸。这些微生物衍生的代谢物在肠道和呼吸道也有抗炎作用,这可能解释了它们对新冠肺炎感染的保护作用。因此,生物疗法的作用可能是一种重要的工具,用于控制新冠肺炎的过度炎症,降低病毒性呼吸道感染的发生率、持续时间和严重程度。
胆汁酸被认为具有抗炎作用,可以通过法尼类X受体和膜G蛋白偶联的胆汁酸受体Gpbar-1抑制NF-κB依赖的促炎细胞因子的转录。此外,UDCA还被证明能在脂多糖引起的肺水肿中刺激肺泡液清除,从而改善急性呼吸窘迫综合征。因此,胆汁酸在新冠肺炎感染中的潜在保护和治疗作用有待进一步研究。促炎细胞因子的增加,被称为“细胞因子风暴”,与严重的SARS-CoV-2感染有关,清楚地反映了宿主免疫功能的失控失调。这种增强的细胞因子和趋化因子的产生可能导致肺部严重急性呼吸综合征和多器官衰竭。肠道微生物区系不仅影响先天免疫反应,还促进CD8+T细胞效应器功能,这是一个涉及病毒(流感)清除的过程。
在中国武汉进行的一项研究调查了肠道菌群组成与健康人感染SARS-CoV-2的易感性的关系。郭台铭和他的同事表明,类杆菌属和链球菌,以及梭状芽孢杆菌目,与大多数被测试的细胞因子(IL-1β,IL-2,IL-4,IL-6,IL-8,IL-10,IL-12p70,IL-13,肿瘤坏死因子-α和干扰素-γ)呈负相关,而乳杆菌属,反刍球菌属和布鲁氏菌属与上述细胞因子呈正相关。因此,阐明肠道微生物区系和肠肺轴在呼吸系统疾病中的作用,以揭示它们在新冠肺炎治疗中的作用是非常重要的。相反,新冠肺炎等病毒性呼吸道感染会影响肠道微生物区系,导致需要抗生素治疗的细菌感染,这也会增加急性呼吸道感染的风险,增加对FMT的需求。新冠肺炎可能通过ACE2受体影响肠道,该受体可以调节肠道氨基酸的动态平衡、AMPs的表达、肠道炎症以及肠道微生物群落的生态。在SARS-CoV-2感染期间,ACE2的表达下调,导致肠道微生物群失调,破坏代谢平衡,并改变肠道代谢产物的水平。例如,SARS-CoV-2已被证明可以降低SCFA丁酸盐,后者是肠道和肺部免疫系统的关键调节剂。这些变化是否会影响肠道粘膜的完整性、引发炎症和细胞因子的释放仍有待研究。此外,在SARS-CoV-2感染患者的临床样本中观察到普雷沃特菌增加,乳杆菌和双歧杆菌减少。因此,可以合理地假设,新冠肺炎可以影响血管紧张素转换酶2受体的表达、肠道微生物代谢物(即单链脂肪酸和胆汁酸)的产生以及免疫系统,并且新冠肺炎感染者与健康非感染者相比存在显著差异。然而,这种变化会持续多久,以及所有这些变化是否都是可逆的,还不得而知。
该文强调迫切需要为粪便捐赠者制定全面和优化的筛查方案,以确保在新冠肺炎期间和新冠肺炎大流行后进行FMT的安全性和有效性。肠道微生物组成和功能与新冠肺炎之间的相互作用,以及性别、年龄和种族等人口统计因素,说明了涉及健康和疾病状态的复杂宿主因素。虽然COVID-19疫苗的竞赛仍在继续,但揭示新冠肺炎和肠肺轴的双向效应对于调整传统的FMT策略,以在大流行期间和之后保持安全和有效至关重要。此外,阐明肠道微生物区系和肠道-肺轴在呼吸系统疾病中的作用,可以在未来为新冠肺炎和其他流行病提供基于微生物群的新的预防和治疗干预措施。
原文出处
Kazemian N, Kao D, Pakpour S. Fecal Microbiota Transplantation during and Post-COVID-19 Pandemic. Int J Mol Sci. 2021;22(6):3004. Published 2021 Mar 16. doi:10.3390/ijms22063004


