Circ Res:南京医科大学季勇等表明NEDD4介导的GSNOR降解加重心脏肥大和功能障碍!
时间:2025-02-01 12:08:47 热度:37.1℃ 作者:网络
S-亚硝基谷胱甘肽还原酶(GSNOR)的减少导致S-亚硝基化的升高,从而加剧了对血流动力学应激反应的心肌病的进展。然而,GSNOR下降的机制仍不清楚。
2025年1月23日,南京医科大学季勇、Xie Liping、哈尔滨医科大学Han Yi共同通讯在Circulation Research在线发表题为“NEDD4–Mediated GSNOR Degradation Aggravates Cardiac Hypertrophy and Dysfunction”的研究论文,该研究表明NEDD4介导的GSNOR降解加重心脏肥大和功能障碍。

心血管疾病在全球越来越普遍,死亡率很高。心脏肥大是一种常见的病理过程,发生在应激诱导的心力衰竭期间,是随后心脏疾病的独立风险因素;然而,心肌梗塞和肥大的潜在机制仍不清楚,新的治疗策略迄今尚未充分发展。NO是一种高度保守的信号分子,在许多生物过程的调节中起着关键作用。NO生物功能的机制是通过蛋白质特定半胱氨酸残基中的S-亚硝基化(SNO)。SNO是一种非酶反应,主要由目标蛋白质结构和局部NO浓度决定。S-亚硝基谷氨酰胺硫酮(GSNO)被认为是NO的主要储库,可被高度保守的GSNO还原酶(GSNOR)不可逆地分解。GSNOR是维持NO和NO平衡的关键调节剂GSNOR活性或水平的波动可以显著影响细胞稳态和存活。
GSNOR的下调可导致SNO水平增加,促进心脏重塑和心力衰竭。GSNOR缺乏导致钙调素的SNO水平增加,加重由β肾上腺素能刺激引发的心脏肥大。同样,GSNOR诱导的MLP SNO(肌肉LIM蛋白)的下调加重炎症并进一步导致心脏肥大。大多数研究关注GSNOR缺乏的结果,但忽略了导致其功能丧失的上游事件。理解GSNOR下调的原因至关重要,因为对其进行干预可以防止心脏肥大。
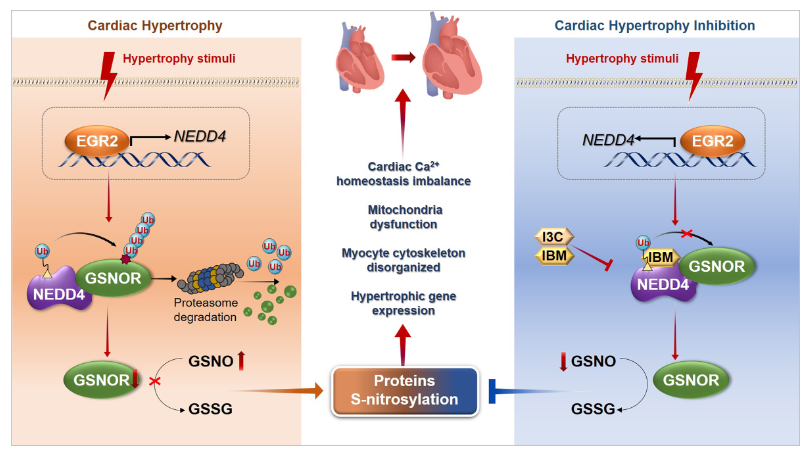
机理模式图(图源自Circulation Research)
NEDD4(表达发育下调的神经元前体细胞4),也称为NEDD4-1,是NEDD4家族中的一种E3 Ub(泛素)连接酶,含有HECT结构域。它通过不同靶点的泛素化在各种发病机制中发挥重要作用。最初确定NEDD4是心肌细胞中GSNOR的唯一E3 Ub连接酶,并在心脏肥大模型中观察到NEDD4的显著上调。最近的研究表明,NEDD4缺乏调节血管内皮细胞的血管钙化和功能障碍,也与心脏发育有关。然而,NEDD4在对血流动力学应激的心脏肥大反应中的确切作用在很大程度上仍未被探索。
在这里,研究人员确定NEDD4(表达发育性下调的神经元前体细胞4)是一种新的分子,它通过调节GSNOR水平,在压力超负荷诱导的心脏肥大的发病机制中起关键作用,从而显示出显著的治疗潜力。在肥大患者和横主动脉缩窄诱导的小鼠的心肌样本中,GSNOR蛋白水平降低,而mRNA水平保持不变,表明GSNOR受泛素化调节。NEDD4是一种E3 Ub连接酶,与GSNOR泛素化相关,在肥大心肌样本中表现出明显更高的表达水平。
此外,NEDD4酶死亡突变体或GSNOR非泛素化突变体降低了GSNOR泛素化并抑制了心脏肥大生长。心肌细胞特异性NEDD4缺陷抑制体外和体内心肌肥大。NEDD4抑制剂IBM有效抑制GSNOR泛素化和心脏肥大。临床上,吲哚-3-甲醇,一种NEDD4抑制剂,在II期临床试验中用作抗肿瘤药物,显示出相当的疗效。该研究发现表明,上调的NEDD4导致GSNOR泛素化和随后的降解,从而促进心脏肥大的进展。NEDD4抑制剂可作为治疗心脏肥大和心力衰竭的潜在治疗策略。
参考消息:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.124.324872


