中山大学AM:电活性敷料通过选择性吸收渗出液治疗复杂伤口
时间:2025-01-29 12:09:53 热度:37.1℃ 作者:网络
渗出液管理与细胞活性增强对复杂伤口愈合至关重要。然而,目前的渗出液管理敷料不加选择地去除渗出液,这对细胞活性增强是不利的。在此,中山大学吴丁财/王辉/黄榕康&南方医科大学广东省人民医院李勇开发了一种新型的电活性双层(cMO/PVA)敷料,通过构建装饰有二氧化锰纳米针簇的商用碳布(MO),原位浇铸聚乙烯醇(PVA)水凝胶,最后进行充电。得益于MO的分级纳米针簇结构,大量的活性位点得以充分暴露,实现了高比电容(例如1881.3 mF cm⁻²),从而为cMO/PVA敷料建立了持久的电场。这种独特的cMO/PVA敷料能够在渗出液管理过程中对有害物质相对于营养物质实现非凡的选择性吸附。同时,其长期电刺激疗法可以促进细胞增殖和迁移,并增强抗菌性能。因此,该多功能cMO/PVA敷料能够迅速修复II型糖尿病大鼠的全层伤口,为复杂伤口的治疗提供了一种先进的策略。该研究以题为“Electroactive Dressing with Selective Sorption of Exudate Enables Treatment of Complicated Wound”的论文发表在《Advanced Materials》上。

图1展示了电活性双层敷料(cMO/PVA)的制备过程及其促进复杂伤口愈合的原理。通过将二氧化锰纳米针簇装饰在商用碳布上,原位浇铸聚乙烯醇(PVA)水凝胶,并进行充电,成功制备了cMO/PVA敷料。该敷料利用MO层丰富的活性位点和高比电容(1881.3 mF cm⁻²),建立了持久的电场,实现了对有害物质的选择性吸附,同时通过长期电刺激促进细胞增殖和迁移,增强抗菌性能,从而加速复杂伤口的愈合。
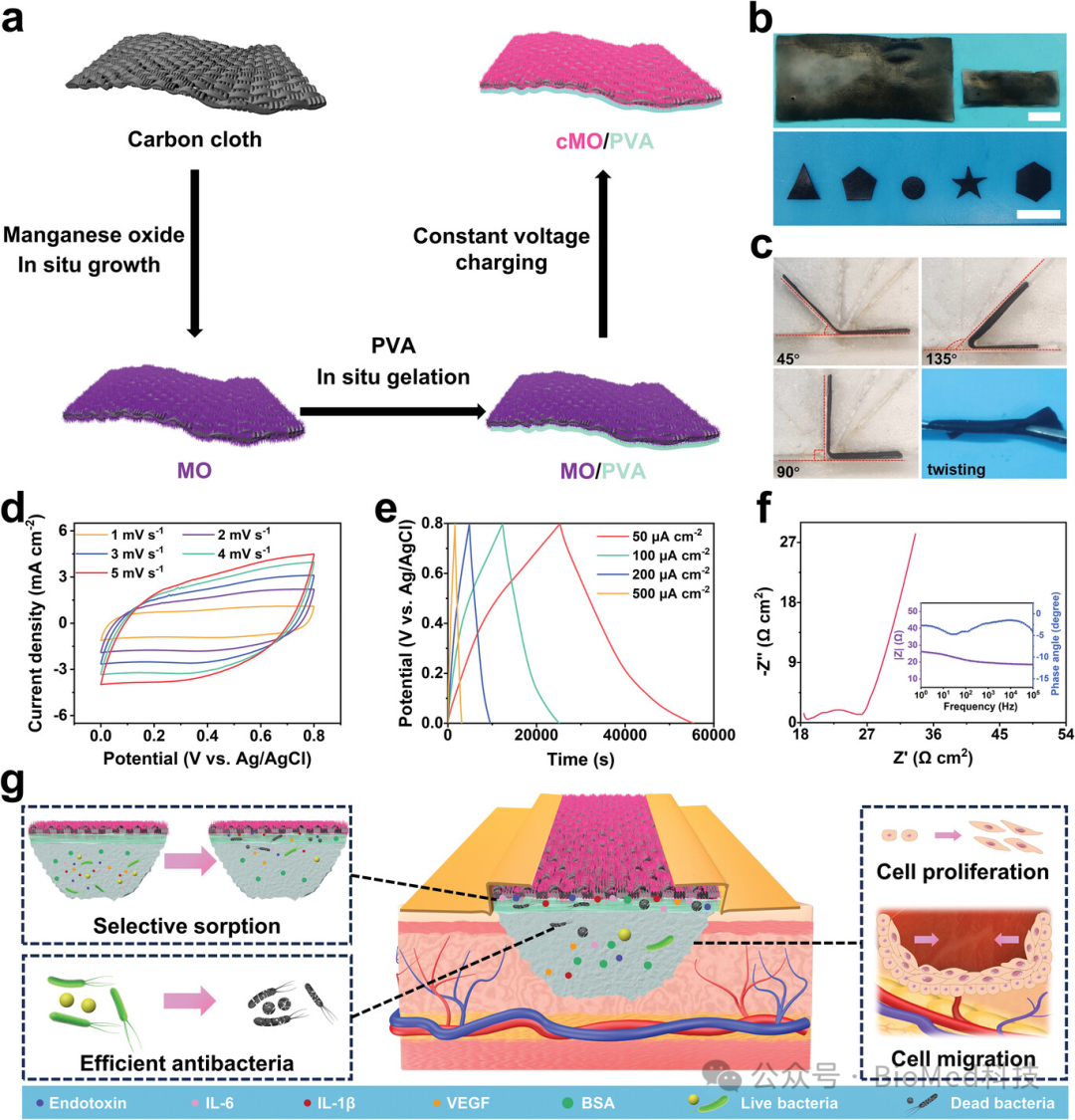
图1. 新型电活性双层敷料制备示意图及特性
【cMO/PVA敷料的抗菌性能】
图2展示了cMO/PVA敷料的抗菌性能和生物相容性。实验结果表明,cMO/PVA敷料对大肠杆菌和金黄色葡萄球菌具有极高的抗菌效率,达到99.99%,远高于未充电的uMO/PVA敷料和纯PVA敷料。此外,cMO/PVA敷料在模拟湿环境中仍保持优异的抗菌性能。生物相容性测试显示,cMO/PVA敷料对成纤维细胞的细胞活性无显著影响,细胞存活率超过90%,表明其具有良好的生物相容性。这些结果表明,cMO/PVA敷料不仅具有强大的抗菌能力,还具备良好的生物相容性,适合用于复杂伤口的治疗。

图2. cMO/PVA敷料的抗菌性能
【cMO/PVA和uMO/PVA敷料对渗出液的吸附率】
图3展示了cMO/PVA敷料在渗出液管理中的选择性吸附性能和电场维持能力。实验结果表明,cMO/PVA敷料对内毒素的吸附比率高达77.1%,远高于未充电的uMO/PVA敷料(11.7%)。在模拟渗出液中,cMO/PVA敷料对有害物质(如IL-6和IL-1β)的吸附比率显著高于营养物质(如VEGF和BSA),显示出对有害物质的高选择性吸附能力。此外,通过模拟伤口系统测试,cMO/PVA敷料在连续泵送不同溶液(如模拟渗出液、内毒素、IL-1β、IL-6、VEGF或BSA溶液)时,能够维持稳定的电场,其电位水平在模拟伤口系统中与实际伤口应用中的电位相近,表明cMO/PVA敷料在实际应用中能够有效维持电场,从而促进细胞增殖和伤口愈合。这些结果表明,cMO/PVA敷料在渗出液管理中具有优异的选择性吸附性能和电场维持能力,为复杂伤口的治疗提供了一种有效的策略。
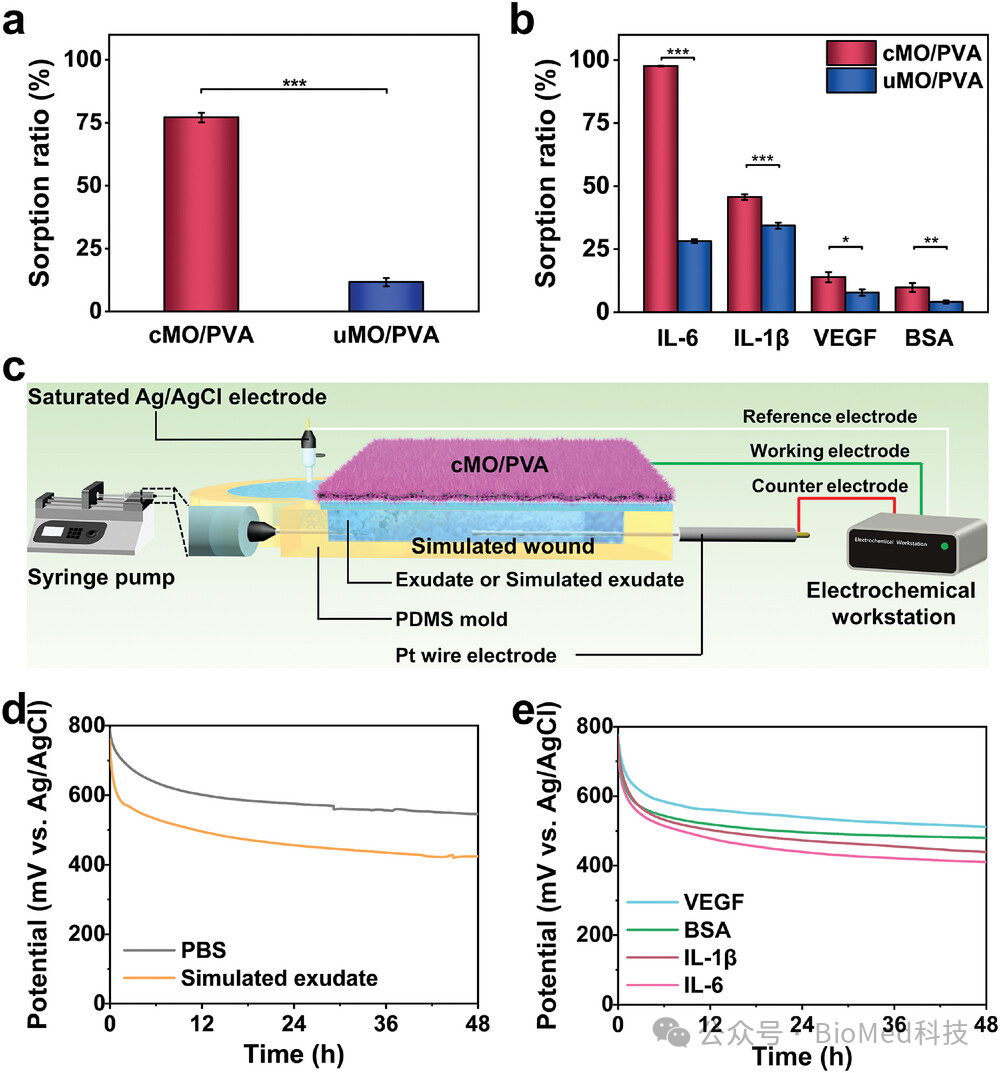
图3. cMO/PVA和uMO/PVA敷料对渗出液的吸附率
【cMO/PVA敷料对伤口愈合的影响】
图4展示了cMO/PVA敷料在II型糖尿病大鼠全层皮肤伤口模型中促进伤口愈合的效果。实验结果表明,cMO/PVA组在治疗期间展现出最显著的伤口愈合率,第5天和第15天的愈合率分别达到51.5%和99.8%。组织学水平上,cMO/PVA组在第7天和第15天展现出更强的肉芽组织形成和更快的上皮细胞再生,以及比其他组更密集的胶原纤维。定量分析显示,cMO/PVA组在第7天的胶原表达最高,第15天的再生表皮最厚,且胶原纤维排列最为有序。这些结果表明,cMO/PVA敷料通过选择性吸附渗出液中的有害物质和提供长期电刺激,显著促进了复杂伤口的愈合。
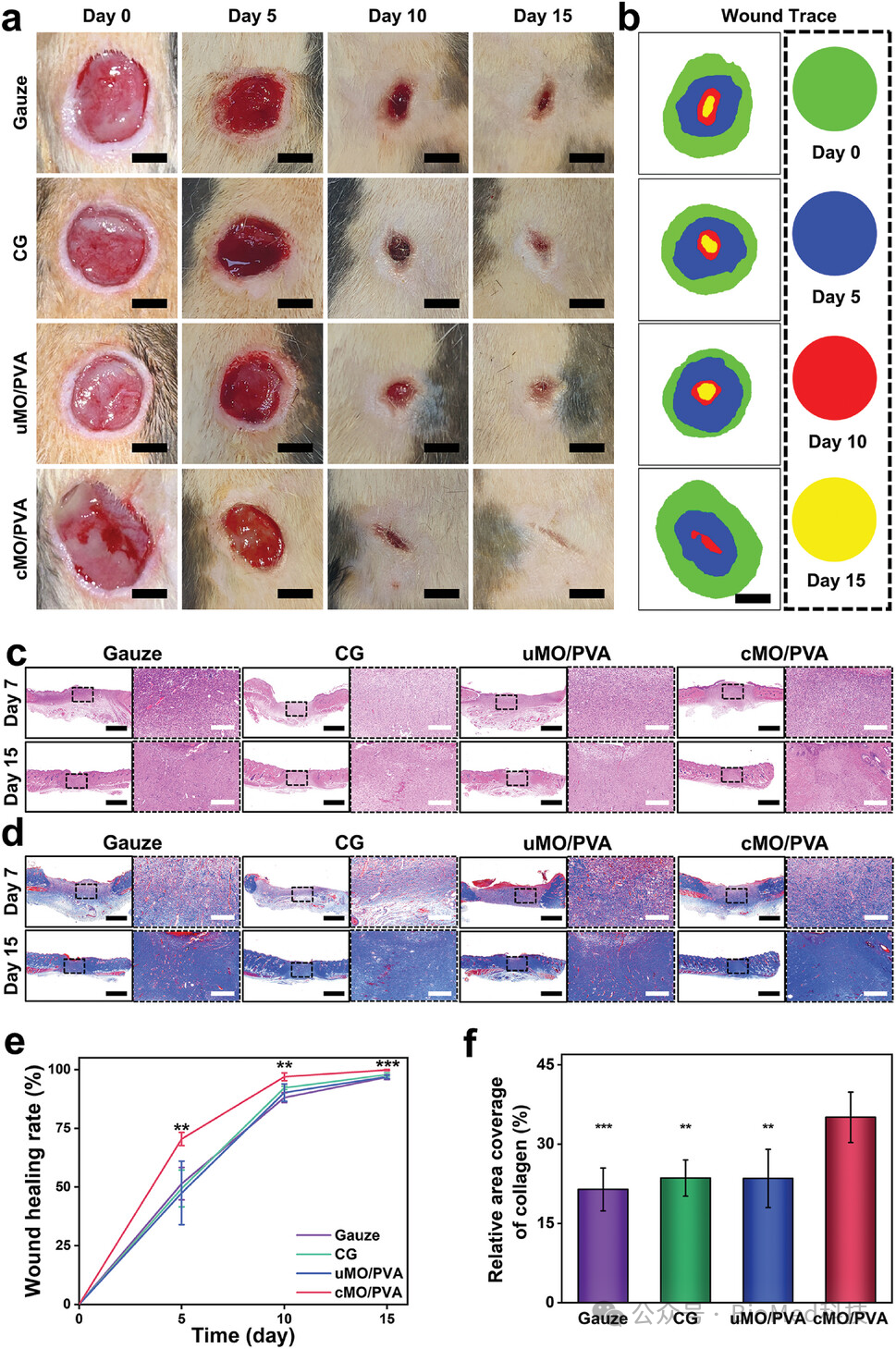
图4. cMO/PVA敷料对伤口愈合的影响
【免疫组化染色】
图5展示了cMO/PVA敷料在II型糖尿病大鼠全层皮肤伤口模型中对炎症反应、血管生成和无瘢痕愈合的影响。实验结果表明,cMO/PVA组在第7天和第15天的促炎细胞因子IL-6和巨噬细胞标志物CD68的表达水平最低,表明该敷料具有优异的抗炎性能。此外,cMO/PVA组在第7天的血管生成标志物CD31和α-SMA的表达水平最高,表明该敷料能够促进早期血管生成。而在第15天,这些标志物的表达水平降低,表明电刺激可能在早期促进血管生成,随后及时诱导不成熟血管退化和肌成纤维细胞凋亡,从而促进无瘢痕愈合。这些结果表明,cMO/PVA敷料通过选择性吸附渗出液中的有害物质和提供长期电刺激,不仅能够减轻炎症反应,还能促进血管生成和无瘢痕愈合,为复杂伤口的治疗提供了一种有效的策略。
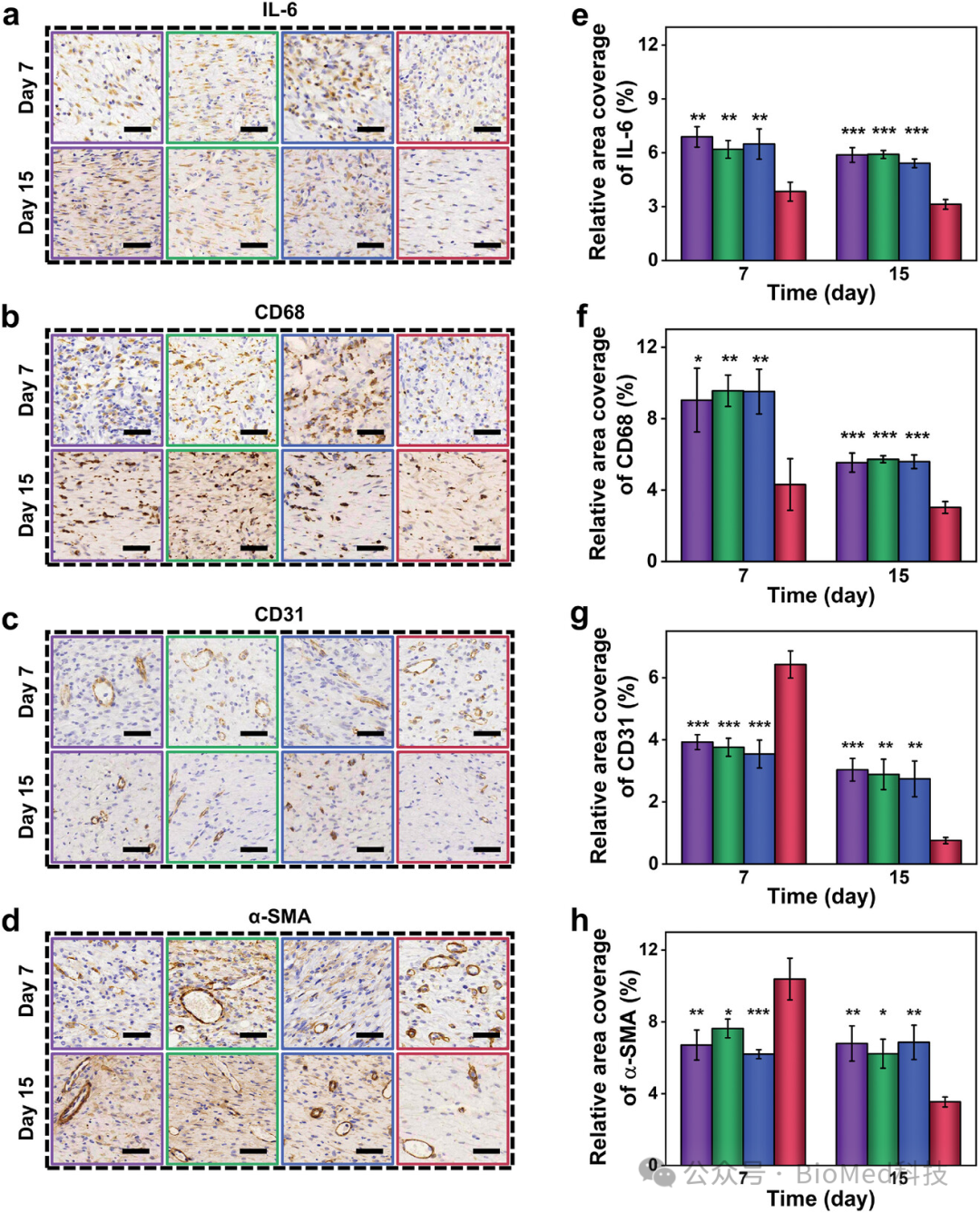
图5. 免疫组化染色
【小结】
本研究成功开发了一种新型的电活性双层敷料(cMO/PVA),该敷料通过构建二氧化锰纳米针簇装饰的商用碳布(MO)层、原位浇铸聚乙烯醇(PVA)水凝胶层,并最终进行充电制备而成。cMO/PVA敷料凭借MO层丰富的活性位点和高比电容(1881.3 mF cm⁻²),能够长时间维持有效的电场,从而在渗出液管理过程中优先吸附有害物质而非营养物质,显著减轻伤口炎症负担并改善微环境。同时,该敷料提供的长期电刺激疗法可促进细胞增殖与迁移,并增强抗菌性能。在II型糖尿病大鼠全层伤口模型中,cMO/PVA敷料展现出卓越的愈合效果,为复杂伤口的高效治疗提供了一种极具前景的新方法。
原文链接:
https://doi.org/10.1002/adma.202413320


