直肠肿瘤几乎完全消失,完全缓解患者翻倍,国内团队免疫治疗联合疗法让“冷”肿瘤变“热”
时间:2025-01-18 12:08:30 热度:37.1℃ 作者:网络
在全球范围内,结肠直肠癌是第三大常见癌症,其致死率仅次于肺癌。在中国,69.6%的直肠癌患者在确诊时已处于局部晚期(II/III期)。针对这类局部晚期直肠癌(LARC),临床指南推荐在手术前进行新辅助治疗,包括完全新辅助治疗或传统的新辅助放化疗,以提高手术成功率,甚至可能让患者有机会保留括约肌或避免手术。
近年来,新辅助免疫疗法在诱导肿瘤消退方面显示出显著成效,特别是在免疫活跃的“热肿瘤”中。在错配修复缺陷型LARC中,新辅助单药抗PD-1治疗甚至达到了100%的临床完全缓解率。然而,93%以上的LARC患者属于错配修复正常型(即“冷肿瘤”),单独免疫治疗的效果有限。因此,全球肿瘤学家正努力将冷肿瘤转化为热肿瘤,以优化免疫治疗环境。
近日,Nature Medicine期刊发表了POLARSTAR试验的研究成果。该试验揭示,在新辅助放化疗的基础上增加PD-1抑制剂,能够显著提升局部晚期直肠癌(LARC)患者的病理完全缓解(pCR)率,即原发病灶与淋巴结均无癌细胞残留,同时未引发显著的安全性问题。此研究的通讯作者包括来自北京友谊医院的张忠涛教授与姚宏伟教授、北京协和医院的肖毅教授,以及北京大学肿瘤医院的武爱文教授。

截图来源:Nature Medicine
已有研究表明,放疗能增强免疫检查点抑制剂(ICIs)的抗肿瘤作用。鉴于中低LARC患者常需新辅助放疗,将ICIs与放疗结合的临床试验显得尤为可行。之前的一些单组试验已报告了23%至48.1%的病理完全缓解(pCR)率,且安全性良好。鉴于pCR与直肠癌的总生存率密切相关,POLARSTAR试验将进一步评估在LARC新辅助放化疗中加入ICIs的有效性和安全性。
POLARSTAR是一项多中心、三臂、随机2期临床试验,涉及中国8家结直肠癌中心,共纳入186例18至75岁的直肠腺癌患者。患者以1:1的比例随机分组接受治疗,随后进行根治性手术。
试验分为三组:
新辅助放化疗+同步PD-1抑制剂组(同步治疗组,63例)、新辅助放化疗+序贯PD-1抑制剂组(序贯治疗组,62例)和单独新辅助放化疗组(61例)。三组的新辅助放化疗方案相同。
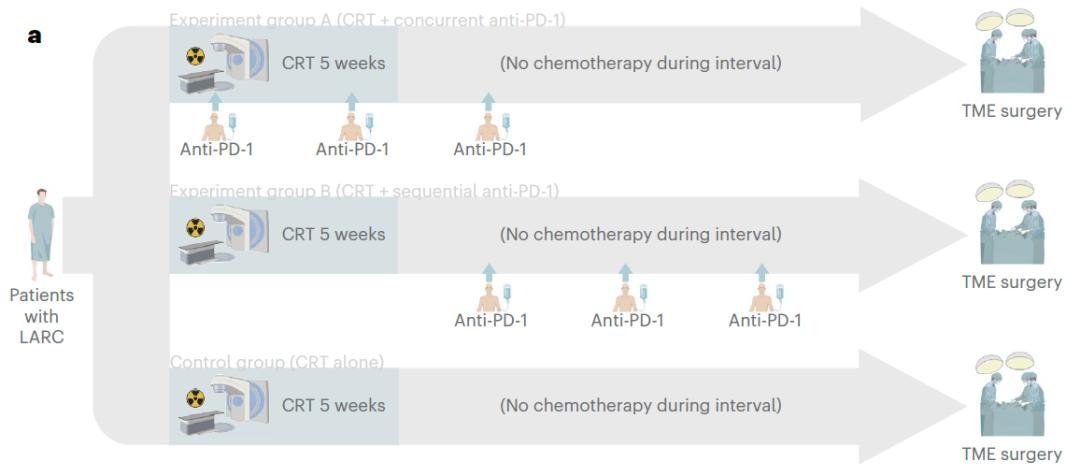
▲三组治疗方案
最终,分析纳入了171例患者,分为同步治疗组(59例)、序贯治疗组(56例)和单独新辅助放化疗组(56例)。研究结果显示,各组的病理完全缓解(pCR)率分别为:同步治疗组27.1%,序贯治疗组32.7%,单独新辅助放化疗组14%。与单独新辅助放化疗组相比,序贯治疗组的pCR率显著提高,患者比例近乎翻倍(风险比RR=2.332,95%置信区间CI:3.4%~34.0%,P=0.019),而同步治疗组与单独新辅助放化疗组之间的差异未达到统计学显著水平(P=0.082)。此外,无论采用何种统计方法分析,各组的结果均保持一致。
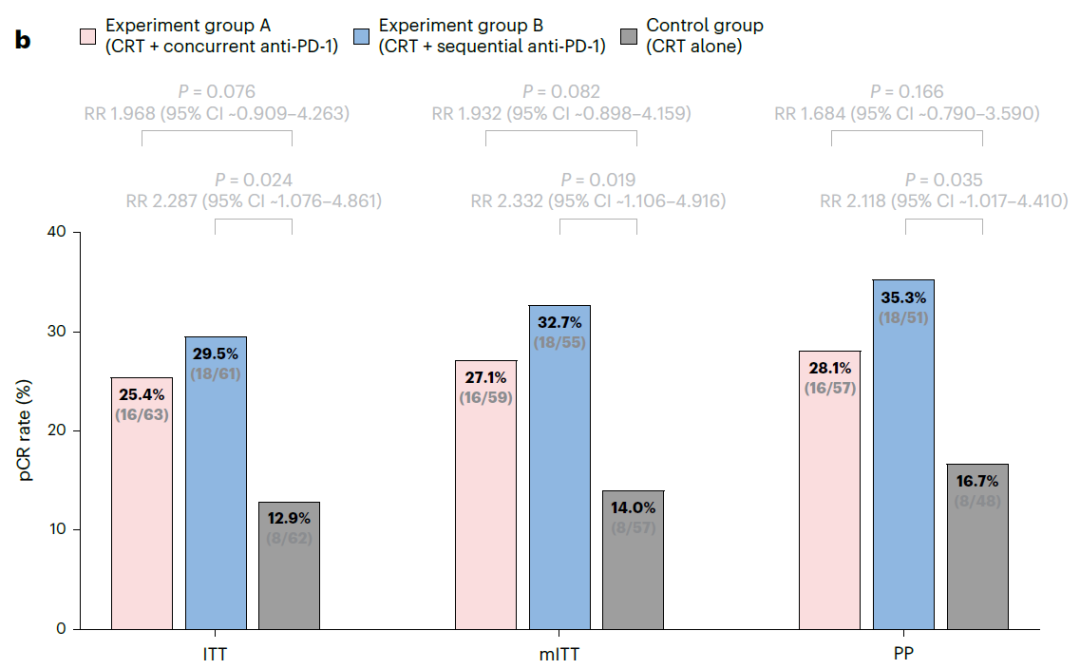
▲意向治疗人群(即最初符合纳入条件的186例患者,ITT)、修订后意向治疗人群(即被纳入主要分析的171例患者,mITT)和符合方案人群(即完全按照治疗方案进行治疗的患者,PP)的同步治疗组(粉色)、序贯治疗组(蓝色)和单独新辅助放化疗组(灰色)pCR率对比
研究人员认为,同步治疗组和序贯治疗组分别设计在放疗第8天和放疗结束后2周给予首剂PD-1抑制剂,旨在利用放化疗的微环境调节作用。序贯治疗组pCR率高于同步治疗组,可能原因是完成整个放化疗后,微环境变化更为彻底。在次要终点方面,无论是意向治疗人群、修订后意向治疗人群还是符合方案人群,同步治疗组和序贯治疗组在影像学和病理学结果方面均显示出相对于单独新辅助放化疗组的优势。尽管同步治疗组在主要终点上未表现出显著优势,但仍存在诱导病理学肿瘤消退的可能性。
总体而言,可初步认为,“新辅助放化疗+PD-1抑制剂”的组合,可有效促进肿瘤消退,且仍存在持续优化的潜力。这种组合模式或可作为传统治疗方式的补充,是一种有效且不良反应较少的方式。
参考来源:https://doi.org/10.1038/s41591-024-03360-5


