European Radiology:使用机器学习识别口腔癌放疗后CT定义的肌肉损失阈值
时间:2025-01-16 12:09:33 热度:37.1℃ 作者:网络
口腔鳞状细胞癌(OCSCC)是最常见的头颈部恶性肿瘤,2020 年全球约有 377713 例新发病例和 177757 例死亡病例。口腔鳞状细胞癌(OCSCC)的主要治疗方法是手术,辅助治疗则根据疾病范围和病理情况而定。辅助放疗可以改善有病理危险因素患者的局部区域控制和生存结局。然而,辅助放疗会引发诸如黏膜炎、吞咽困难和口干等急性毒性反应,这些反应可能导致患者营养状况恶化和骨骼肌流失。
骨骼肌已被认定为一种内分泌器官,能够产生和分泌肌动蛋白,以自分泌、旁分泌或内分泌的方式发挥作用。在头颈部癌症中,可以使用计算机断层扫描(CT)或磁共振成像(MRI)在第三颈椎(C3)水平对骨骼肌进行客观测量。这种方法使临床医生能够在临床实践中利用为放疗计划和随访而获取的计算机断层扫描(CT)或磁共振成像(MRI)扫描来评估肌肉变化。在口腔鳞状细胞癌(OCSCC)患者中,辅助放疗后通过计算机断层扫描(CT)测量到的肌肉流失与不良生存情况有关,不过,与生存相关的肌肉流失的最佳阈值仍有待阐明。这个阈值可能有助于临床医生识别放疗后肌肉流失严重的患者,并指导采取强化干预措施来改善肌肉量。
肌肉流失与生存之间的关联可能是非线性的,并且涉及复杂的相互作用,这使得确定肌肉流失的最佳阈值变得困难。机器学习(ML)能够处理非线性关系和复杂的相互作用,并且在预测临床结局方面表现出良好的性能。随着可解释人工智能的发展,SHapley Additive exPlanations(SHAP)方法可以通过可视化机器学习模型的内部工作原理来帮助解释模型,并确定与生存相关的肌肉流失的最佳阈值。尽管可解释人工智能已在肿瘤学中得到应用,但这种方法从未被用于探究口腔鳞状细胞癌(OCSCC)中肌肉流失与生存之间的关联或确定肌肉流失的阈值。

最近,发表在European Radiology 上的一篇文章利用可解释人工智能来确定口腔鳞状细胞癌(OCSCC)中与生存相关的肌肉流失阈值。
研究纳入了来自两家三级医疗中心的 1087 例接受手术及辅助放疗的口腔鳞状细胞癌(OCSCC)患者(推导队列中有 660 例,外部验证队列中有 427 例)。通过放疗前后在第三颈椎(C3)椎体水平的计算机断层扫描(CT)来测量骨骼肌指数(SMI)。构建了随机森林(RF)、极限梯度提升(XGBoost)以及分类提升(CatBoost)模型来预测全因死亡率,并使用受试者工作特征曲线下面积(AUC)评估它们的性能。运用 SHapley Additive exPlanations(SHAP)方法确定肌肉流失阈值,并通过考克斯回归分析进行验证。
在外部验证队列中,随机森林(RF)、极限梯度提升(XGBoost)以及分类提升(CatBoost)模型在预测全因死亡率方面均取得了良好的性能(受试者工作特征曲线下面积(AUC)分别为 0.898、0.859 和 0.42)。SHapley Additive exPlanations(SHAP)方法显示,放疗后骨骼肌指数(SMI)的变化是预测全因死亡率的最重要特征,并且在这三个模型中均一致确定骨骼肌指数(SMI)流失≥4.2% 为阈值。在多变量分析中,骨骼肌指数(SMI)流失≥4.2% 在两个队列中均与全因死亡率风险增加独立相关(推导队列:风险比为 6.66,p < 0.001;外部验证队列:风险比为 8.46,p < 0.001)。
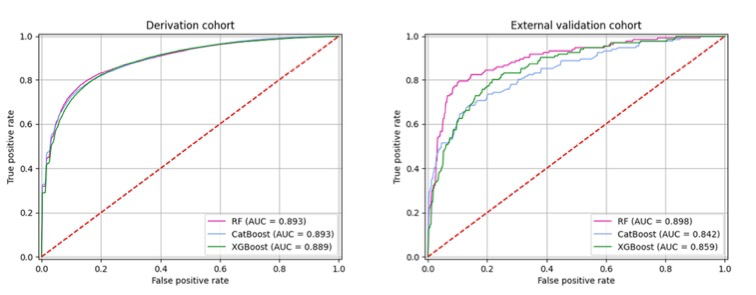
图 机器学习模型的受试者工作特性曲线
本研究结果有助于临床医生识别治疗后肌肉流失严重的患者,并指导采取干预措施来改善肌肉量。
原始出处:
Jie Lee,Jhen-Bin Lin,Wan-Chun Lin,et al.Identifying threshold of CT-defined muscle loss after radiotherapy for survival in oral cavity cancer using machine learning.DOI:10.1007/s00330-024-11303-4


