中山大学STTT:突破性进展!SHR-1701组合治疗显著提升晚期结直肠癌患者生存希望
时间:2024-12-19 12:00:34 热度:37.1℃ 作者:网络
转移性结直肠癌(mCRC)因其高死亡率和有限的治疗选择而成为一个重要的临床问题。尽管现有的治疗策略,如FOLFOX、FOLFIRI和XELOX等化疗方案结合靶向疗法(如贝伐珠单抗或西妥昔单抗),能够通过靶向特定分子途径来提高疗效,但患者的预后仍然很差,中位总生存期约为30个月。
免疫治疗的出现为癌症治疗带来了革命性的变化,尤其是在高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)的肿瘤中,免疫检查点抑制剂(ICIs)如帕博利珠单抗和纳武利尤单抗显示出显著的疗效。然而,MSI-H/dMMR肿瘤仅占晚期mCRC病例的约5%,而大多数患者具有错配修复正常(pMMR)或微卫星稳定(MSS)的肿瘤,对ICIs单药治疗的反应有限。
为了改善pMMR/MSS mCRC患者的预后,近期研究集中于组合疗法,这些疗法可能增强ICIs的疗效。将ICIs与化疗、靶向疗法或其他免疫调节剂结合使用,被假设可以通过增加新抗原释放和调节肿瘤微环境来增强抗肿瘤免疫反应。SHR-1701作为一种新型双功能融合蛋白,结合了针对PD-L1的单克隆抗体和转化生长因子-β受体II(TGF-βRII)的细胞外域,旨在同时抑制PD-L1介导的免疫检查点信号和在肿瘤微环境中隔离TGF-β配体,从而增强抗肿瘤免疫反应并克服mCRC中的免疫抵抗机制。
中山大学骆卉妍、徐瑞华和邱妙珍等人评估了SHR-1701与贝伐珠单抗和XELOX化疗联合使用作为不可切除mCRC的一线治疗的疗效和安全性。相关内容以“Addition of SHR-1701 to first-line capecitabine and oxaliplatin (XELOX) plus bevacizumab for unresectable metastatic colorectal cancer”为题发表在《Signal Transduction and Targeted Therapy》上。

【主要内容】
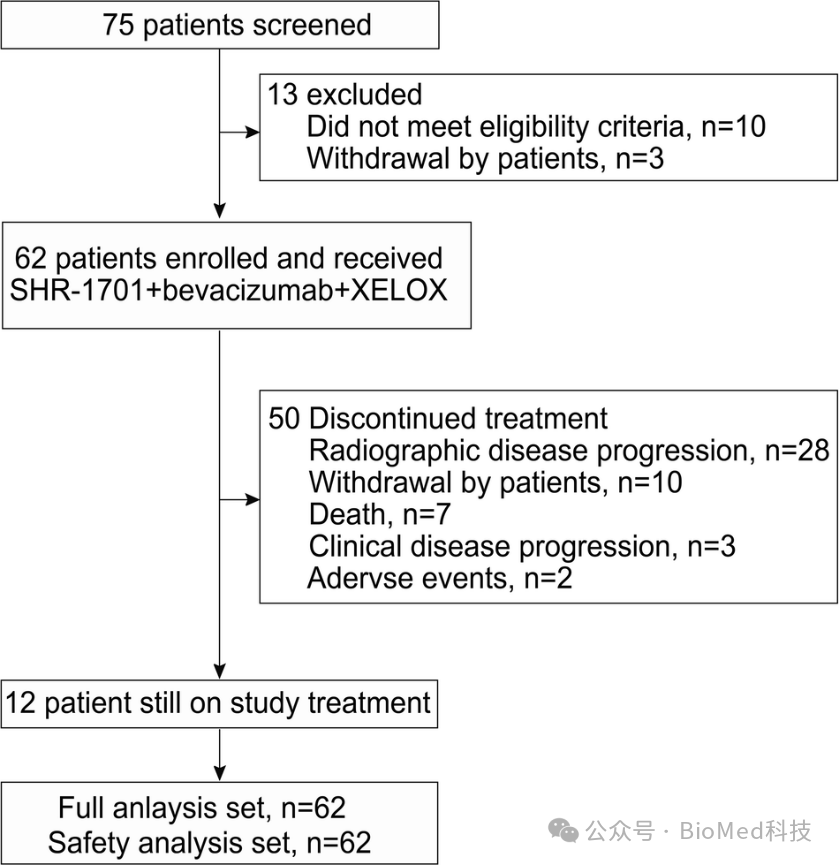
图1 研究流程图
文章采用了单臂的二期临床试验来评估SHR-1701联合XELOX和贝伐珠单抗的疗效和安全性。研究共纳入62名未经治疗的、组织学证实的结直肠腺癌患者,这些患者之前未接受过转移性疾病的系统治疗。患者接受SHR-1701(30 mg/kg)、贝伐珠单抗(7.5 mg/kg)和奥沙利铂(130 mg/m²)静脉注射,以及口服卡培他滨(1 g/m²,每日两次)的21天周期治疗。最多进行八个诱导周期,随后对有反应或疾病稳定的患者进行维持治疗。
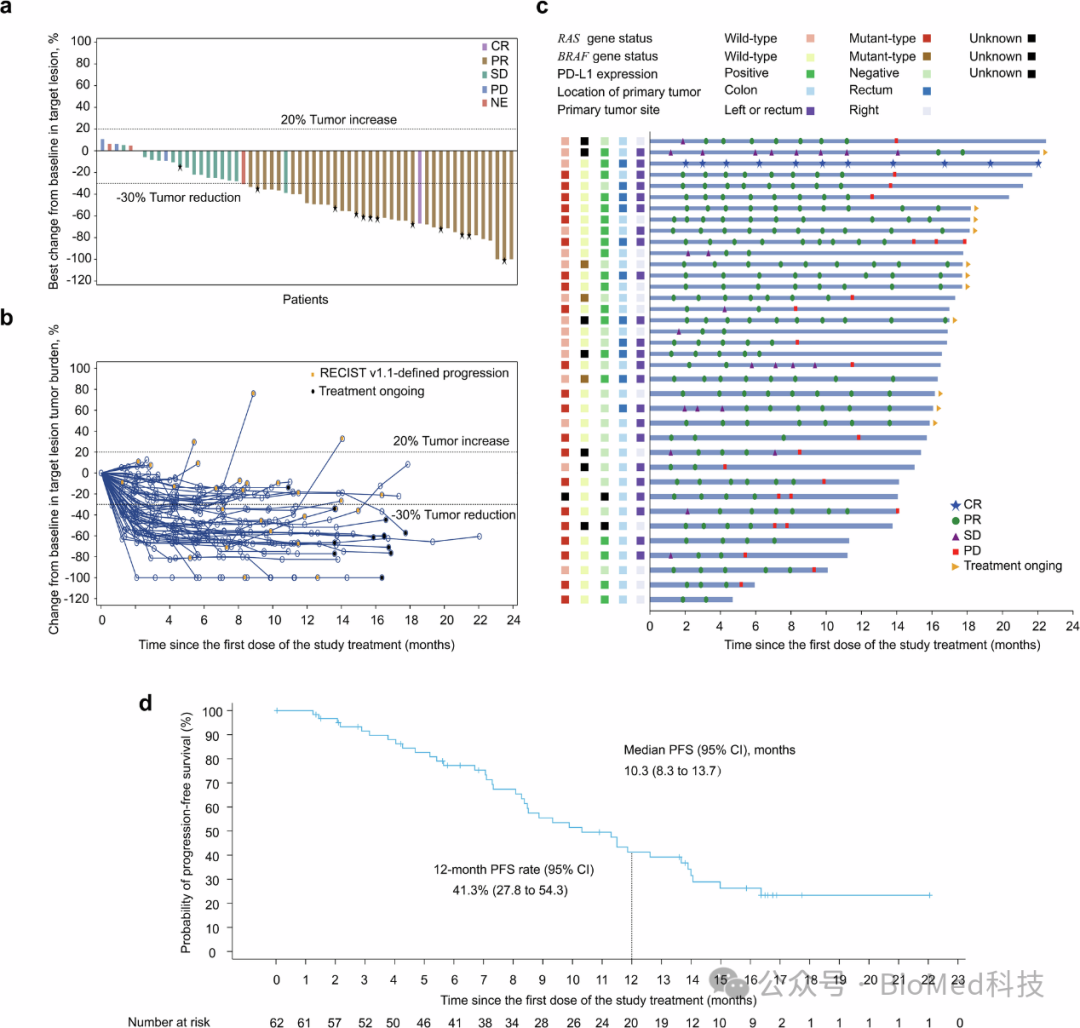
图2 SHR-1701联合治疗的抗肿瘤活性
这种组合疗法达到了59.7%的客观反应率(ORR)和83.9%的疾病控制率(DCR),中位无进展生存期(PFS)为10.3个月。这些数据表明,SHR-1701的加入显著增强了XELOX和贝伐珠单抗的抗肿瘤活性。此外,估计的12个月总生存率(OS)为67.7%。在安全性方面,研究显示SHR-1701联合疗法的不良事件发生率与已知的化疗和免疫治疗的毒性特征一致,未发现新的安全问题。这为该组合疗法的临床应用提供了重要的安全性数据支持。
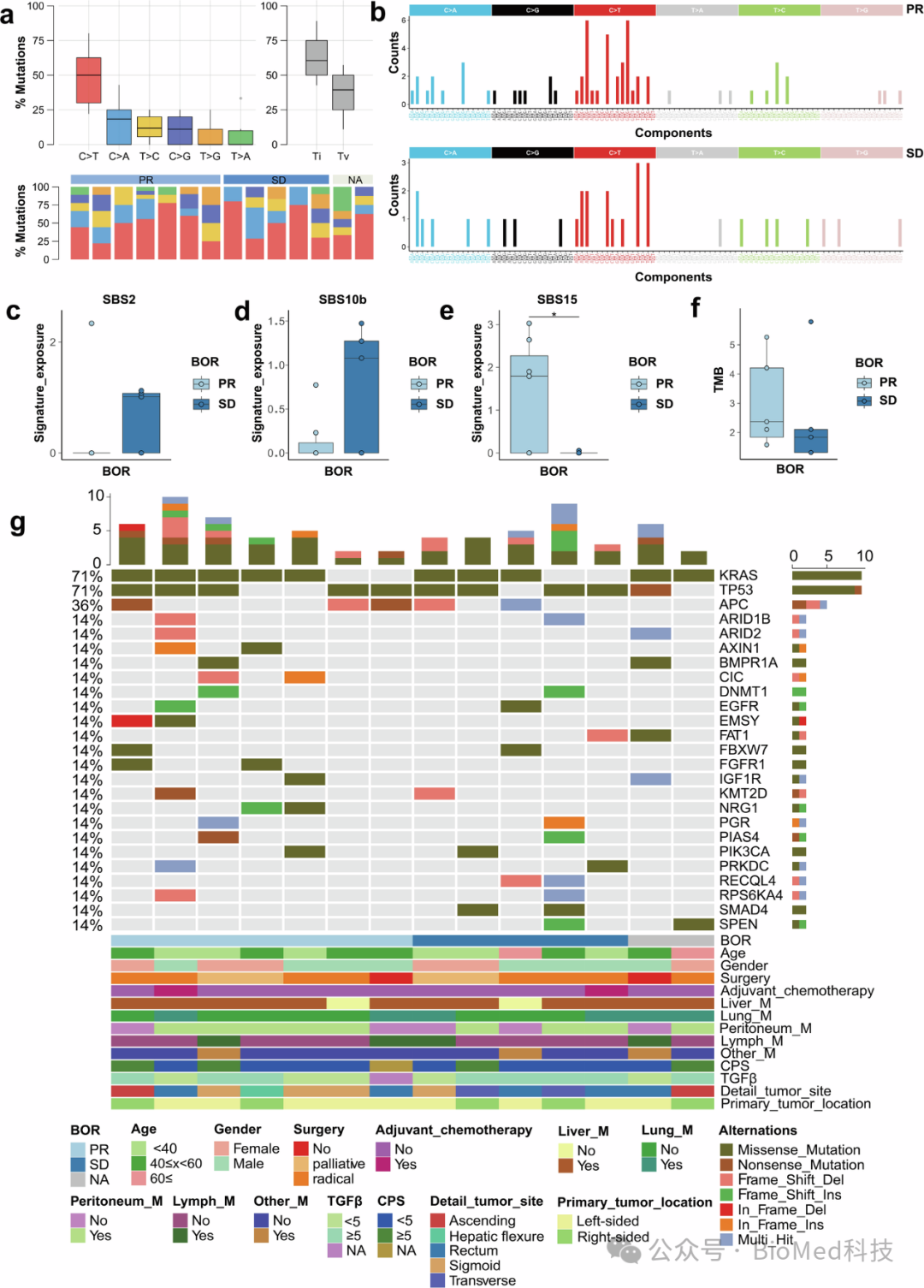
图3 基因组改变与SHR-1701临床反应
文章还进行了潜在生物标志物的探索,以预测治疗效果。研究发现,PD-L1表达、RAS基因状态和基线乳酸脱氢酶(LDH)水平可能与治疗反应相关。
【全文总结】
这篇文章通过一项精心设计的临床试验,展示了SHR-1701联合XELOX和贝伐珠单抗在不可切除mCRC中的潜在疗效和安全性。研究结果不仅为mCRC的治疗提供了新的治疗选择,也为未来的双途径抑制策略研究奠定了基础。然而,文章也指出了一些局限性,如缺乏对照组和随访时间的不足,这提示未来的研究需要更长时间的随访和更大规模的患者群体来验证这些初步发现。
未来的研究可能会集中在以下几个方面:首先,扩大样本量和延长随访时间以验证这些初步发现;其次,进一步探索和验证潜在的生物标志物,以实现个体化治疗;最后,探索其他可能的组合疗法,以进一步提高mCRC患者的治疗效果和生存质量。
原文链接:
https://doi.org/10.1038/s41392-024-02063-0


