郑大王永超/河南省人民医院张连仲/河南工业大学张贝贝AFM综述:声遗传学在肿瘤诊疗中的研究进展
时间:2024-12-15 12:00:27 热度:37.1℃ 作者:网络
癌症的诊断与治疗仍面临诸多挑战,因此,亟需发展精准且可控的策略以实现高效的肿瘤诊疗。声遗传学作为一种融合超声技术与基因工程的前沿技术,为这一难题提供了具有广阔前景的解决方案。通过利用超声技术的非侵入性特点以及深层组织穿透能力,声遗传学能够实现精准的肿瘤诊断与靶向治疗。

2024年12月10日,郑州大学生命科学学院王永超副研究员、河南省人民医院张连仲教授及河南工业大学李瑞芳教授团队合作,在国际知名期刊Advanced Functional Materials上发表题为“Ultrasound-Enabled Sonogenetics: Pioneering Advances in Cancer Theranostics”的综述文章,第一作者为河南工业大学张贝贝。该综述系统总结了声遗传学在癌症诊疗中的最新进展。文章详细阐述了超声的基本物理特性以及声遗传学的机理;同时,重点介绍了声遗传学在癌症治疗中的典型应用,包括基于工程化细胞、基于工程化细菌以及靶向肿瘤细胞的精准治疗。此外,文章还探讨了声遗传学在癌症诊断中的重要应用,特别是基于基因工程化气体泡囊及原位产生气体泡囊的技术,以实现高灵敏的肿瘤诊断。最后,文章对声遗传学面临的关键挑战及其临床转化前景进行了深入分析和展望。
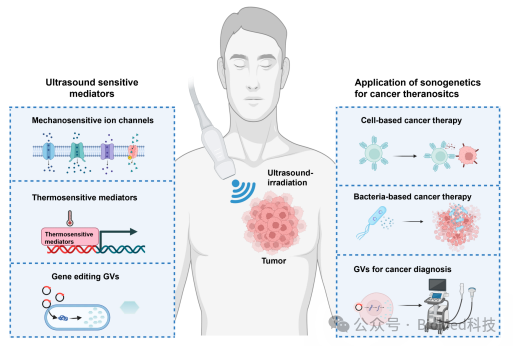
图1. 声遗传学在癌症诊疗中的应用。
本文要点
要点一:声遗传学的发展历史及机理
声遗传学是一种结合超声技术与基因工程的新兴技术,能够以非侵入性方式精确调控细胞活动,为癌症的诊断与治疗开辟全新途径。声遗传学的兴起源于克服传统技术(如光遗传学和磁遗传学)在监测与调控细胞过程中的局限性。相比之下,声遗传学以其非侵入性、高精度和深部组织穿透的优势,成为这些早期技术的理想替代方案。2014年,Heureaux提出利用超声操控细胞活动,为声遗传学的发展奠定了基础。随后,Ibsen于2015年正式提出声遗传学概念,并通过在秀丽隐杆线虫中过表达TRP-4蛋白,实现了超声诱导的行为调控。近年来,声遗传学研究呈现快速发展趋势,尤其是在超声敏感元件的鉴定和结构优化方面取得了重要突破。这些超声敏感元件可通过超声波激活,从而实现对细胞功能的靶向调控。
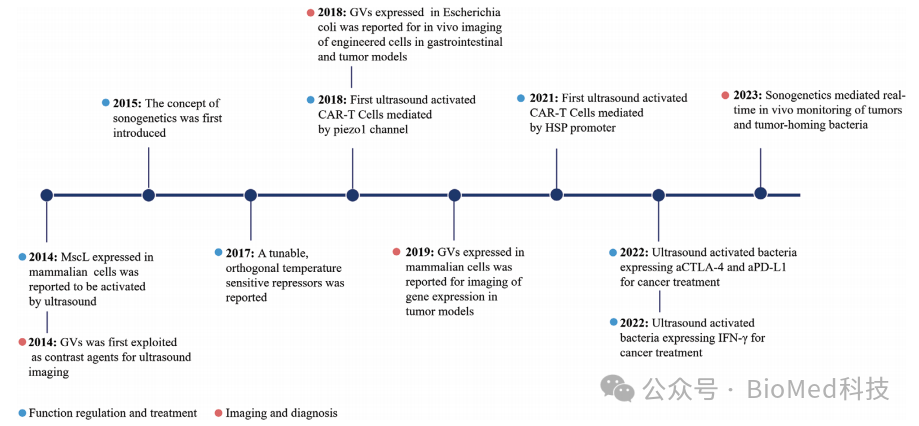
图2. 声遗传学重大进展的历史时间轴。
本文梳理了声遗传学的发展历程,并详细介绍了关键超声敏感元件,包括机械敏感离子通道、热敏蛋白以及基因编码的气体囊泡,这些元件共同构成了声遗传学机制的核心基础。机械敏感离子通道是整合于细胞膜中的蛋白质,能够响应超声波产生的机械力。在超声刺激下,这些通道会发生构象变化,从而打开离子通道,调节离子流动,实现对细胞活动的精确控制。除了机械敏感通道,声遗传学还利用热敏蛋白来调控细胞功能。热敏蛋白包括热敏启动子和抑制子,它们可以整合到遗传回路中,通过超声波引起的温度变化来控制基因表达。此外,基因编码的天然气体囊泡已被开发为一种极具前景的超声造影剂,用于癌症诊断。这些气体囊泡是充气的蛋白质纳米结构,可通过增强超声成像对比度,并通过在肿瘤原位产生的方式实现癌症的高灵敏检测。
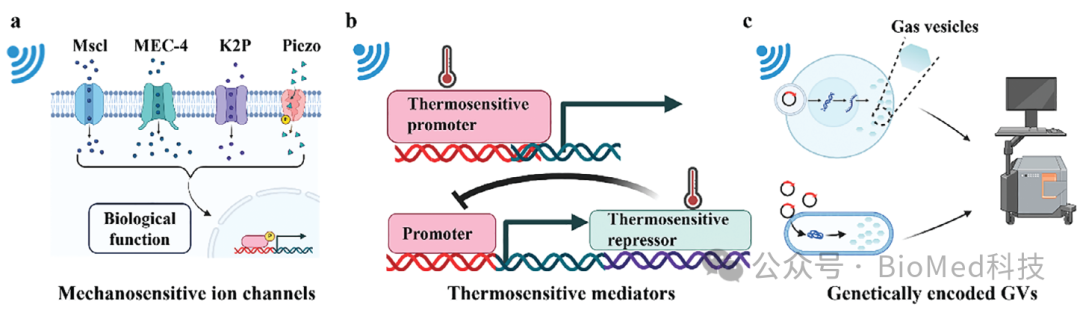
图3. 超声敏感元件及声遗传学机制示意图。
要点二:声遗传学在肿瘤治疗中的研究进展
在过去几十年中,癌症治疗取得了快速进展,细胞和细菌疗法作为具有潜力的治疗策略逐渐崭露头角。这些疗法通过基因工程改造的细胞或细菌,将治疗性物质递送或在肿瘤部位产生,从而提高治疗效果。然而,当前疗法仍面临较高的毒性和有限的可控性,亟需更精确、可控的治疗方法。声遗传学,作为一种新兴技术,利用超声波调节细胞功能,提供了一种创新的癌症治疗策略。本部分内容详细介绍了声遗传学如何通过超声刺激,激活基因改造的细胞和细菌,进而表达治疗性蛋白,如凋亡蛋白和免疫检查点抑制剂,实现有效的肿瘤治疗。此外,声遗传学还可以直接调节肿瘤细胞,诱导其凋亡并增强抗肿瘤免疫反应。由于其非侵入性、空间精确度和深度穿透能力,声遗传学为提高治疗效果、减少副作用提供了独特的优势。
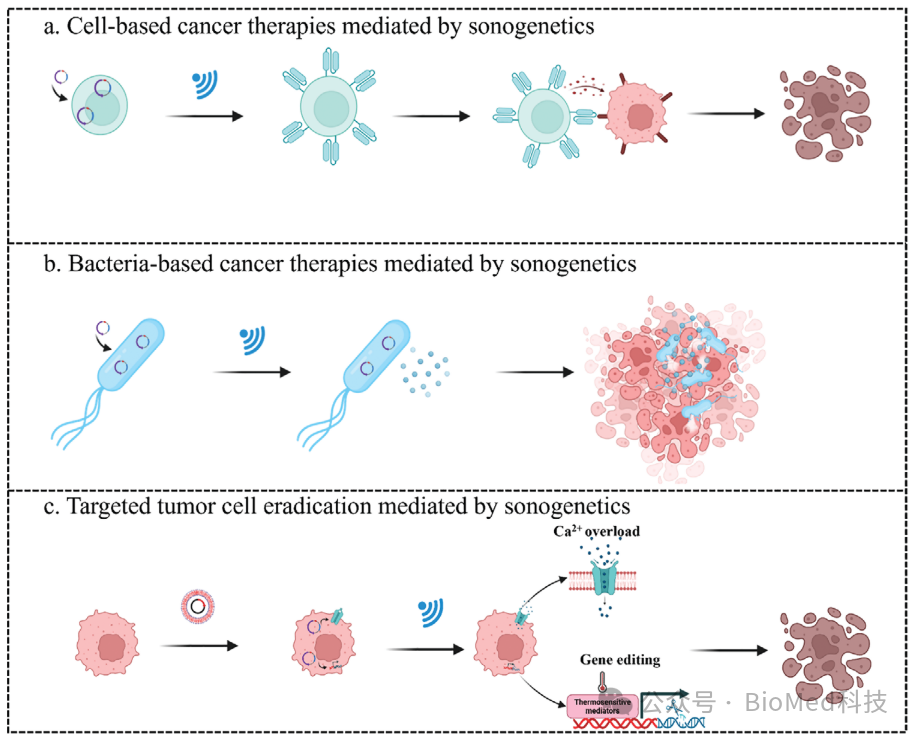
图4. 声遗传学在肿瘤治疗中的示意图。
要点三:声遗传学在肿瘤诊断中的研究进展
超声成像因其实时成像能力、非电离辐射和便携性在肿瘤的诊断中备受关注。传统超声成像是利用超声波在遇到密度差异的组织时产生的反射和散射而成像。然而,这种技术在空间分辨率上存在一定局限,尤其在区分声学性质相似的组织时表现不足。为提升空间分辨率,合成微泡作为超声成像造影剂被引入,从而发展出对比增强超声技术。微泡因其卓越的造影性能,大幅提高了成像对比度。然而,它们在稳定性和颗粒尺寸方面存在一定的技术瓶颈。为克服这些不足,基于声遗传学的超声成像技术结合超声波与基因编码的天然气体囊泡,为癌症诊断提供了一种创新且前景广阔的替代方案。特别地,结合基因工程的手段,气体囊泡能够在细菌(原核细胞)和肿瘤(真核细胞)中兼容表达,这使研究人员能够在活体内追踪肿瘤中的细菌群落,为深入了解肿瘤微环境以及肿瘤细胞与微生物组之间的相互作用提供了重要的技术手段。
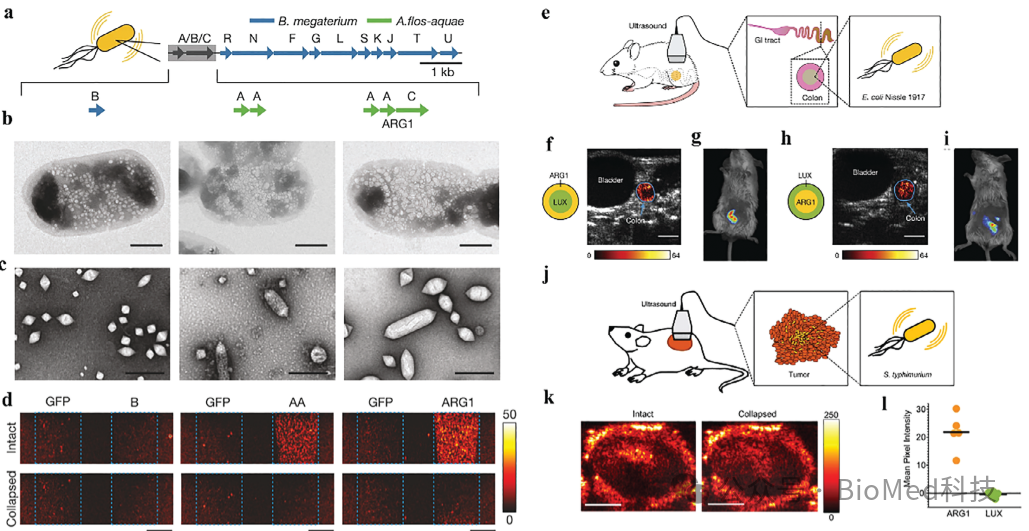
图5. 通过原位生成的气体囊泡对小鼠胃肠道和肿瘤组织中微生物的非侵入性成像。
总结与展望
尽管声遗传学在肿瘤的诊疗中取得了令人瞩目的进展,但该领域仍面临如下挑战:
(1)超声敏感元件的特异性和灵敏性性问题
开发具有高特异性和敏感性的超声敏感元件,是当前面临的主要挑战。现有的机械敏感离子通道和热敏蛋白往往缺乏足够的特异性,可能导致非特异性毒性。特别是热休克蛋白启动子不仅对超声引起的热敏感,还对其他刺激敏感,这增加了非特异性响应的风险。因此,亟需开发更加特异性和敏感性的超声敏感元件。
(2)声遗传学的安全性问题
高强度聚焦超声(HIFU)作为常用的手段被用于激活超声敏感元件以调控细胞功能。然而,HIFU可能对组织施加过高的热和机械应力,导致过热、空化诱发的组织损伤以及细胞结构的破坏。因此,开发能够通过传统或低强度超声波激活的声遗传工具具有重要意义。这类创新技术将有助于实现对细胞过程和分子靶点更精确、安全的调控,同时最大限度减少对健康组织的损伤。
(3)基因递送与声学报告基因的挑战
声遗传学在体内实现高效的肿瘤成像和靶向治疗,关键在于将编码超声敏感元件的基因精准且高效地递送至肿瘤细胞。然而,现有递送方法,如病毒载体或基于纳米颗粒的递送系统,仍面临诸多挑战,包括免疫原性、脱靶效应以及在实体瘤中的低转染效率。这些限制显著阻碍了声遗传技术的临床转化。因此,研发更加高效、靶向的基因递送技术是推动声遗传学发展的核心需求。此外,声学报告基因种类较少,这限制了在肿瘤中对不同细胞或分子靶点的多重成像的灵活性。因此,扩展报告基因库及优化基因表达效率,是提高临床应用转化的关键。
综上所述,声遗传学作为一项前沿技术,在肿瘤的诊断和治疗领域展现出了巨大的潜力。该技术利用超声波非侵入性穿透组织和精准调控基因表达的独特优势,为实时监测细胞过程和靶向癌症治疗提供了全新的策略。然而,目前声遗传学仍面临诸多技术挑战,包括超声敏感元件的特异性性、递送系统的高效性、声学报告基因的多样性以及专用超声设备的优化等。通过在这些关键领域的持续技术创新和突破,声遗传学有望克服现有障碍,为肿瘤的诊断和治疗提供新的技术手段。
原文链接:
https://onlinelibrary.wiley.com/doi/epdf/10.1002/adfm.202418748


