Nature子刊:杨辉/胥春龙/施霖宇/姚璇合作利用AAV递送RNA编辑工具,治疗神经系统罕见病
时间:2024-12-15 10:00:46 热度:37.1℃ 作者:网络
甲基CpG结合蛋白2 (MECP2)基因的重复引起MECP2重复综合征(MDS)。
2024年12月12日,辉大基因/中国科学院上海药物所杨辉、临港实验室胥春龙、辉大基因施霖宇、姚璇共同通讯在Nature Neuroscience(IF=21.2)在线发表题为“An RNA editing strategy rescues gene duplication in a mouse model of MECP2 duplication syndrome and nonhuman primates”的研究论文,该研究开发了一种高保真的Cas13Y(hfCas13Y)系统,该系统能够靶向MECP2(hfCas13Y- gMECP2)信使RNA,降解并降低人源化MECP2转基因小鼠大脑中的蛋白水平。
此外,脑室腺相关病毒(AAV)在新生儿或成年MDS小鼠中递送hfCas13Y-gMECP2恢复了失调的基因表达并改善了行为缺陷。值得注意的是,AAV9-hfCas13Y-gMECP2治疗使MECP2转基因小鼠的中位生存期从156.5天延长至226天。此外,对猴子的研究表明,单次注射AAV9-hfCas13Y-gMECP2足以在广泛的脑区中驱动hfCas13Y的稳健表达,MECP2的敲除效率达到52.19±0.03%,显著降低了生物标记基因GDF11的表达。研究结果表明,靶向RNA的hfCas13Y-gMECP2系统是一种有效的MDS干预手段,为治疗其他剂量敏感疾病提供了潜在的策略。

MeCP2由剂量敏感的MeCP2基因编码,是一种对正常脑功能至关重要的表观遗传调节因子。当它被破坏时,会导致两种罕见的儿童X连锁神经发育障碍。MECP2基因的功能缺失突变导致Rett综合征,而含有MECP2的染色体位点Xq28的重复或三倍复制导致MECP2重复综合征(MDS),这表明正确的MECP2水平在脑功能中的重要性。
MDS是男性最常见的由亚端粒基因组重排引起的疾病之一,约占所有X连锁智力低下病例的1%,显示出完全外显率。MDS的主要特征包括婴儿性张力低下、智力残疾、焦虑、运动功能障碍、癫痫和反复呼吸道感染。大约一半的感染者活不过25岁,通常死于呼吸道感染。迄今为止,全球已报道了600多例MDS,并表现出类似的临床病理。
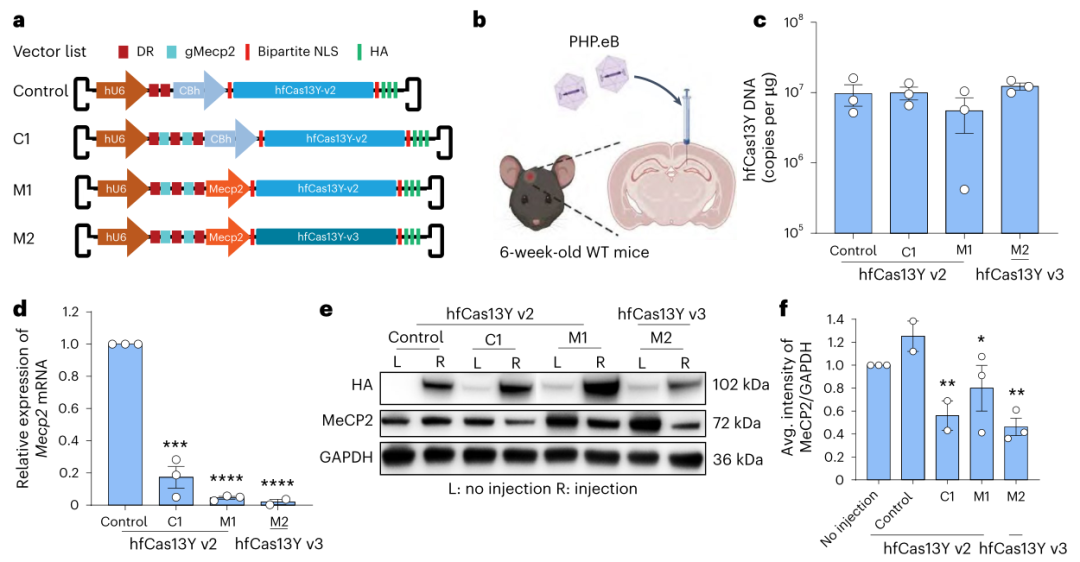
AAV-hfCas13Y RNA编辑系统介导的MECP2体内敲除效率(图源自Nature Neuroscience )
由于MeCP2的剂量对MeCP2的正常功能至关重要,因此有效的治疗策略需要精确的药物剂量来精细地控制MeCP2的水平。反义寡核苷酸(ASO)和CRISPR-Cas9治疗方法在人源化MDS小鼠模型中已有报道。然而,ASO治疗需要反复给药,这可能给患者带来负担。CRISPR DNA编辑通常会破坏MECP2,导致MECP2表达水平极低和MECP2功能丧失,从而导致Rett综合征。最近报道了一种微型CRISPR-Cas13系统,该系统可以选择性地与靶基因的转录物杂交,通过靶向降解RNA转录物实现有效沉默。与CRISPR-Cas9 DNA编辑工具不同,CRISPR-Cas13的效果不会永久改变基因靶标的编码序列,从而提供了有效控制剂量的机会。
在这项研究中,研究人员们设计了一个小尺寸的hfCas13Y变体。研究人员将其打包成一个AAV(AAV-PHP)。在MDS小鼠和非人灵长类动物(NHPs)中,利用靶向MECP2的引导RNA (gRNAs)抑制MECP2全脑递送后的水平,从而导致靶向MECP2信使RNA的选择性沉默,具有高效率和低脱靶效应。作为功能指标,通过单次双侧脑室内(ICV)注射携带hfCas13Y-gMECP2的AAV载体,MECP2转基因(MECP2 TG)小鼠模型表现出的异常行为缺陷在持续敲低致病性MECP2转录本后得到明显恢复。该研究结果证明hfCas13Y作为治疗MDS和其他基因剂量敏感疾病的治疗干预的潜力。
该研究由辉大基因/中国科学院上海药物研究所杨辉团队及临港实验室胥春龙团队共同完成,杨辉研究员、胥春龙研究员、辉大基因施霖宇博士、姚璇博士为本文的共同通讯作者,辉大基因研发中心杨栋博士、吴晓晴、段梦思、中科院上海药物所博士后姚依楠博士为本文的共同第一作者。
参考消息:
https://www.nature.com/articles/s41593-024-01838-6


