北京中医药大学揭秘黄芪甲苷III激活RXRa机制,心力衰竭治疗迎来曙光!
时间:2024-12-13 17:00:16 热度:37.1℃ 作者:网络
心肌梗死引发的心力衰竭(HF)是全球范围内导致死亡和残疾的主要因素。研究揭示,HF的病理特征之一是线粒体能量产生的功能障碍。因此,针对能量产生途径的药物靶向策略展现出巨大的潜力。类视黄素X受体α(RXRα)是一种配体激活型转录因子,能够形成同型或异型二聚体,并促进底物利用及氧化磷酸化相关基因的转录激活。然而,目前尚缺乏能够高亲和力特异性激活RXRα同型二聚体的激动剂。因此,开发针对RXRα同型二聚体的选择性激动剂,作为心脏保护剂,已成为一项迫切需求。
黄芪甲苷作为黄芪中的主要活性成分,多项研究已证实其能够改善线粒体功能。特别是黄芪甲苷Ⅳ,已被观察到在腹膜纤维化过程中对RXRa具有调节作用,这表明黄芪甲苷家族的化合物具备激活RXRa和改善线粒体功能的潜能。基于此,研究推测黄芪甲苷可能作为RXRa同型二聚体的潜在激活剂。
日前,一篇题为“Activation of RXRa exerts cardioprotection through transcriptional upregulation of Ndufs4 in heart failure”的文章深入探讨了黄芪甲苷III(AS-III),该物质作为一种直接作用于RXRa的激动剂,在HF治疗领域显示出显著的心肌保护效果。

图1 论文首页
AS-Ⅲ靶向RXRα,保护线粒体功能,发挥心脏保护作用
该研究利用分子对接、表面等离子共振(SPR)以及微尺度热泳(MST)技术,鉴定出AS-III为黄芪甲苷家族中具有最高亲和力的化合物。SPR和MST的实验结果揭示了AS-III与RXRα的特异性结合,其解离常数(KD值)分别为3.05×10^-7 mol/L(图2a)和1.35×10^-7 mol/L(图2b),这表明AS-III对RXRα具有显著的高亲和力。结合预测分析进一步显示,AS-III已成功地对接至RXRα二聚体的界面(图2c)。
通过均方根偏差(RMSD)模拟,研究了AS-III与RXRα蛋白的相互作用,模拟结果表明在20纳秒后,两者达到稳定构象(图2d)。接下来,研究探讨了AS-III是否能够诱导RXRα的转录活性。鉴于Ccl6受RXRα同二聚体的转录调节,研究采用了Ccl6启动子荧光素酶报告基因进行报告基因测定。通过RXRα siRNA逆转了oxygen-glucose剥夺/恢复(OGD/R)损伤中AS-III依赖性的保护作用,从而证明RXRα是AS-III的重要治疗靶点(图2e)。
随后,研究通过超声心动图评估了LAD结扎诱导的体内HF小鼠的心功能。与假手术组相比,模型组显示出严重的心功能障碍,表现为功能性缩短(FS)和射血分数(EF)显著下降。心功能的其他指标和HF的直接指标也得到了评估。与模型组相比,不同剂量的AS-III显著增加了EF和FS,与辛伐他汀具有相似的疗效(图2f,g)。低剂量和高剂量的AS-III均展现出相当的心脏保护作用,因此,后续实验选择了低剂量的AS-III。
研究还使用透射电子显微镜(TEM)和高效液相色谱(HPLC)检查了心肌组织中的线粒体结构和功能。LAD结扎心脏中的线粒体出现肿胀,脊消失(图2h)。AS-III部分减轻了线粒体损伤。HPLC结果显示,模型组的ATP和ADP浓度显著低于假手术组。尽管如此,AS-III提高了ATP浓度(图2i),表明它促进了HF小鼠中ATP的产生。此外,蛋白质印迹显示AS-III抑制了小鼠HF模型中RXRα的下调(图2j)。RNA测序分析结合qPCR验证证实了AS-III治疗上调了模型组中严重受损的线粒体复合体亚基(Ndufs1-6和8)(图2k,l)。
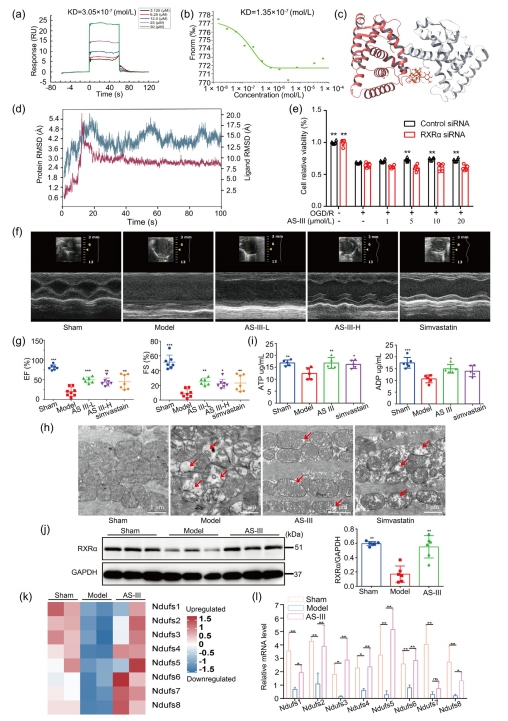
图2 AS-III靶向RXRa保护线粒体功能作用
RXRα以其同二聚体方式调控Ndufs4转录,AS-Ⅲ通过上调心脏中Ndufs4的表达促进线粒体功能
基于现有文献和先前的实验结果,研究推测RXRa通过Ndufs调控线粒体复合体I,利用HUMAN TFDB网站和Cytoscape软件确定Ndufs1-8为RXRa的直接转录靶基因。随后,通过qPCR验证了RXRa与Ndufs1-8之间的关系,结果表明RXRa siRNA下调了Ndufs2、Ndufs4、Ndufs6和Ndufs8的表达(图3a),而RXRa过表达则上调了Ndufs4的表达(图3b)。
Western blot结果显示,RXRa敲低显著降低了Ndufs4的水平,而RXRa过表达则上调了Ndufs4的水平。CUT和Tagseq分析用于确定RXRa和nduf4之间的调控关系,在Ndufs4基因中鉴定出RXRa结合序列(图3c)。此外,采用ChIP-qPCR方法证实了RXRa与Ndufs4的互作。双荧光素酶报告基因实验发现RXRa激活了ndufs4驱动的荧光素酶基因表达。然而,在突变的Ndufs4荧光素酶活性中未观察到这种差异(图3d)。这些结果支持RXRa直接靶向Ndufs4从而促进其转录的观点。
qPCR结果显示,在转染RXRa质粒的H9c2细胞中,9-cis RA(RXRa泛激动剂)能诱导Ndufs4表达,而LG100754(PPAR/RXR的激动剂,但为RXR同型二聚体的拮抗剂)不能诱导Ndufs4表达,且LG100754和9-cis RA共处理未能上调Ndufs4的表达,这表明RXRa以其同二聚体形式调控Ndufs4的转录(图3e)。
进一步研究发现,已知与RXRa同型二聚体结合的rxre -荧光素酶报告基因表明AS-III通过激活RXRa同型二聚体发挥作用。与分子对接结果一致,AS-III可以诱导RXRa同型二聚体的转录激活(图3f)。此外,AS-III上调了Ndufs4 mRNA的表达,RXRa siRNA显著减弱了Ndufs4 mRNA的表达(图3g)。还有,AS-III改善了OGD/R损伤的线粒体结构和功能,在LAD模型中发现AS-III通过rxra - ndufs4介导的线粒体功能发挥心脏保护作用(图3h,i)。
Western blot结果亦显示AS-III处理强烈诱导Ndufs4表达,然而这种效应在AAV-RXRa KD小鼠中被破坏(图3j)。AAV-RXRa KD+LAD结扎组,AS-III对线粒体的保护作用减弱(图3K)。
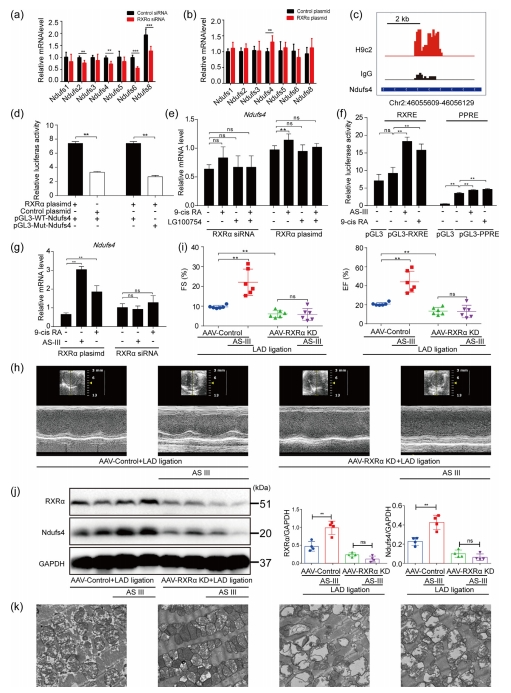
图3 AS-III在心脏中通过激活RXRa上调Ndufs4的表达促进线粒体功能
结论
总之,AS-Ⅲ是一种理想的直接靶向RXRα的激动剂,该化合物通过激活RXRα同源二聚体,进而上调Ndufs4的转录,从而改善线粒体损伤和心功能障碍。该研究为HF治疗提供了一种新的潜在药物,并揭示了通过反式激活RXRα同源二聚体上调Ndufs4并促进能量代谢途径,作为一种HF治疗新策略的可能性。
参考文献:
Shao M, Li L, Ma L, Song C, Li W, Zhang Y, Cheng W, Chen Y, Yang Y, Wang Q, Li C, Wang Q, Wang W, Wang Y. Activation of RXRα exerts cardioprotection through transcriptional upregulation of Ndufs4 in heart failure. Sci Bull (Beijing). 2024 May 15;69(9):1202-1207. doi: 10.1016/j.scib.2024.01.031


