【JNCCN】慢性期慢性髓性白血病调整给药剂量的管理建议
时间:2024-12-12 20:01:14 热度:37.1℃ 作者:网络
随着 BCR::ABL1 靶向酪氨酸激酶抑制剂(TKI)的问世,大多数慢性期慢性髓性白血病(CP-CML)患者的预后良好,预期寿命与同龄人相似。目前 CML 的治疗手段包括一代TKI伊马替尼;二代TKI 达沙替尼、尼洛替尼、博舒替尼(bosutinib)、氟马替尼(中国)和radotinib(韩国);三代TKI 泊那替尼ponatinib)、奥雷巴替尼(中国);变构抑制剂阿思尼布。
TKI治疗中出现的不良事件(TEAE)会损害生活质量,许多患者长期受低水平慢性不良事件的影响,对某些患者来说,这些不良事件不仅影响情绪健康,还影响社交和工作功能。
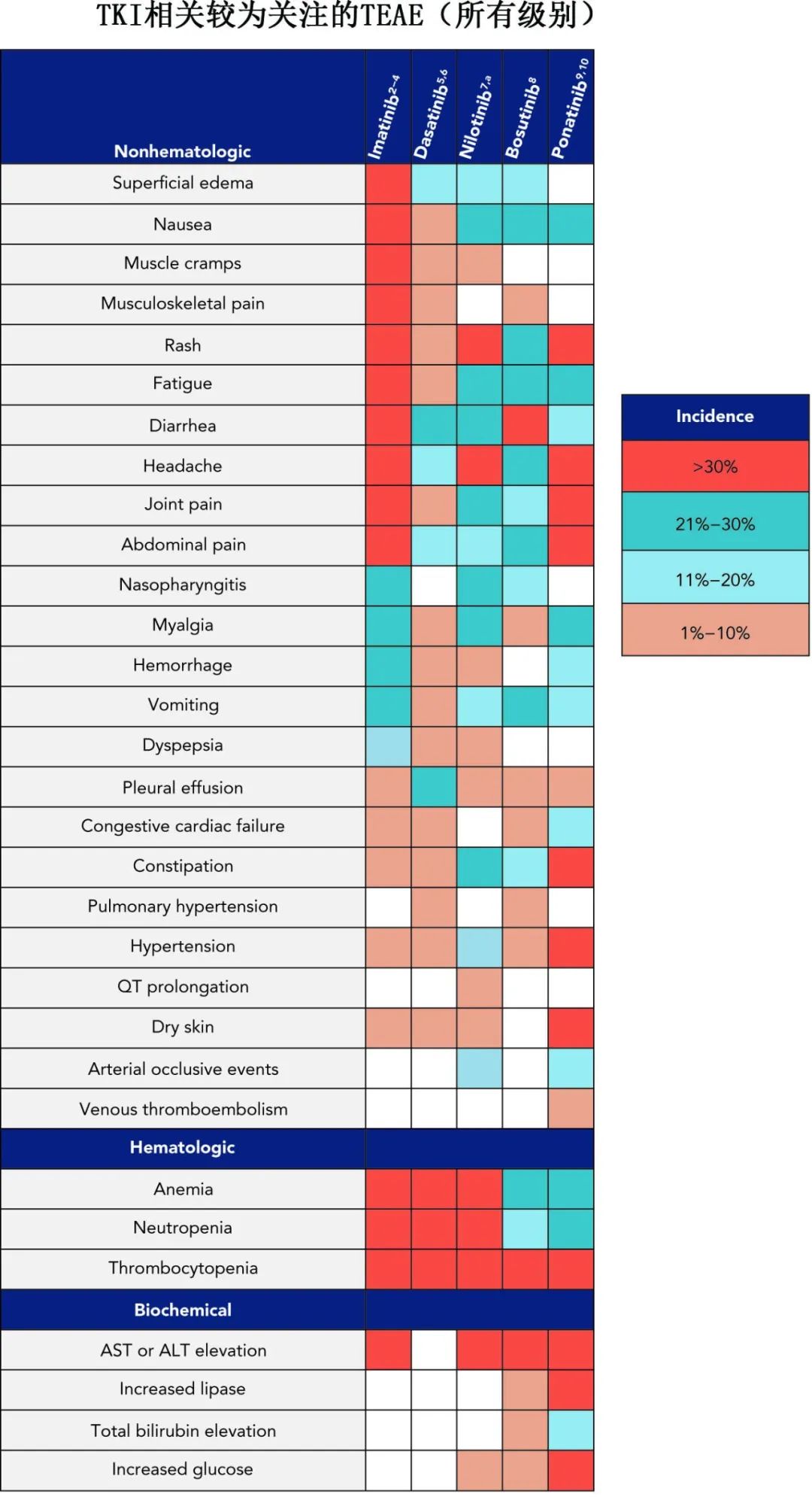
越来越多的数据表明,许多 TEAE 与治疗剂量相关,减少剂量可改善。然而减少剂量不应改变当前的预后,尤其是对于丧失反应或转变为急性白血病的高风险患者。包括NCCN在内的组织已经开始探讨 CP-CML 患者何时可以考虑减少剂量。
NCCN的官方杂志《Journal of the National Comprehensive Cancer Network》近日发表文章,回顾了报告患者剂量减少后结局的回顾性和前瞻性数据,并回顾了支持在一线和后续治疗中降低初始剂量的数据,还提出调整剂量的路径图。

对于接受推荐剂量的TKI,何时可减少剂量?
NCCN、ELN及处方信息均为特定TEAE下的降低剂量提供了指导,然而慢性 TEAE可能会影响生活质量。在美国“Life After Stopping TKIs”研究中,处于无治疗缓解(TFR)的患者报告疲劳、抑郁、腹泻、睡眠障碍和社会功能有所改善,但重新开始使用TKI后情况恶化。因此如果无法停用,一个重要的临床问题在于,在无需重新升级的情况下减量是否会损害预后。
伊马替尼
CP-CML患者推荐的伊马替尼剂量为每日 400mg,常见TEAE包括疲劳、恶心、腹泻、肌肉痉挛、体液潴留、转氨酶升高和皮疹。日本成人白血病研究组(JALSG)的 II 期 CML202 研究比较每日 400 mg和每日 300mg,总体生存率(OS)和无事件生存率(EFS)无差异。然而,减量至每日<300mg与较差的缓解率和生存结局相关。
相比之下,对于分子学反应更深的患者,如 MR4(BCR::ABL1≤0.01% IS)或 MR4.5(BCR::ABL1 ≤0.003% IS),规模较小的回顾性研究支持减量或间歇性服用伊马替尼是可行的,并且总体上是安全的。一项针对 43 例主要为低危或中危患者,在将剂量减至每日 300mg后检查结果。在剂量减量前,MR4 的中位持续时间为 4.1 年(2.2-5.9 年)。在 36 个月时,30 例(69.8%)患者处于 MR5(BCR::ABL1 ≤0.001% IS),9 例(20.9%)处于 MR4.5,3 例(7.0%)处于 MR4,1 例(2.3%)处于主要分子学反应(MMR;BCR::ABL1≤0.1% IS)。62.2%的TEAE较基线有所改善,几乎所有报告的患者症状均完全缓解。在伊马替尼相关的贫血患者中,13 例患者中有 12例的红细胞指标有所改善。
DESTINY 研究提供了前瞻性数据,表明在达到MMR或深度分子学反应(MR4)的患者中,TKI减量后仍可保持持久反应。这项多中心、II 期队列研究纳入 174 例CP-CML患者,主要接受伊马替尼治疗(n=148),但也包括接受达沙替尼(n=10)或尼洛替尼(n=16)。纳入标准包括接受 TKI 治疗≥3 年,且稳定保持 MMR 或 MR4 ≥12 个月。在 MMR 组和 MR4 组,TKI 使用的中位持续时间分别为 7.7 年和 6.5 年。伊马替尼剂量减至200mg每日一次;达沙替尼减至50 mg每日一次;尼洛替尼减至200mg每日两次,并持续 12 个月。主要终点为能够首先降阶治疗 12 个月,然后在接下来的 2 年中不丧失 MMR 的患者比例。在中期分析中,MR4 组患者在减量后的反应持久性优于 MMR 组,分别仅有 3例(2.48%)和 9 例(18.75%)患者丧失MMR(P=0.0007)。减量后的最初 3 个月内,包括嗜睡、腹泻、皮疹、恶心、眶周水肿和头发稀疏在内的TEAE有所改善。所有分子学复发患者在恢复全剂量TK后重新达到MMR或更深层次的分子学反应。在 MR4 组,减量并未影响患者成功停用 TKI。
另一种减量的方案为间歇性给药。INTERIM 多中心、II 期前瞻性研究纳入 76 例老年CML患者(年龄>65 岁),患者接受一线伊马替尼治疗 2 年,且达到稳定的完全细胞遗传学反应(CCyR;大致等同于 BCR::ABL1 # 1%)。大多数(81%)患者每日服用 400mg伊马替尼。间歇性给药方案为:在第 1 至 4 周,每周给药 1 周/停药 1 周;在第 5 至 12 周,每周给药 2 周/停药 2 周;在第 13 周及之后,每月给药 1 个月/停药 1 个月。共有 13 例(17%)患者丧失 CCyR 和 MMR,但除 1 例患者外,其余患者在恢复持续给药后,分别在中位时间 7 个月和 6 个月时恢复CCyR 和 MMR。在“给药”月份,未报告新发或恶化的TEAE。20 例患者中有 11 例患者的 TEAE 得到缓解。一项正在进行的纳入年龄>60 岁患者的 III 期研究OPTkIMA 正在评估 INTERIM 方案(“固定”)与渐进性间歇性给药(随后的几年中停药时间更长)在接受伊马替尼、达沙替尼和尼洛替尼的患者中的效果。
达沙替尼
CP-CML患者使用达沙替尼的推荐剂量为每日 100mg,常见TEAE包括胃肠道副作用、胸腔积液和皮疹,心包积液和肺动脉高压很少见,胸腔积液的发生率随剂量和年龄的增加而增加。在达沙替尼一线治疗的 III 期 DASISION 研究中,接受治疗的患者中有 28%在 5 年内出现胸腔积液;而在关于达沙替尼后续治疗的 CA180-034/剂量优化研究中,接受每日100mg治疗的患者中有 28%在7 年内出现胸腔积液。该毒性的发生率再加上减量后疗效的报告,促使人们研究抢先给予更低剂量。DESTINY 研究的数据支持对有深度反应(MMR 或更深)的患者减量,正在进行的 OPTkIMA 研究也在研究接受达沙替尼治疗的患者间歇性给药。
尼洛替尼
新诊断CP-CML患者推荐的尼洛替尼剂量为每日两次,每次 300mg;对于耐药或不耐受的 CP-CML 患者,剂量为每日两次,每次 400mg。TEAE包括皮疹、高血糖、高胆红素血症、高脂血症和 QT 延长,尼洛替尼还与动脉阻塞事件(AOE)风险增加有关,包括心血管、脑血管和外周动脉事件。在回顾性审查中,10%至 25%的患者出现此类事件,且风险会随着时间的推移而持续。在一项一线随机 III 期 ENESTnd 研究的 5 年和 10 年随访中,接受每日两次 300mg尼洛替尼的患者中有 7.5%和 16.5%报告AOE;接受每日两次 400mg尼洛替尼的患者中有 13.4%和 23.5%报告 AOE;接受伊马替尼的患者中有 2.1%和 3.6%报告AOE。以摘要形式发表的 NILO-RED 观察性研究报告了 81 例患者MMR、MR4 或 MR4.5 时减量后的结果。经过中位 29 个月的全剂量治疗,分别有 13.4%、25.4%和 61.2%的患者达到 MMR、MR4 或 MR4.5;大多数患者(86.6%)的剂量减至每日 450mg,10.4%减至每日 40mg,3%减至每日 300mg。中位剂量减量持续时间为 24 个月(5-54 个月),末次随访时分别有 6.3%、16.4%和 77.6%的患者处于MMR、MR4或 MR4.5。有两例患者在减量期间失去主要分子学反应,但在未干预的情况下恢复更深的分子学反应。
Bosutinib
推荐的Bosutinib剂量为:新诊断CP-CML患者每日 400mg,后线治疗中每日 500 mg。胃肠道毒性极为常见(80%的患者),且与剂量相关。在一线随机 III 期 BFORE 研究中,30.6%的患者将Bosutinib剂量减至300mg,剂量减低后45.1%的患者实现MMR,17.1%维持MMR 超过 6 个月。TEAE减少>10%,包括腹泻、血小板减少症、恶心、呕吐和贫血。Bosutinib后线治疗的 I/II 期研究的回顾性审查,也报告了Bosutinib二线治疗(CP2L)的患者中284例从每日500mg减低,119例接受Bosutinib三线或后线治疗(CP3L)的患者减低剂量。对于 CP2L 患者,83例(29.2%)减至每日 400mg,50例(17.6%)减至每日 300mg;42例(51%)在减至每日 40mg后实现或维持CCyR,23例(46%)在减至每日 300mg后实现或维持CCyR。对于 CP3L 患者,33例(27.7%)减至每日 400 mg,22例(18.5%)减至每日 300 mg;8例(24%)在减至每日 400mg后实现或维持CCyR,7例(32%)减至每日 300mg后实现了或维持CCyR。在所有队列中可评估的患者中,在 400mg和 300mg剂量减量队列中分别有33%和24%实现或维持MMR。值得注意的是,对于在Bosutinib减量前已实现CCyR或MMR的患者,仅有 2% CP2L 患者丧失反应,无 CP3L 患者丧失反应。在整个患者队列中,剂量减少与腹泻(400mg时减少33%,300mg时减少54%)、恶心(400mg时减少26%,300mg时减少29%)和呕吐(400mg时减少9%,300mg时减少23%)的显著减少有关;血液学毒性方面未观察到改善。
Ponatinib
Ponatinib为三代TKI,适用于后续治疗方案以及 T315I 突变的CML患者,其黑框警告包括急性肾盂肾炎、静脉血栓栓塞事件、心力衰竭和肝毒性,TEAE还包括胰腺炎、高血压、神经病变、体液潴留和伤口愈合受损。在 II 期 PACE 研究中报告了AOE的高发生率;然而其他分析表明,Ponatinib剂量较低时急性肾盂肾炎的风险较低。这些观察结果促成了随后的剂量探索性 II 期研究 OPTIC。OPTIC 评估了 3 个Ponatinib剂量组,这些患者对二代 TKI 不耐受或耐药,或存在 T315I 突变:每日 45mg(A 组)、每日 30 mg(B 组)和每日 15mg(C 组)。在 A 组和 B 组中,当 BCR::ABL1 达到≤1% IS 时,剂量降至每日 15mg。在 A 组、B 组和 C 组中,分别有 52%、36%和 25%的患者在 12 个月时实现BCR::ABL1 ≤1% IS。对于 T315I 突变患者,疗效与起始剂量密切相关,在 12 个月时,A 组 60%、B 组 25%和C组11%的患者实现 BCR::ABL1 ≤1% IS。在将减量至每日 15mg后(中位随访 32 个月),从45mg或 30mg减量的患者中分别有73%和79%维持反应。治疗中出现的 AOE 与剂量相关,A组最高,为9.6%,B组为 5.3%,C组为3.2%。最近的一项分析估计,根据反应调整剂量可将 AOE 的风险降低约 60%。
何时可考虑低剂量初始给药?
从低剂量开始治疗并根据反应情况增加剂量是一种颇具吸引力的策略;然而令人担忧的是,使用这种方法可能会遗漏实现最佳反应的能力,从而影响治疗结局。正是这些担忧导致了一种更谨慎的剂量调整方法,且与NCCN和ELN的处方信息有所不同。随访时间更长的新兴前瞻性和回顾性数据支持低剂量治疗能取得成功,不过对于高危CP-CML患者仍需谨慎。
达沙替尼
低剂量达沙替尼(50mg和70mg)的回顾性研究支持其疗效和改善耐受性。支持一线治疗中每日50mg剂量的前瞻性数据来自一项纳入81例CP-CML的美国单臂研究,目前中位随访5 年。在 3 个月时,几乎所有患者(96%)的 BCR::ABL1 转录本减少至≤10% IS,包括77%的转录本≤1% IS。12 个月时CCyR 的累积发生率为94%,MMR为79%,MR4为52%,MR4.5为43%,60 个月时分别提高到 98%、95%、83%和 82%。该研究的患者主要是低危 CP-CML 患者(65%为低危,29%为中危,Sokal评分)。为了将这些结果与历史队列进行比较而进行了倾向评分分析,在匹配基线特征后,12月时低剂量组和标准剂量组CCyR(分别为 97% vs 91%;P=0.17)和 MMR(81% vs 74%;P=0.44)相似,无进展生存期(EFS)或总生存期(OS)也无差异。标准剂量组相对于低剂量组TEAE更为常见,胸腔积液发生率分别为 21%和 5%(P<0.02)。
最近一项纳入日本老年患者的单臂前瞻性多中心研究检验了一种极低剂量的方案。DAVLEC 研究纳入 52 例新诊断CP-CML患者(年龄70 岁;中位77.5 岁),患者最初每日服用20mg达沙替尼,并根据治疗反应和耐受性在 3、6 和 9 个月时增加剂量。在 12 个月时,60%(31/52)的患者实现MMR,其中包括 23例(44%)仍每日服用 20mg剂量的患者;此外,分别有27%和 14%的患者实现MR4 和 MR4.5。目前尚不清楚这种极低剂量的方案在其他种族/民族中是否同样有效,但该研究强调了在多样化患者群体中进行谨慎研究的重要性。
尼洛替尼
目前尚无前瞻性研究评估新诊断CP-CML患者在接受尼洛替尼治疗时一线较低初始剂量,但有几项回顾性综述评估了在后续治疗中减少尼洛替尼剂量的安全性。ENESTswift 单臂研究评估了 20例患者因不耐受而非耐药而改用尼洛替尼,患者最初每日两次服用300mg尼洛替尼。在 24 个月内的任何时间点,50%的患者达到MR4.5。对于对先前治疗不耐受但非耐药的患者,最初每日两次服用 300mg尼洛替尼可能是合适的。
Bosutinib
由于腹泻、恶心、呕吐的发生率较高,血清转氨酶水平升高,且低剂量使用时疗效显著,专家小组建议每日起始剂量为 200 至 300mg,并根据临床指征增加剂量。II 期 GIMEMA BEST纳入 63例(年龄>60 岁)患者,在二线治疗中开始使用减量Bosutinib。Bosutinib最初每日 200mg,持续 2 周,然后增加到每日300mg。3 个月后BCR::ABL1 转录本>1%的患者可进一步增加剂量;73%的患者仍维持每日300mg,6%的患者仍维持每日200mg。12 个月时MMR率为 59%,到36 个月时实现或维持MMR的概率为 78%、MR4 为 54%、MR4.5 为 46%;胃肠道毒性的发生率低于其他报告。另一项关于在二线或三线治疗中每日起始剂量为300mg Bosutinib且逐步增加剂量的前瞻性研究强调了高剂量Bosutinib的胃肠道毒性,40%的患者无法增加到推荐的每日 500mg剂量。尽管该研究提前终止,但总体疗效极佳,79%的患者实现MMR,中位每日剂量为 387mg。与其他报告不同的是,该研究并未报告逐步增加剂量能改善胃肠道毒性。
讨论
大多数CP-CML患者可实现预期寿命正常,因此减少剂量时最重要的担忧是影响该结果。然而影响健康相关生活质量的TEAE很常见,似乎与剂量相关。此外,特定的毒性(如胸腔积液和AOE)可能导致永久性器官损伤,也似乎与剂量有关。尽管TKI停药是最终目标,但大多数患者仍可多年接受治疗。对于具体患者的最佳起始剂量尚不清楚。理想情况下,需要对不同种族和民族群体的药代动力学进行更深入的了解,并确定反应和毒性的生物标志物。个性化给药的方法之一是治疗药物监测(TDM)。一项纳入新诊断CP-CML 患者的前瞻性研究评估了早期逐步减量(目标是达沙替尼谷浓度[Cmin] ≤3nmol/L),发现 TDM 组胸腔积液的发生率低于对照组,但分子学反应无差异。尽管此类方法很有吸引力,但尚未在临床上广泛应用。
回顾性和前瞻性数据进行总结,支持在特定情况下减少TKI的剂量。在没有持久MMR或深度分子学反应的情况下,伊马替尼每日<300mg剂量与更差的预后相关,因此对于这种效力较弱的 TKI,应谨慎给予每日<400mg的一线剂量。对于每日 50mg启动剂量的达沙替尼,一项前瞻性试点研究的长期随访表明其疗效相似,但胸腔积液发生率较低。需要注意的是,该研究中的大多数患者并非高危CP-CML,因此对于这些患者应谨慎。回顾性数据表明,标准剂量的达沙替尼在老年和亚洲人群中的毒性更高,而前瞻性 DAVLEC 研究为老年日本患者极低剂量达沙替尼提供了证据,不过该结果是否适用于其他种族或民族群体尚不清楚。对于尼洛替尼,在后续治疗中给予每日两次 300mg(而非每日两次 400mg)的起始剂量是合理的,尤其是如果由于不耐受而非耐药而更换治疗方案。对于bosutinib,专家小组建议起始剂量为每日 200 至 300mg,并根据临床指征增加剂量以限制过早停药。尽管部分患者的预后良好,但对于高危CP-CML患者仍需谨慎。有关诊断时存在的特定额外突变(如 ASXL1)的新数据表明,对于该人群应谨慎进行剂量调整,因为这些突变可能与较差的分子学反应和较差的无失败生存期相关。对于ponatinib,基于OPTIC研究,当 BCR::ABL1 ≤1% IS时,应考虑减量至每日15mg,以减轻AOE风险,同时不影响疗效。目前尚缺乏阿思尼布减量的数据。
对于较年轻患者、可耐受全剂量TKI的患者、强烈优先考虑TKI停药的患者以及高危CP-CML患者,开始使用全剂量可能是最佳策略。回顾性和前瞻性研究支持,对于这些患者,如果在达到MMR或更深层次的反应时减少剂量,在大多数情况下不会影响反应。DESTINY 研究主要是接受伊马替尼治疗的患者,减量50%后19%的 MMR 患者丧失 MMR,但MR4 患者中只有2%丧失。对于持续MR4或MR4.5的患者,在TKI停药前减量也是一种合理方案。伊马替尼减量的替代方案是间歇性给药,可为无治疗日提供了可能性。正在进行的 OPTkIMA 研究正在评估固定和渐进式减量策略,并将为其他 TKI 的间歇性给药提供更多见解。对于接受Bosutinib治疗的患者,最大的回顾性研究报告称,在后线治疗中服用Bosutinib的患者中,仅有2%在减量至每日 400mg或 30mg时丧失CCyR或MMR。对于接受尼洛替尼治疗的患者,NILO-RED 研究支持MMR或更深反应的患者将剂量减少至每日 450mg或 400mg。但又一个重要的未回答问题,即进一步的剂量减少是否会降低AOE。作者提出的方案概述见图 2 和图 3。
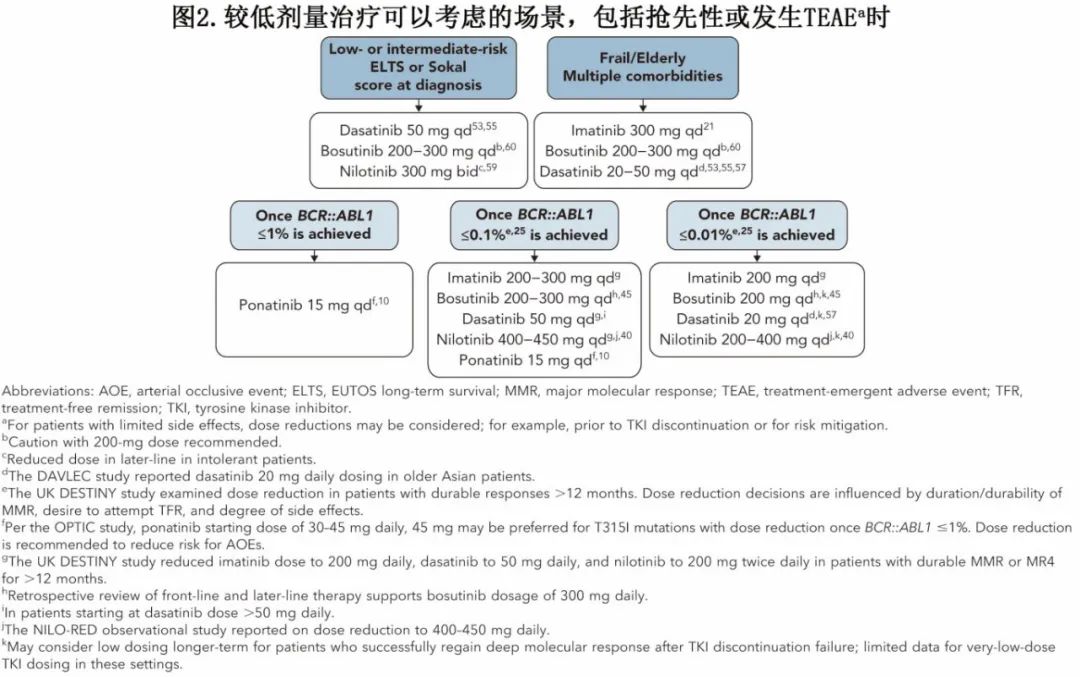
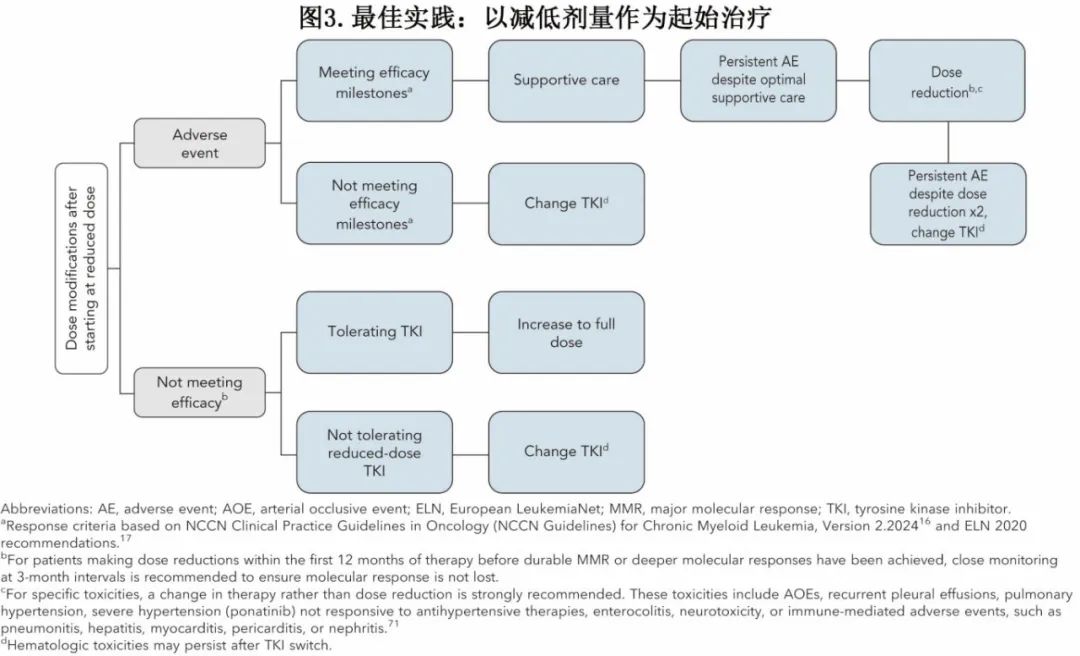
总体而言,减量似乎能降低TEAE的发生率,如伊马替尼或Bosutinib引起的胃肠道毒性、达沙替尼引起的胸腔积液发生率以及ponatinib引起的AOE。然而中重度血细胞减少症患者的管理仍存在问题,而且即使降低剂量下血细胞减少症仍会发生。此外,对于部分患者,在所有线治疗中都可能会出现一系列不耐受的情况。最后,对于特定的毒性,包括AOE、肺动脉高压和反复胸腔积液,建议更换治疗方案而非减量(图 3)。总之,在CML的治疗手段中, TKI减量是一个日益重要的考虑因素,并且在治疗方案转换之前就应该予以考虑。此外减量后密切监测至关重要,以确保正常预期寿命不受影响。
参考文献
Oehler VG, et al.Dose Modifications in the Management of Chronic Phase Chronic Myeloid Leukemia: Who, What, and When.J Natl Compr Canc Netw . 2024 Nov;22(9):e247044. doi: 10.6004/jnccn.2024.7044.


