中国医学科学院黄帆/南开大学史林启《Angew》: 机械免疫检查点抑制剂硬化肿瘤细胞增强抗肿瘤免疫反应
时间:2024-12-12 06:00:55 热度:37.1℃ 作者:网络
肿瘤通常会劫持某些免疫检查点,以逃避由细胞毒性淋巴细胞介导的免疫监视,包括自然杀伤(NK)细胞和细胞毒性效应T细胞。通过抗体阻断基于配体受体对的免疫检查点已被证明可以恢复和重新激活抗肿瘤免疫,从而取得显著的临床疗效。然而,对于对现有免疫检查点阻断(ICB)抗体无应答的患者,迫切需要寻找新的免疫检查点。最近的证据显示,癌症进展涉及细胞力学的显著变化,这揭示了机体的免疫监视行为具有一个被忽视的“机械维度”。例如,恶性肿瘤细胞通常比非恶性肿瘤细胞更加柔软,而且这种软化与肿瘤转化和恶性程度密切相关。这种密切的关联与淋巴细胞介导的攻击机制有关,该过程依赖于淋巴细胞通过免疫突触与靶细胞产生直接相互作用。在攻击过程中,这些淋巴细胞被激活,并向突触间隙分泌穿孔素或颗粒酶,从而诱导靶细胞凋亡。肿瘤细胞的软化会削弱淋巴细胞的活化,导致效应细胞因子的产生减少。因此,肿瘤细胞的硬度可被视为一种“机械免疫检查点”,诱导肿瘤细胞对淋巴细胞介导的细胞毒性产生抵抗。
研究表明,质膜中的胆固醇在决定细胞硬度方面起着重要作用。肿瘤细胞膜的胆固醇水平通常高于正常细胞,这使得肿瘤细胞更加柔软。甲基-β-环糊精 (MeβCD) 作为一种临床药物增溶剂,已被证明对胆固醇具有高亲和力。受此启发,中国医学科学院黄帆研究员与南开大学史林启教授团队提出了一种机械免疫检查点抑制剂 (Mechanical Immune Checkpoint Inhibitor, MICI) 策略。该策略可以靶向肿瘤细胞,并通过消耗肿瘤细胞膜中的胆固醇有效地增加细胞硬度,进而增强多种肿瘤模型中NK细胞和T细胞介导的抗肿瘤免疫反应。MICI是通过将合成的CD脂质整合至肿瘤细胞靶向膜融合脂质体中制备得到的。使用MICI可将CD脂质有效融合到肿瘤细胞膜中,随后CD脂质通过特异的主-客体相互作用捕获并消耗膜内的胆固醇,从而显著提高提高肿瘤细胞硬度,增强NK细胞和T细胞活化,使肿瘤细胞更容易受到淋巴细胞的攻击(图1)。研究结果表明,通过MICI硬化肿瘤细胞能够克服机械免疫检查点的抑制作用,显著提高了过继性NK细胞和T细胞免疫疗法的抗肿瘤效果。此外,MICI还可以提高免疫检查点阻断疗法对实体瘤的治疗效率。与直接使用商品化的MeβCD相比,MICI具有显著优势,因为游离的MeβCD必须以高剂量使用才能达到有效的膜胆固醇消耗,但是此操作同时也可能破坏淋巴细胞的脂质筏,干扰淋巴细胞的募集和趋化性,甚至影响T细胞受体的聚集和信号传导。考虑到膜融合脂质体在递送亲水性和疏水性药物方面的巨大潜力,该工作为开发具有临床转化潜力的联合抗肿瘤疗法提供了全新的策略。
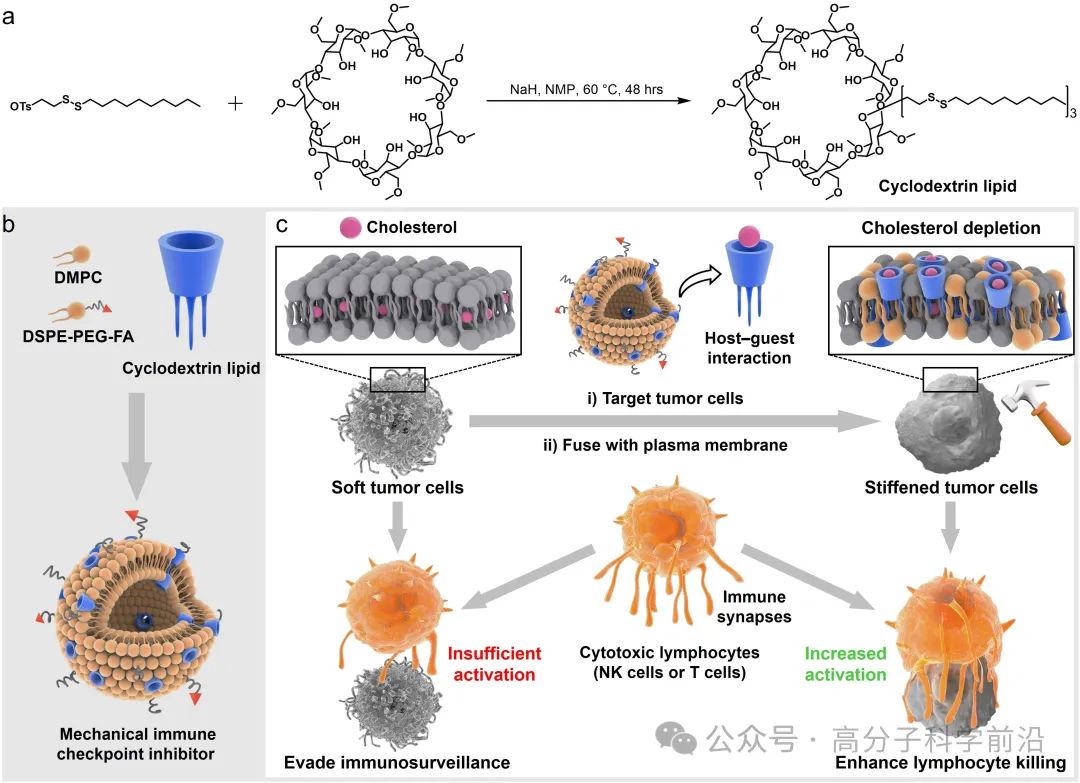
图1. 机械检查点抑制剂MICI硬化肿瘤细胞增强淋巴细胞抗肿瘤活性
该研究以“A Mechanical Immune Checkpoint Inhibitor Stiffens Tumor Cells to Potentiate Antitumor Immunity”为题在线发表在《Angewandte Chemie》上(DOI: 10.1002/anie.202417518)。中国医学科学院放射医学研究所黄帆研究员和南开大学史林启教授为本文的通讯作者,南开大学毕业生赵宇博士为本文的第一作者。该研究得到了国家自然科学基金,天津市自然科学基金重点项目,中国医学科学院医学与健康科技创新工程等项目的支持。
论文信息:
Yu Zhao, Xiaoxue Hou, Zeyu Wang, Shiyu Peng, Chunxiong Zheng, Qingqing Huang, Yufei Ma, Yuanfeng Li, Yong Liu, Yang Liu, Linqi Shi*, and Fan Huang*,A Mechanical Immune Checkpoint Inhibitor Stiffens Tumor Cells to Potentiate Antitumor Immunity
全文链接:
https://doi.org/10.1002/anie.202417518


