揭秘桥本脑病(hashimoto encephalopathy,HE)
时间:2024-12-06 12:01:24 热度:37.1℃ 作者:网络
论坛导读:自1966年Lord Brain等最初描述桥本脑病(hashimoto encephalopathy,HE)以来已经讨论和探索了50 多年,但甲状腺/大脑/免疫相互作用的所有方面仍然不是很清楚,HE 仍然是甲状腺学和神经精神疾病的神秘现象之一。HE 的发病机制可能包括各种自身抗体对 CNS 内靶细胞的直接作用,就像它发生在自身免疫性脑炎中一样,但也取决于间接联系,通过次级细胞因子产生和/或自身免疫的代谢作用和甲状腺变化介导。深入的探索也许可以成为防治中枢神经系统自身免疫缺陷的一个突破口。
1966年Lord Brain等报道了第1例与桥本甲状腺炎(hashimoto’s thyroditis,HT)相关的脑病,该患者甲状腺功能正常状态下出现神经精神异常的症状,同时伴有血清甲状腺抗体滴度的增高,并对糖皮质激素治疗有效。桥本脑病(hashimoto encephalopathy,HE)是一种与HT相关的自身免疫性脑病,伴有自身免疫性抗体增高,临床表现复杂多样,多表现为认知功能损伤,精神异常,昏迷,癫痫,肌痉挛等症状,同时对激素治疗有效。HE通常伴有甲状腺抗体TPO-Ab和TG-Ab滴度的升高,病程呈复发-缓解交替或缓慢进展性发展。HE患病率为2.1/10万,平均发病年龄为42岁,多发于女性,患病率女性和男性比例为4:1。
HE是一种与自身免疫性甲状腺炎相关的自身免疫性疾病,发病机制复杂,大多表现为脑病和甲状腺抗体的升高,尽管HE的发病机制与HT的关系尚不明确,但对于HE的发病机制,自1966年发现该疾病后,学者们提出了不同的可能:(1)自身免疫介导的中枢神经系统(CNS)血管炎;(2)血管源性水肿学说;(3)促甲状腺激素释放激素(TRH)在CNS促甲状腺激的毒性作用;(4)自身抗神经细胞抗体或α-烯醇化酶(NAE)抗体对甲状腺组织和CNS共有的抗原的自身免疫反应。
HE临床表现复杂,并且无特异性症状,易与朊蛋白病、癫痫持续状态、边缘性脑炎、急性播散性脑脊髓炎等疾病造成混淆,容易造成误诊、漏诊影响治疗。研究表明,最常见的症状为癫痈(52%)、意识混乱(43%)、肌阵挛(37%)、认知功能受损(36%)、波动性意识障碍(36%),这些症状常组合存在,亦可单独存在。亦有以延髓麻痹为首发症状的报道。
临床表现可分为两种:
(1)血管炎型且以中风样为发作特点,起病急,同时可能伴有意识模糊、认知障碍、癫痫等症状;
(2)伴有精神逐步恶化的渐进扩展型,初期病情隐匿,伴有严重记忆障碍、痴呆、焦虑、亢奋、淡漠、自闭等症状,意识可能逐渐或相当快速转化为嗜睡甚至昏迷,癫痫频繁发作,也会出现共济失调、震颤、肌痉挛等症状。
脑病通常在一周发生,通常表现为复发或缓解的过程,通常认知功能障碍,包括记内忆或语言功能障碍;癫痫发作包括局灶性痫病、全身性癫痫、复杂部分发作性痫病和症状性痫病。另外,率表现出明显的精神病性症状、情感障碍、行为异常等多种精神症状,极易误诊,值得精神科临床关注,尤其对急性、亚急性起病以及诊断不明确的患者,应及时完善甲状腺抗体检查,排除桥本脑病。
HE的诊断除依据病史及临床症状特点外,还需颅脑MRI、脑电图、甲状腺功能等实验室检查和对激素治疗有效等特点的支持。
1、脑电图:(慢波多见,特异性不高,但90%有异常)常提示为慢波背景,可星弥漫或局限性,常伴有高幅尖波,但痫样放电少见,弥漫性慢波或额叶慢波最常见。
2、抗体:(必须的条件,和疾病严重程度正相关)。几乎 100%伴有血清TPO-Ab(甲状腺过氧化物酶抗体)增高和或伴TG-Ab(甲状腺球蛋白抗体)增高。高滴度的抗甲状腺抗体可存在于5%-20%的正常人群中。滴度的高低与甲状腺功能水平及临床表现无明显相关,激素并不能使抗体滴度降低。CSF蛋白:80%是要增高的。对激素反应:98%有效,绝大多数1周见效。(急性期可以冲击;注意递减,病人是可以反复的;这个与ADEM很容易纠葛,后者单向病程的血管炎,抗原似乎来自外缘,而HE抗原来自本身,一定程度上注定有复发的可能)
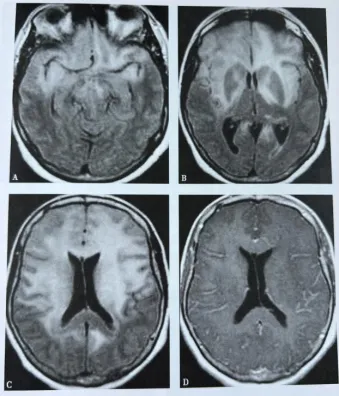
3.MRI:大部分HE患者MRI无特异性改变,有学者认为大约50%的HE患者MRI可有特异性改变,以脑萎缩改变最为常见,也可表现为皮层下白质的异常信号;部分HE患者颅脑MRI可以出现特异性改变,并且这种特异性改变大多是可逆的。
4.CSF:80%蛋白增高,对于伴有三联征(脑病、脑电图慢波改变和脑脊液蛋白升高)的患者,建议常规检测血清和脑脊液抗甲状腺抗体,而不管甲状腺激素水平是否异常。
Mocell等2007年诊断标准:HE应至少具备以下条件:
(1)表现为认知功能受损或神经精神症状的脑病;
(2)抗甲状腺抗体滴度显著升高;
(3)实验室及影像学检查可除外感染性、中毒性、代谢性、肿瘤性及副肿瘤性病因所致。此外,脑电图呈现弥漫性慢波、脑脊液中蛋白含量增高、颅脑MRI呈非特异性改变、对糖皮质激素治疗反应良好等现象均有助于诊断。不过,对激素治疗无反应并不能排除HE。
HE临床变异性大,应与病毒性脑炎、自身免疫介导的边缘叶脑炎(LE)相鉴别。以上诸病若累及颞叶时可出现不同程度的颞叶癫痫、人格改变、精神行为异常等临床特点。HE好发于中年女性,多有甲状腺功能异常,TPOAb异常是其特异性改变,激素疗效显著;病毒性脑炎多急性起病,有感染前驱史,脑脊液病毒学检测有助于诊断,抗病毒治疗有效;自身免疫介导的LE血清及脑脊液中的特异性抗体阳性有助于确定诊断。抗甲状腺过氧化物酶抗体(TPOAb)为86-100%,抗血清抗甲状腺球蛋白抗体(TGAb)为73%,促甲状腺素受体抗体(TRAb)也可升高为10-20%。没有证据表明甲状腺抗体在HE发病机制中的具有诊断性作用,但可能与自身免疫异常相关。HE常伴自身免疫疾病,如:重症肌无力、肾小球肾炎、系统性红斑狼疮、类风湿性关节炎、干燥综合征等,并且由于脑脊液的炎性表现,激素治疗有效等,可推测HE属于自身免疫疾病。
近年来自身免疫性脑炎(AE)的强势崛起给HE的存在与否带来了不小的冲击。同时随着自身免疫性脑炎中抗体重叠的现象得到深入的探究,已有新型自身免疫性脑炎伴甲状腺抗体升高的文献报道。有学者指出若将此类脑炎做出桥本脑病的诊断有可能延误对肿瘤的筛查,鉴于桥本脑病无明确的神经病理机制,且甲状腺抗体在健康者和有免疫背景人群中广泛存在,并不具有特异性,不建议对同时存在明确自身免疫脑炎抗体且甲状腺抗体升高的脑病患者诊断为桥本脑病。
HE呈急性或亚急性发作时,采用大剂量糖皮质激素的冲击疗法,可用泼尼松50~150mg/d口服,连用10~15d,或者静脉应用甲泼尼龙1g/d,连用3~7d后改口服泼尼松治疗,此后,根据治疗反应逐渐减至维持量,总疗程6个月至2年以防复发。对于反复发作、单用糖皮质激素无效或因副作用而无法常规应用的患者,可采用其他免疫疗法。对有甲减或癫痫发作的患者要相应给予甲状腺激素及抗癫痫药物治疗。
参考文献
Marta Waliszewska--Prosół ,Maria Ejma,Hashimoto Encephalopathy—Still More Questionsthan Answers,Cells,2022,11, 2873
Peschen-Rosin R,Sehabet M,Dichgans J.Manifestation of Hashimoto、s encephalopathy years before onset of thyroid disease.[J]Eur Neurol,1999,41(2):79-84.
李仕林, 常明则, 刘志勤,等. 以颞叶癫痫为主要表现的桥本脑病一例[J]. 中国神经免疫学和神经病学杂志, 2017, 24(1):69-70.
杜一平,范源,刘涛.桥本脑病的临床诊治研究进展[J].昆明医科大学学报,2020,41(02):1-6.
王东升,梅蕊. 桥本氏脑病临床及影像的动态演变1例报道.神经损伤与功能重建·2014,9(5):451-452.


