迷走神经刺激在心血管系统中的应用:解剖与原理
时间:2024-12-05 13:06:52 热度:37.1℃ 作者:网络
在现代医学研究中,迷走神经刺激(VNS)作为一种新兴的治疗手段,正逐渐展现出其在多种疾病治疗中的潜力。特别是在心血管系统疾病方面,VNS的研究成果令人瞩目。
今天,就让我们深入了解一下VNS的解剖基础和作用原理。
一、迷走神经的解剖结构
迷走神经是人体神经系统的重要组成部分,属于副交感神经系统。它起源于脑干,其纤维广泛分布于身体的多个器官。
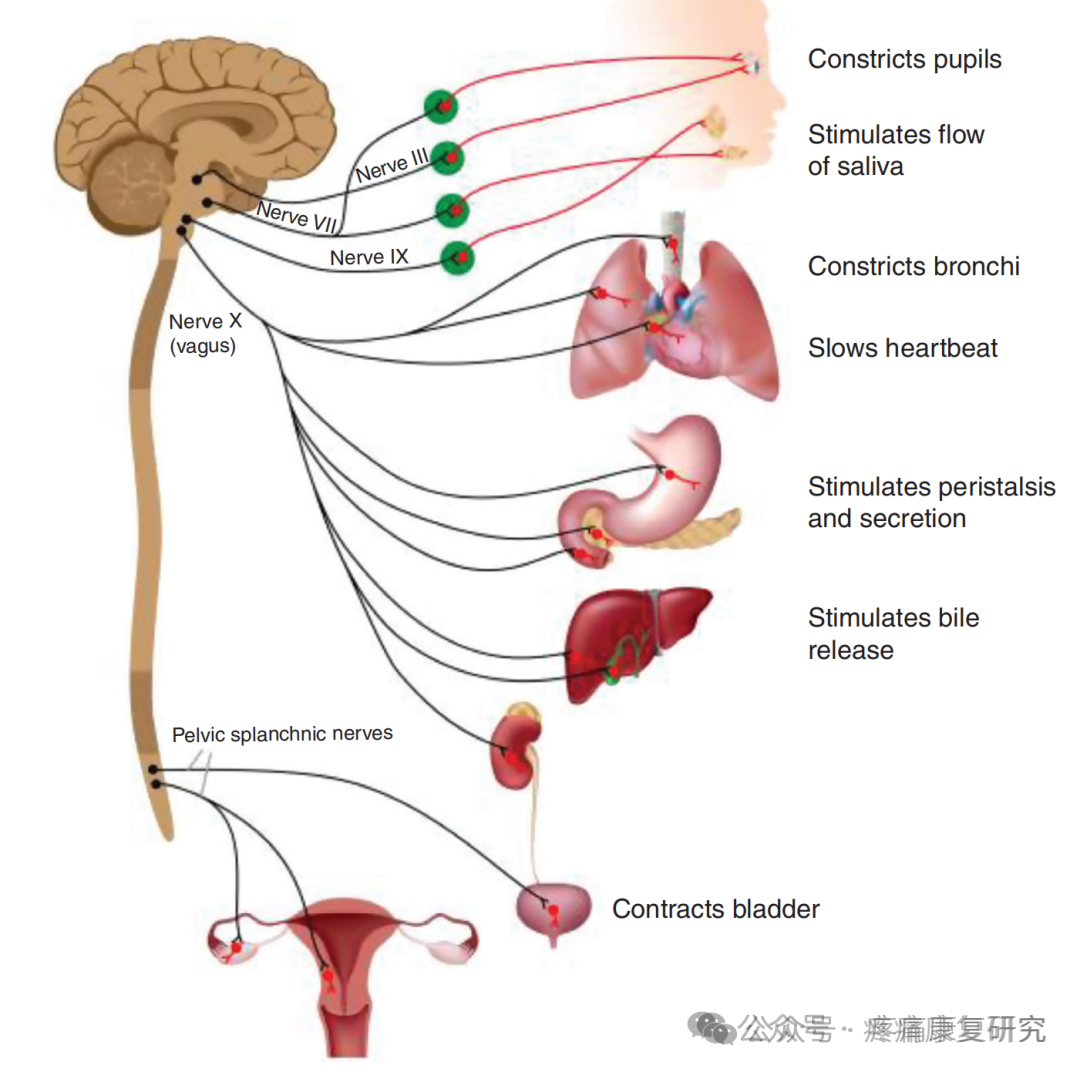
副交感自主神经系统(ANS)传出(运动)投射的示意图。
脑神经III、VII和IX支配瞳孔,导致瞳孔收缩,并支配唾液腺,使唾液流量增加。
盆内脏神经支配膀胱,其激活会导致膀胱收缩和排尿便利,支配下肠道,促进排便;它们还支配男性和女性性器官。副交感ANS的主要传出通道,即运动性迷走神经,起始于脑干中的两个核团中的细胞,即迷走神经背核和疑核。
这些细胞的轴突投射到各种器官,与位于这些器官处或非常靠近这些器官的副交感神经节中的神经节细胞形成突触。
来自神经节细胞的节后轴突支配肺部(促进支气管收缩)、心脏(减慢心率、降低心脏收缩力)、肺血管和体循环血管(血管舒张和降低血压)、胃(促进蠕动和胃液分泌)、肝脏和胰腺(复杂的代谢作用)、脾脏(节前轴突与脾神经相互作用,促进抗炎作用)以及肾脏(影响血管张力和滤过率)。
在心血管系统中,迷走神经的作用尤为关键。
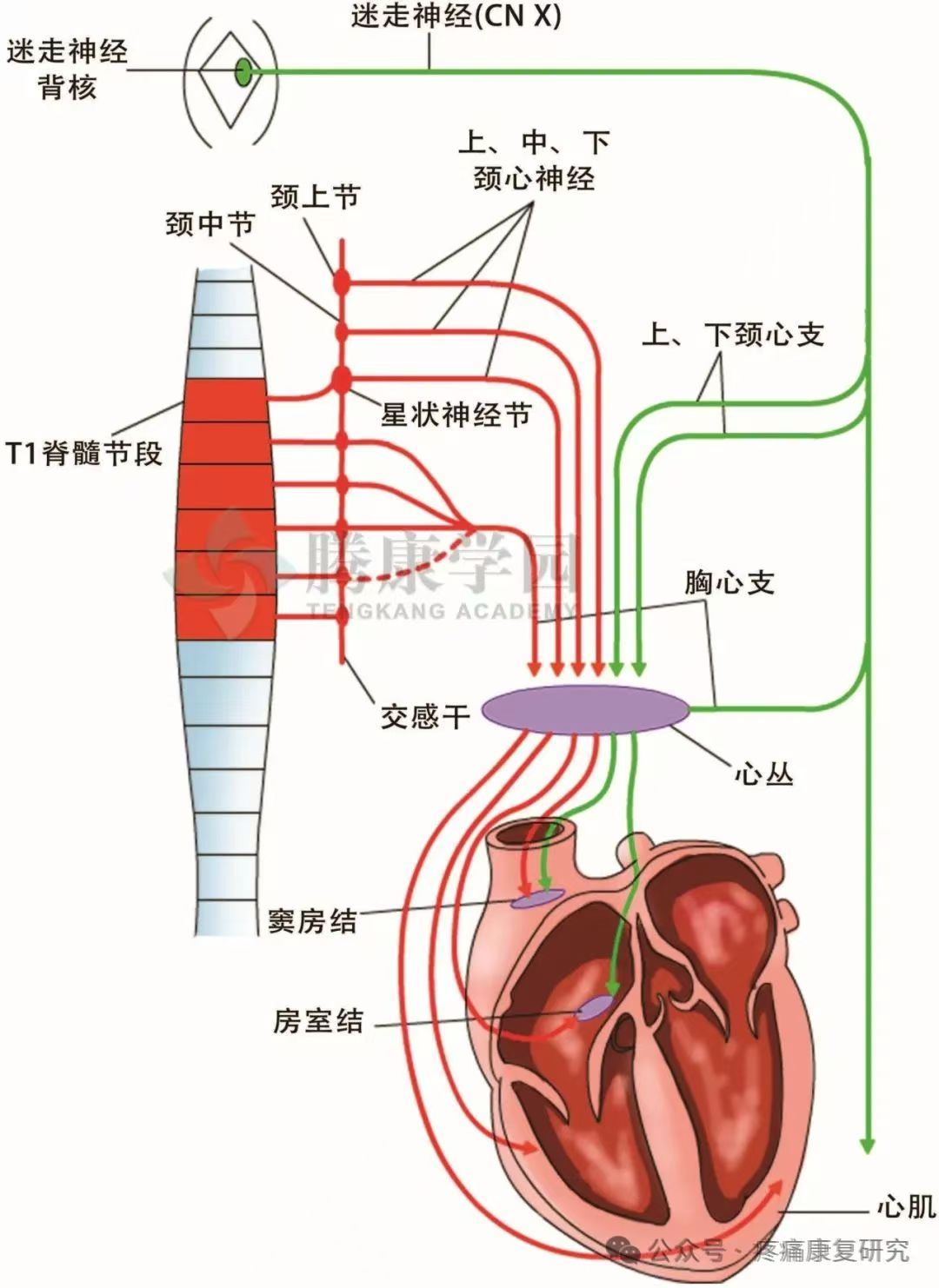
它的传出纤维支配着心脏的心肌细胞和传导系统,包括窦房结(SAN)、房室结(AVN)、心室心肌以及心室传导系统等。这些神经纤维通过释放神经递质,如乙酰胆碱,来调节心脏的生理活动。
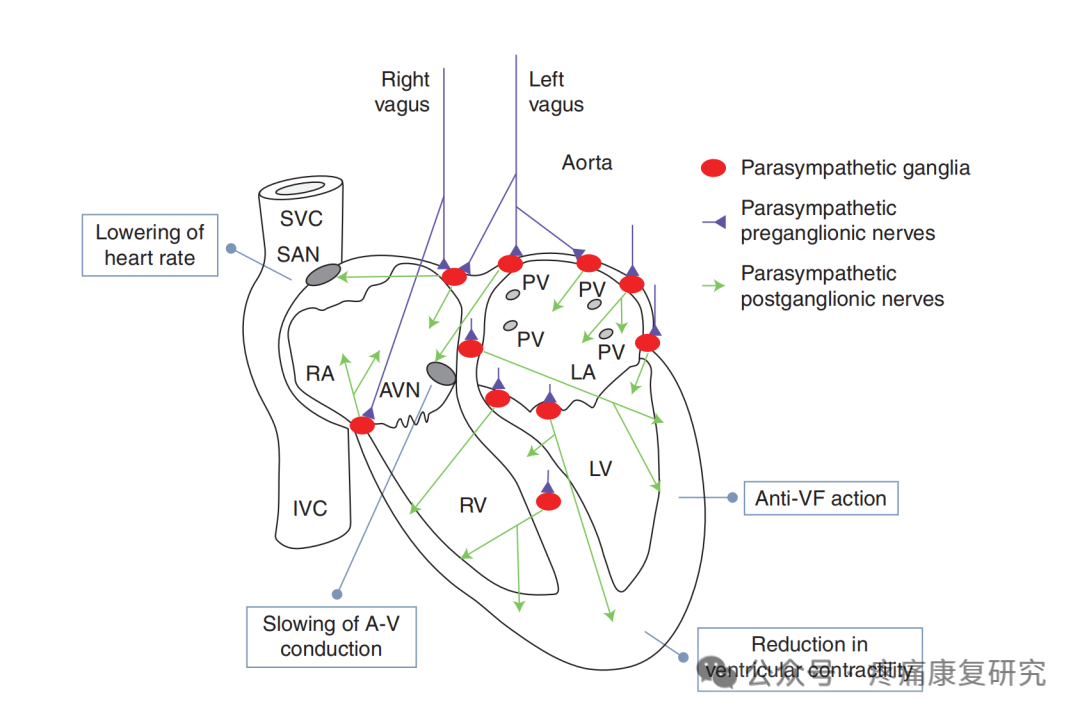
图:心脏中的迷走神经支配情况。
图中蓝色部分显示的是左右两条心脏迷走神经节前纤维。它们与位于心外膜以及心房和心室间隔处的若干副交感神经节(以红色显示)形成突触连接。
副交感神经节神经元发出节后轴突(以绿色显示),延伸至心脏的不同部位;这些轴突的解剖学分布有助于解释迷走神经在心脏中的生理作用。
具体如下:
窦房结(SAN):迷走神经激活会导致心率降低(负性变时作用);房室结(AVN):会使房室传导减慢(负性变传导作用);左右心室壁(RVs、LVs)及传导系统:会使心室收缩力降低(负性变力作用);还会提高诱发心室颤动(VF)的阈值。
SVC:上腔静脉;IVC:下腔静脉;RA/LA:右心房/左心房;PV:肺静脉。
二、VNS的发展历程
VNS的研究可以追溯到19世纪末,当时美国神经学家James Corning首次尝试将其用于治疗癫痫,但最初的尝试并不成功。
随着时间的推移,科学家们对VNS的研究不断深入。20世纪中叶,研究人员开始关注VNS对心脏功能的影响。
到了21世纪初,随着对炎症反射机制的深入理解,VNS的研究取得了重大突破,其在多种疾病治疗中的潜力也逐渐被揭示。
三、VNS在心血管疾病中的作用原理
1. 自主神经调节平衡
VNS主要通过调节自主神经系统的平衡来发挥作用。
自主神经系统包括交感神经和副交感神经,正常情况下两者相互制约,维持心脏的正常节律和功能。在心血管疾病中,这种平衡常常被打破。
例如,在心力衰竭时,交感神经过度激活,导致心脏负荷增加,心肌耗氧量上升,进一步加重心脏损伤。
VNS通过刺激迷走神经,增强副交感神经的活性,抑制交感神经的过度兴奋,从而改善心脏的神经调节失衡状态。
研究发现,VNS可以影响心脏的多个生理参数。如在动物实验中,刺激迷走神经可使心率减慢,这是因为迷走神经释放的乙酰胆碱作用于心脏的窦房结,降低其自律性,产生负性变时作用。
同时,VNS还能影响房室结的传导,减慢房室传导速度,防止过快的心房冲动传导至心室,起到负性变传导作用,从而减少心律失常的发生风险。
2.抗炎与抗凋亡机制
VNS具有显著的抗炎作用。炎症反应在心血管疾病的发生发展中起着关键作用,如在心肌梗死和心力衰竭等疾病中,炎症细胞因子的释放会导致心肌细胞损伤和心脏功能恶化。
VNS可以通过调节炎症反射来减轻炎症反应。具体而言,它作用于α7烟碱乙酰胆碱受体(α7nAchR),抑制促炎细胞因子如肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)等的释放。
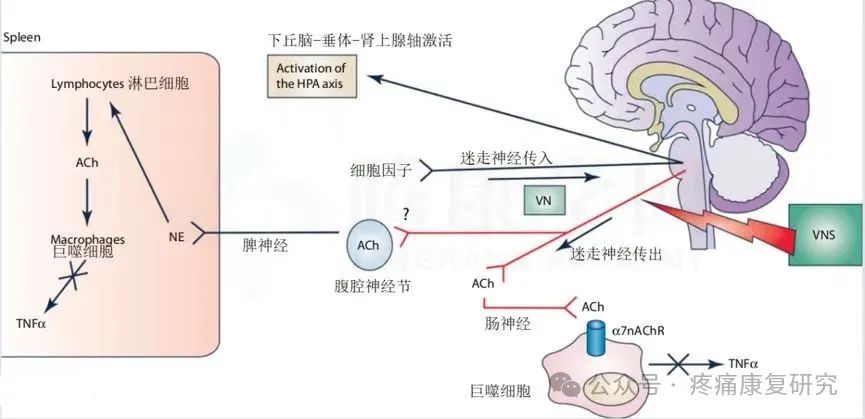
此外,VNS还具有抗凋亡作用。在心肌梗死等情况下,心肌细胞会发生凋亡,导致心脏功能受损。VNS通过减少细胞色素c的释放,抑制凋亡信号通路的激活,从而保护心肌细胞。
例如,在一些动物模型研究中,VNS治疗后的心肌梗死面积明显减小,这与VNS的抗凋亡和抗炎作用密切相关。
3.对心脏重构的影响
心脏重构是心血管疾病进展的重要病理过程,包括心肌细胞肥大、心肌纤维化等改变,最终导致心脏结构和功能的恶化。
VNS在抑制心脏重构方面具有潜在作用。它可以调节多种信号通路,如抑制肾素-血管紧张素-醛固酮系统(RAAS)的过度激活,减少醛固酮等激素对心脏的不良影响,从而减轻心肌纤维化。
同时,VNS还能影响心肌细胞的代谢和功能,促进心肌细胞的存活和修复。
例如,在心力衰竭动物模型中,长期的VNS治疗可以改善心脏的收缩和舒张功能,减少心室的扩张和心肌肥厚,延缓心脏重构的进程。
4.对血管功能的调节
VNS不仅对心脏有直接作用,还能影响血管功能。它可以通过调节血管内皮细胞的功能,促进一氧化氮(NO)等血管舒张因子的释放,导致血管舒张,降低外周血管阻力,从而减轻心脏的后负荷。
在高血压等疾病中,血管阻力增加是重要的病理生理改变,VNS的这种血管调节作用有助于降低血压,改善心脏的血液动力学环境。
此外,VNS对血管平滑肌细胞的增殖和迁移也有一定的抑制作用,有助于维持血管的正常结构和功能,减少动脉粥样硬化等血管病变的发生风险,进一步保护心血管系统的健康。
四、在不同心血管疾病中的具体作用
1.心脏骤停
在动物实验中,VNS与心肺复苏(CPR)联合使用,可提高大鼠自主循环恢复(ROSC)的成功率,减少CPR的持续时间和所需的电除颤次数。
这可能是因为VNS能够抑制交感神经系统的过度激活,改善心脏的电生理稳定性。
2.心力衰竭
研究发现,VNS可以改善心力衰竭动物模型的左心室功能,降低死亡率。
其机制可能与调节交感-副交感神经平衡、抑制炎症反应、改善心肌能量代谢等有关。
在临床研究中,虽然VNS对心力衰竭患者的死亡率和心脏重构没有显著改善,但在改善患者的生活质量方面显示出一定的效果,如提高6分钟步行距离、改善纽约心脏协会(NYHA)功能分级和生活质量评分等。
3.急性心肌梗死
VNS在急性心肌梗死中的作用机制较为复杂。
一方面,它可以通过调节自主神经系统的平衡,减少心律失常的发生;另一方面,VNS具有抗炎和抗凋亡作用,能够减轻心肌梗死的面积,保护心肌细胞。
例如,在猪和大鼠模型中,VNS可改善心肌梗死后的心室功能,减少梗死面积。
4.心房颤动
心房颤动与自主神经系统的失衡密切相关,尤其是交感神经的过度激活。
LL-VNS通过刺激迷走神经,调节自主神经系统的平衡,抑制心房的电重构和结构重构,从而降低心房颤动的发生风险和复发率。
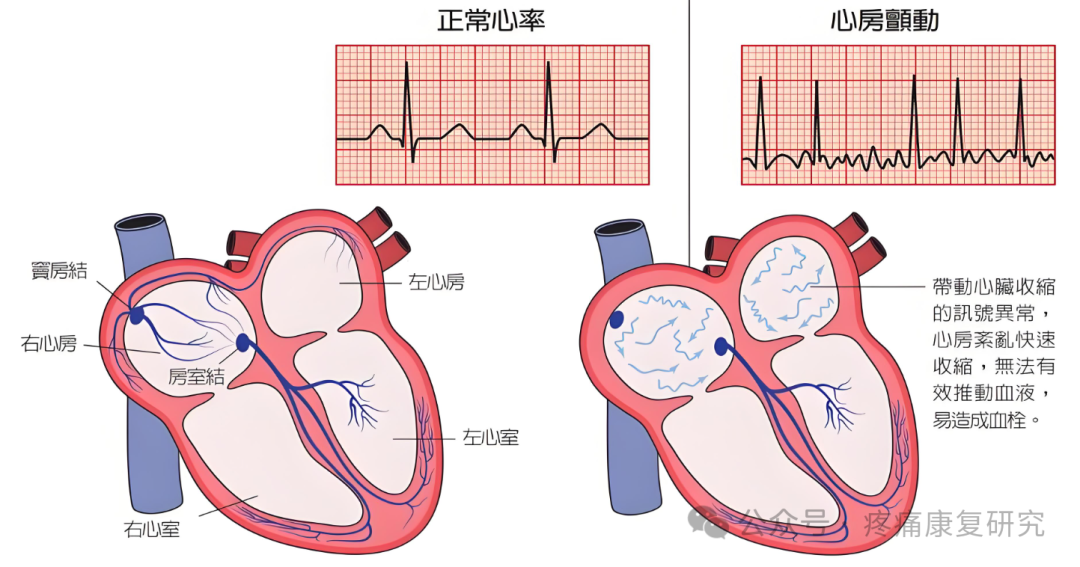
研究表明,LL-VNS可以逆转快速心房起搏诱导的心房重塑,抑制心房颤动的诱发。
VNS在心血管系统中的应用前景广阔。通过深入了解其解剖结构和作用原理,我们为未来开发更有效的心血管疾病治疗方法提供了重要的理论依据。
虽然目前仍有许多问题需要进一步研究和探索,但VNS无疑为心血管疾病的治疗带来了新的希望。
参考文献
Capilupi MJ, Kerath SM, Becker LB. Vagus Nerve Stimulation and the Cardiovascular System. Cold Spring Harb Perspect Med. 2020 Feb 3;10(2):a034173. doi: 10.1101/cshperspect.a034173. PMID: 31109966; PMCID: PMC6996447.


