Adv Sci:中山大学郭志勇团队研究揭示通过USP19介导的SLC7A11去泛素化抑制无缺血肝移植中肝细胞凋亡
时间:2024-11-25 18:00:19 热度:37.1℃ 作者:网络
无缺血肝移植(IFLT)是一种避免缺血再灌注损伤的新型临床方法。
2024年11月22日,中山大学郭志勇团队在Advanced Science 在线发表题为“Suppression of Hepatocyte Ferroptosis via USP19-Mediated Deubiquitination of SLC7A11 in Ischemia-Free Liver Transplantation”的研究论文。该研究旨在确定IFLT移植与传统肝移植(CLT)中最显著的程序性细胞死亡途径,并探讨其潜在机制。
铁死亡是IFLT和CLT移植之间最明显的程序性细胞死亡形式。在各种细胞死亡抑制剂中,ferroptosis抑制剂(Ferrostain-1)是防止氧剥夺/再氧化(OGD/R)引起的肝细胞损伤最有效的一种。在人和猪中,IFLT与CLT移植相比,肝细胞铁死亡明显减轻。泛素化酶筛选确定了IFLT与CLT移植中泛素特异性蛋白酶19 (USP19)的增加量。USP19在移植物中的上调与肝移植受者病理性Suzuki评分降低、移植后肝酶峰值水平降低、早期异体移植物功能障碍减少相关。USP19过表达减轻小鼠移植后肝损伤。在机制上,USP19通过去除其K63连接的泛素链来抑制溶质载体家族7成员11 (SLC7A11)的降解。值得注意的是,USP19过表达在小鼠中以SLC7A11依赖的方式减少铁死亡和IRI。总的来说,USP19介导的通过去泛素化SLC7A11抑制肝细胞铁死亡是IFLT消除移植物IRI的关键机制。

肝移植是终末期肝病的标准治疗方法。在常规肝移植(CLT)中,供体肝脏在冷冲洗后获得,通常在低温(4°C)保存液中保存和运输,然后在低温和缺氧条件下植入。移植后的再灌注不可避免地引入移植物缺血-再灌注损伤(IRI),导致各种并发症,包括再灌注后综合征、早期同种异体移植物功能障碍、原发性无功能和缺血型胆道病变。
IRI是一个两阶段的现象,与器官血流量减少有关,导致缺氧和细胞损伤,然后在氧气输送恢复后加剧。虽然许多干预措施可以改善小鼠IRI,但这些策略仅仅转化为临床实践。最近,各种类型的机器灌注已被用于保存供肝。机器灌注减少移植物IRI的可行性和有效性已在临床试验中得到证实。这些入路可以减轻损伤的后果。然而,由于机器灌注仅在保存阶段使用,并且在机器灌注之前和植入期间肝脏遭受缺血,移植物IRI仍然存在。研究提出了一种无缺血肝移植(IFLT)的新概念,在此过程中,供体肝脏在持续的恒温氧合条件下被获取、保存和植入。研究不仅证明了IFLT的可行性,而且通过移植超过85%的大泡性脂肪变性的供体肝脏,也证明了这种方法的优点。最近的随机试验表明,IFLT可显著减少IRI相关并发症。特别相关的是,肝活检的组织学、转录组学和代谢组学分析表明,IFLT中几乎没有移植物IRI。因此,IFLT不仅提供了一种全新的方法来避免IRI,而且还提供了一种独特的模型来研究肝移植期间移植物IRI的机制。
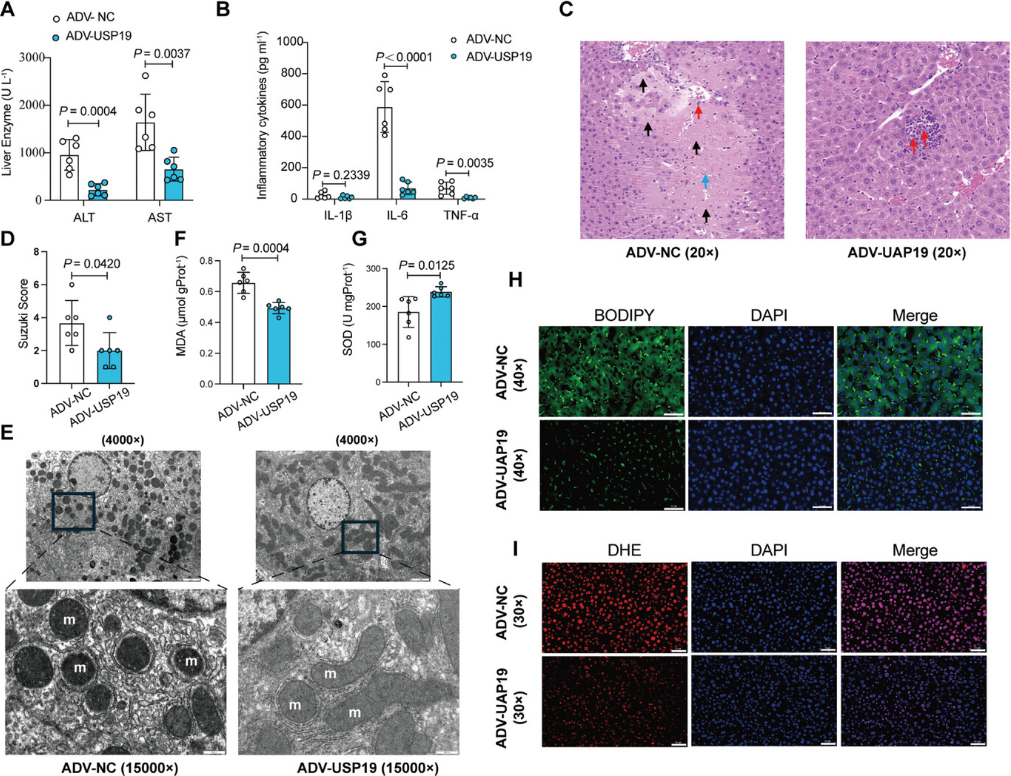
USP19抑制IRI并抑制铁死亡(图源自Advanced Science )
多种细胞死亡通路的激活是肝脏IRI发生的关键机制之一。铁死亡在形态学、遗传学和生物化学上不同于其他已知的细胞死亡途径。形态学上,铁死亡细胞表现出典型的坏死样变化。生物化学上,铁死亡的特点是产生致命水平的铁依赖性脂质过氧化。溶质载体家族7成员11 (SLC7A11)-谷胱甘肽(GSH)-谷胱甘肽过氧化物酶4 (GPX4)轴被认为是预防铁死亡的关键。泛素化是蛋白质翻译后修饰(PTM)的一种可逆形式。泛素化和去泛素化之间的动态变化可以调节蛋白质的丰度、定位和活性,从而影响细胞的生存和死亡。
在目前的研究中发现铁死亡是IFLT和CLT移植之间最明显的程序性细胞死亡形式。IFLT与CLT移植相比,铁死亡明显减少。从机械上讲,泛素特异性蛋白酶19 (USP19)在IFLT移植物中的表达上调,通过去泛素化SLC7A11来抑制铁死亡。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202406200


