Theranostics:卜培莉教授团队揭示FBLN7在高血压血管重构中的重要作用
时间:2024-11-15 06:00:11 热度:37.1℃ 作者:网络
血管重构是众多慢性血管疾病共有的病理标志,也是心血管并发症的重要风险因素,对人类健康构成严重威胁。因此,采取有效的干预措施来减轻其有害影响是必要的。作为一种细胞外基质蛋白, FBLN7在心血管疾病中的研究尚少。最近的研究表明,FBLN7在成纤维细胞激活和心肌纤维化中起重要作用,FBLN7基因敲除可以缓解小鼠心肌梗死后心肌纤维化。然而,FBLN7在其它心血管疾病中的作用仍在很大程度上未被探索。
2024年11月4日,山东大学齐鲁医院卜培莉教授团队在Theranostics上发表题为“FBLN7 mediates vascular smooth muscle cell phenotype switching and vascular remodeling in hypertension”的研究论文。该研究发现FBLN7是血管平滑肌细胞表型转换的调节因子,FBLN7能够通过其C端与多配体蛋白聚糖Syndecan-4的细胞外和跨膜域结合,从而影响SDC4的功能和二聚体形成。这种相互作用抑制ROCK/MRTF-A信号通路,促进平滑肌细胞从收缩表型向合成表型的转变,并加剧血管重构。

研究人员首先通过生物信息学分析揭示了FBLN7在血管重构模型主动脉组织中表达升高,通过Elisa技术检测到FBLN7在高血压患者及小鼠高血压模型外周血中表达升高,这表明FBLN7可能参与了高血压血管重构的发展。通过分析主动脉组织单细胞测序数据及WB验证,表明FBLN7在血管平滑肌细胞(VSMCs)中高表达。通过WB、IHC、IF验证表明在Ang II诱导的小鼠高血压血管重构模型中,FBLN7在主动脉中膜表达升高且与平滑肌细胞标记物α-SMA共定位。

接下来,研究人员构建了FBLN7基因敲除小鼠和腺相关病毒载体介导的平滑肌细胞特异性FBLN7过表达小鼠。通过微量渗透泵连续28天给予小鼠Ang II建立了高血压血管重构模型,结果表明FBLN7敲除可减轻Ang II诱导的血管重构,减少主动脉壁厚度和胶原形成。相反,VSMC特异性FBLN7过表达会加剧重构表型。采用RNA测序、WB和IF等方法研究FBLN7在VSMCs中的生物学功能。结果表明,FBLN7主要影响细胞粘附、细胞膜受体结合、血管平滑肌收缩以及肌动蛋白细胞骨架调节相关基因的表达,且FBLN7可以通过ROCK/MRTF-A途径抑制平滑肌收缩相关基因的表达。

为进一步探索FBLN7介导平滑肌表型转化的机制,研究人员对FBLN7潜在受体进行了筛选。已知硫酸乙酰肝素蛋白聚糖(HSPGs)是FBLN7的潜在受体。SDC4作为HSPGs家族的一员,在血管组织中广泛表达,并被证明可以通过RhoA途径介导VSMCs的表型转化。研究人员通过LC-MS/MS、Co-IP、分子对接技术验证了FBLN7和SDC4的结合及结合的节段。通过WB、Co-IP、分子动力学模拟技术揭示了FBLN7可以影响SDC4二聚体的形成。最后,通过功能实验验证证明SDC4二聚化及FBLN7-SDC4相互作用会影响平滑肌细胞表型转化。
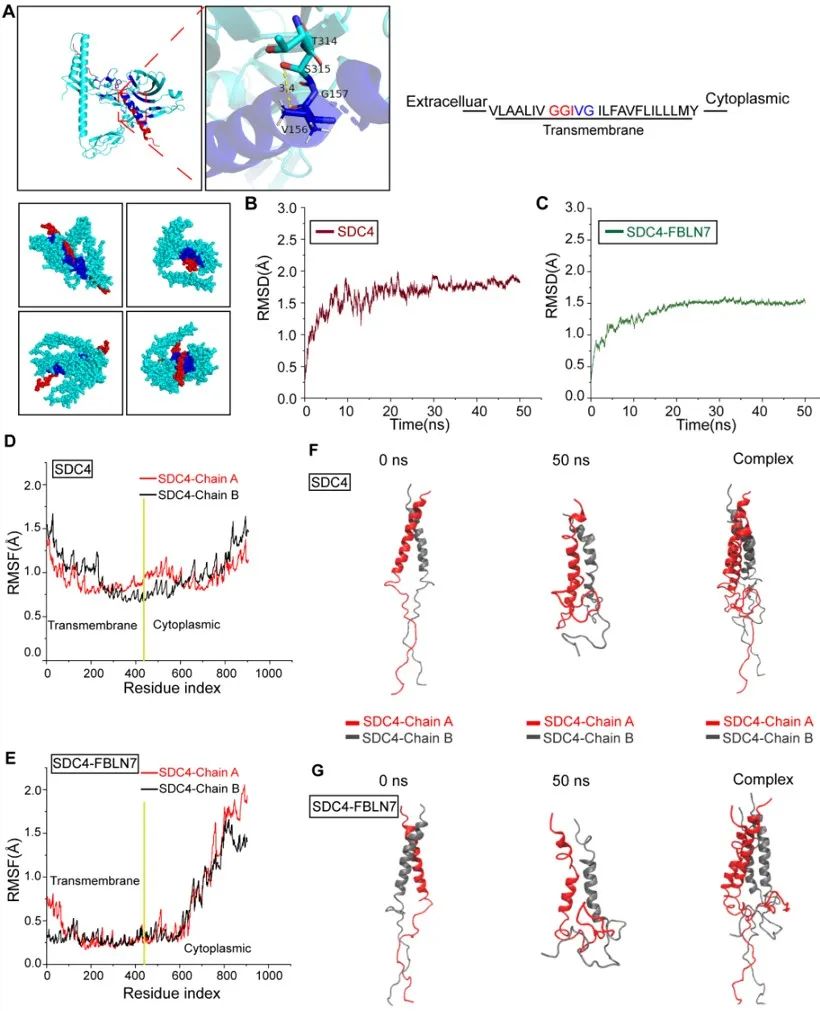
综上所述,该研究证明了FBLN7在血管重构中的重要作用。FBLN7主要通过调节与VSMCs收缩功能和细胞骨架重排相关的基因来参与血管重构。FBLN7与细胞膜受体的相互作用是其功能实现的关键途径。具体而言,FBLN7与SDC4的相互作用会抑制SDC4的功能,并导致其同源二聚体的解离。这会抑制ROCK/MRTF-A途径的激活,从而降低与平滑肌收缩表型相关基因的表达。
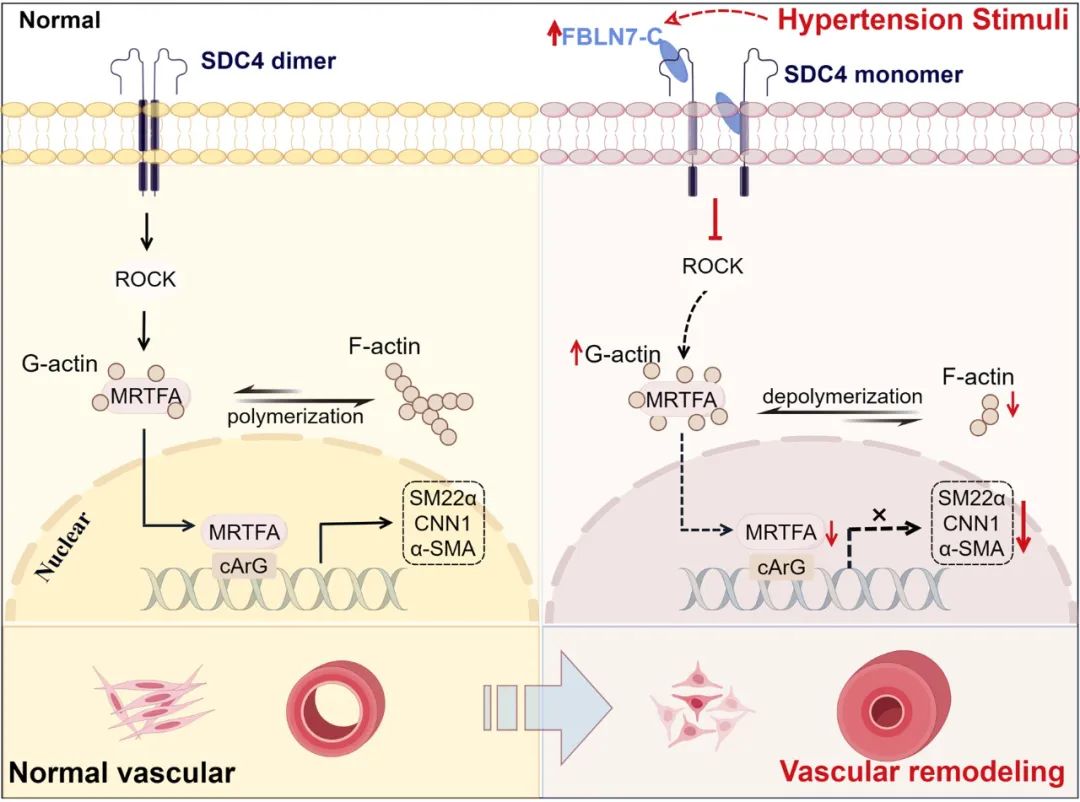
山东大学齐鲁医院心血管内科的卜培莉教授和提蕴副教授为文章的共同通讯作者,山东大学齐鲁医院心血管内科姚国庆博士研究生为文章的第一作者。
原文链接:
https://www.thno.org/v14p7569.htm


