Life Sci 河北大学郭蕊团队发现hBMSC-Exos缓解PD-1/PD-L1抑制剂导致的心肌损伤的作用机制
时间:2024-10-23 14:00:21 热度:37.1℃ 作者:网络
免疫检查点抑制剂(ICIs)疗法作为一种新兴的肿瘤治疗手段,在癌症治疗领域取得许多重大进展,给癌症患者带来新的希望。ICIs通过增强机体免疫系统对肿瘤细胞的杀伤来起到抑制肿瘤的作用,然而ICIs在激活免疫系统的同时,也导致了一些与免疫相关的不良反应(irAE)。大多数irAE在停止用药后或者激素治疗后会逐渐消退,但是ICIs导致的心肌炎(ICIAM)却演变极其迅速,且致死率高。目前,ICIs导致的心肌炎具体分子机制尚不完全清楚。另一方面,临床上控制ICIAM的主要方式是抑制亢进的免疫系统,但这样做又会同时导致肿瘤的治疗效果受到影响。因此,阐明ICIAM的具体分子机制并开发能有效治疗ICIAM的方法对癌症治疗领域有着重要意义。
2024年10月5日,河北大学生命科学学院干细胞与生物医学实验室郭蕊教授在著名期刊Life sciences上发表了题为“Exosomes from human bone marrow MSCs alleviate PD-1/PD-L1 inhibitor-induced myocardial injury in melanoma mice by regulating macrophage polarization and pyroptosis”的研究成果。该研究一方面阐明PD-1/PD-L1抑制剂导致心肌损伤的具体分子机制,另一方面还证实了人骨髓间充质干细胞来源的外泌体(hBMSC-Exos)不仅能够用于治疗PD-1/PD-L1抑制剂导致的心肌损伤,而且对肿瘤也有一定抑制作用。本研究为开发新的肿瘤治疗策略提供新的线索和思路。

首先,研究团队通过对心肌炎人群的单细胞测序数据进行分析,并分别筛选出心肌炎患者和心肌炎小鼠中的差异表达基因,发现在心肌炎中,巨噬细胞和细胞焦亡可能发挥着重要作用(图1)。
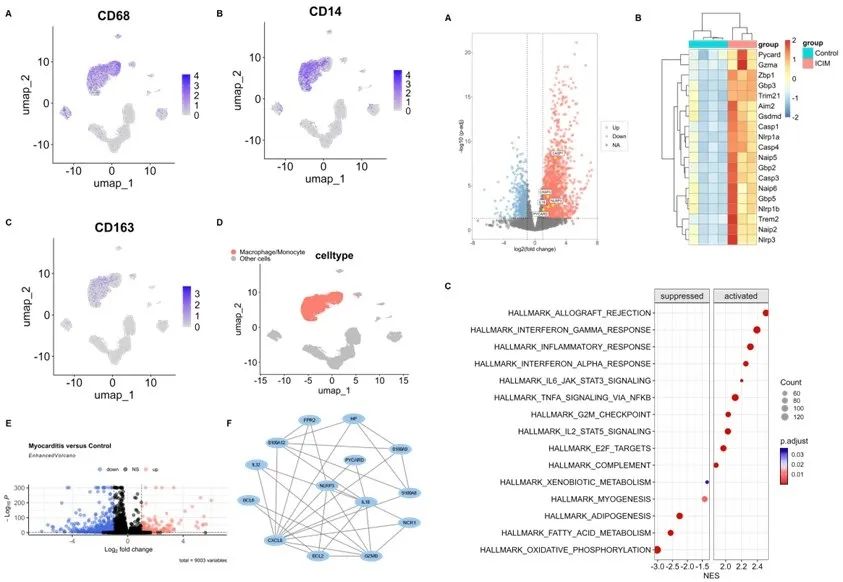
图1 (出自原文Figure 1、Figure 2)
随后,研究人员在体外使用PD-1/PD-L1抑制剂分别直接处理心肌细胞系HL-1和从小鼠腹水中提取并培养的巨噬细胞,检测了TNF-α、IL-6、IL-1β、Nlrp3、Pycard、IL-18等炎性因子和细胞焦亡指标。实验结果表明,PD-1/PD-L1抑制剂并不会直接造成心肌细胞炎症和焦亡(图2A-F),但可以使巨噬细胞向M1型极化(图2G)。这些结果提示,PD-1/PD-L1抑制剂引起心肌损伤很可能是通过影响巨噬细胞极化造成的。
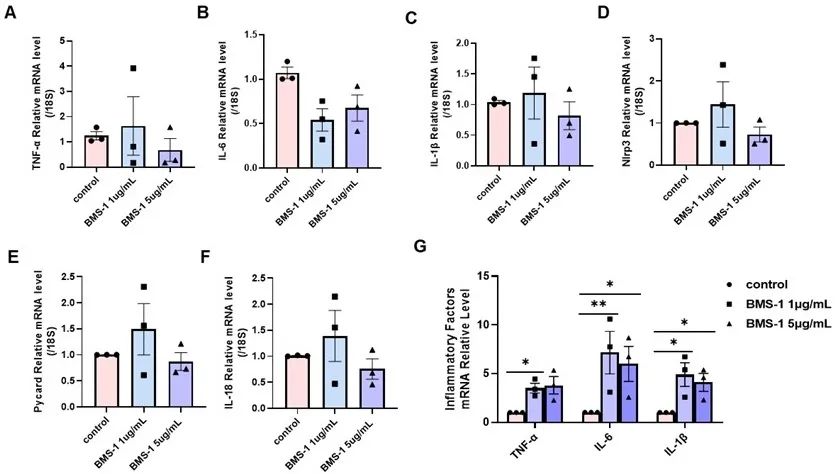
图2 (出自原文Figure 3)
然后,研究团队给予黑色素瘤荷瘤小鼠和正常小鼠注射PD-1/PD-L1抑制剂和hBMSC-Exos后,运用心脏超声检查小鼠心功能,结果发现hBMSC-Exos能够改善PD-1/PD-L1抑制剂造成的心脏功能损伤(图3A-C)。这表明hBMSC-Exos有望用于缓解PD-1/PD-L1抑制剂在心脏方面的副作用。
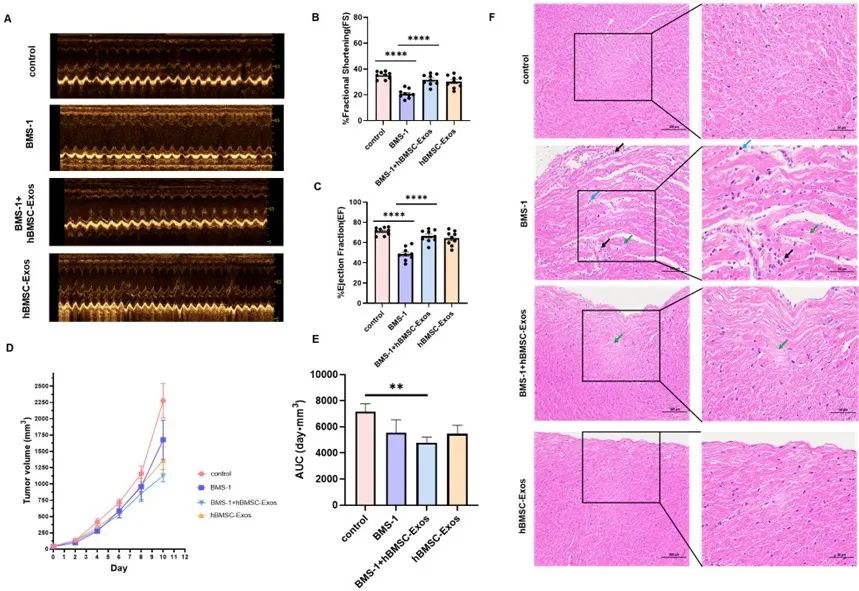
图3 (出自原文Figure 5、Figure S2、Figure S3)
与此同时,研究人员检测了在给予PD-1/PD-L1抑制剂和hBMSC-Exos处理后,巨噬细胞及小鼠心脏组织中炎性因子的表达。同时,采用流式细胞术和免疫荧光鉴定了巨噬细胞的表型,并对处理后小鼠心脏组织中的iNOS和CD163进行了免疫组化染色。结果显示,无论是在体内还是体外,hBMSC-Exos均能有效促使巨噬细胞由M1型转变为M2型(图4),这表明hBMSC-Exos改善心脏功能的作用是通过改变巨噬细胞极化实现的。
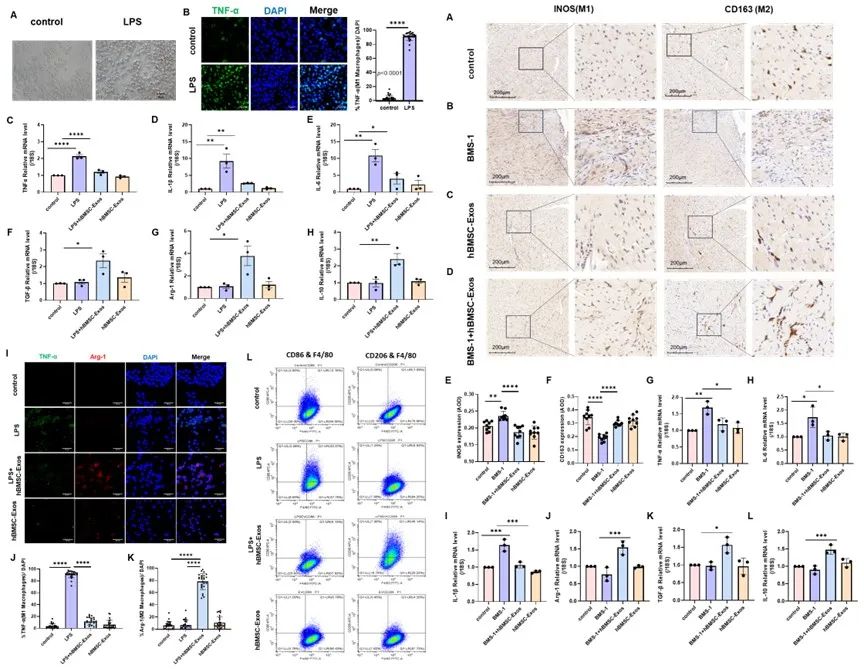
图4 (出自原文Figure 6、Figure 7)
进一步,研究人员对小鼠心脏组织和血清中与焦亡相关的指标进行了检测。同时将巨噬细胞与心肌细胞共培养,在使用PD1/PD-L1抑制剂和hBMSC-Exos对巨噬细胞进行处理后,对心肌细胞的焦亡标志物进行了检测。结果表明,hBMSC-Exos无论在体外还是体内均可以起到抑制细胞焦亡的作用(图5)。这表明hBMSC-Exos可以通过改变巨噬细胞极化来抑制细胞焦亡,从而起到心肌保护作用。
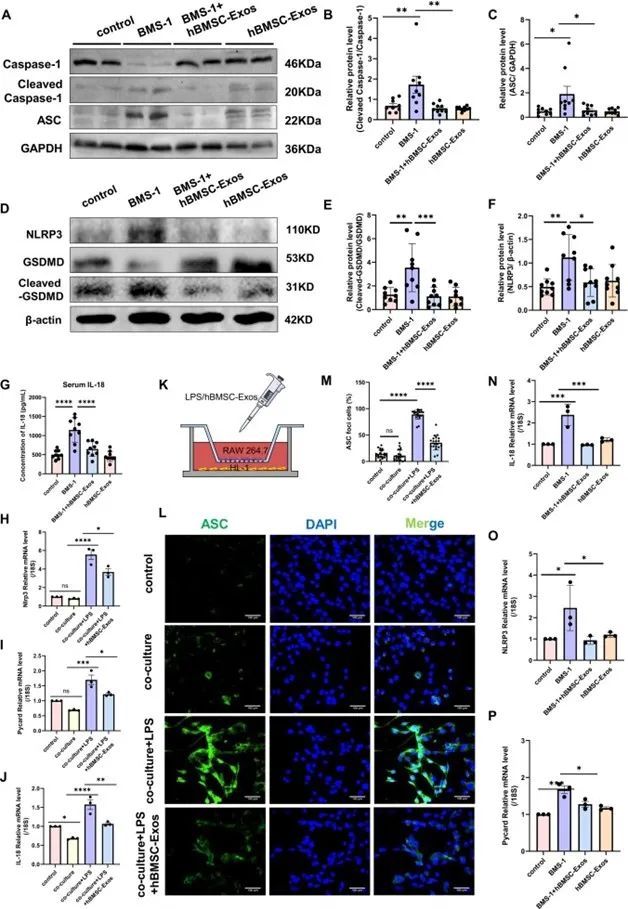
图5 (出自原文Figure 8)
最后,研究人员通过定期测量肿瘤体积发现,hBMSC-Exos对黑色素瘤的生长具有抑制作用(图3D-E)。这一发现使得PD-1/PD-L1抑制剂与hBMSC-Exos联合应用于抗肿瘤治疗的前景更加广阔。
综上,本研究表明,PD-1/PD-L1抑制剂抑制了巨噬细胞的M2极化,同时增强了M1极化,导致心肌细胞的焦亡和随之而来的心肌损伤。有趣的是,hBMSC-Exos有效抵消了PD-1/PD-L1抑制剂的有害影响,无论是单独使用还是与BMS-1联用,均表现出对黑色素瘤生长的抑制作用。本研究突显了PD-1/PD-L1抑制剂引起的心肌损伤与焦亡之间的关系,以及M1巨噬细胞在触发这一过程中的关键角色。重要的是,这项研究开创性地探索了hBMSC-Exos在缓解ICIs引起的心肌损伤方面的应用。这些发现表明,hBMSC-Exos在减轻与癌症治疗相关的心脏毒副作用方面具有潜力,从而为肿瘤心脏病学领域开辟了新的治疗途径。
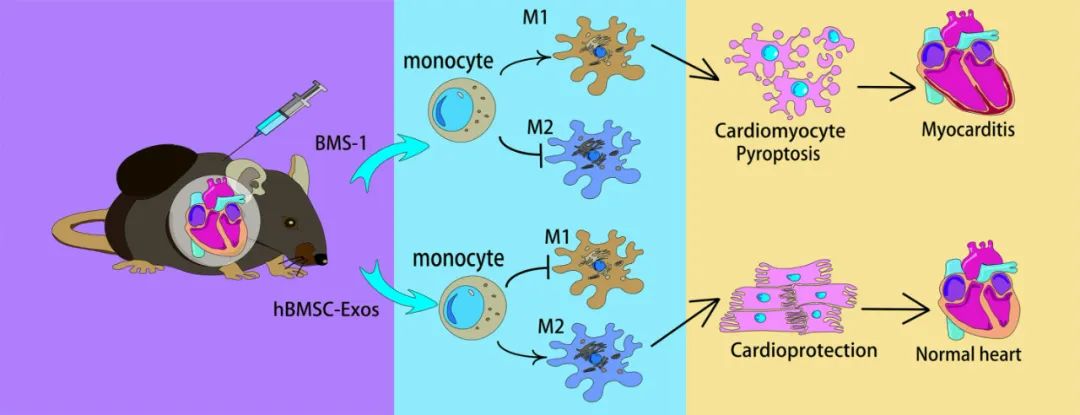
hBMSC-Exos保护PD-1/PD-L1抑制剂导致心肌损伤的示意图
河北大学生命科学学院硕士研究生周冰倩、覃芹、方越为本文的共同第一作者,硕士研究生刘晓宇、张孟雨,本科生王硕参与了该研究。河北大学生命科学学院干细胞与生物医学实验室郭蕊教授为本文的指导教师和通讯作者,并提供资金支持,钟理教授提供项目管理和资源方面支持。该研究得到了国家自然科学基金委员会、河北省自然科学基金委员会、京津冀基础研究合作专项、河北大学自然科学交叉学科研究项目的经费支持。
原文链接:
https://www.sciencedirect.com/science/article/abs/pii/S0024320524006982?via%3Dihub


