FDA批准的70款大环药物分析
时间:2023-05-04 09:36:15 热度:37.1℃ 作者:网络
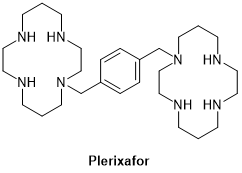
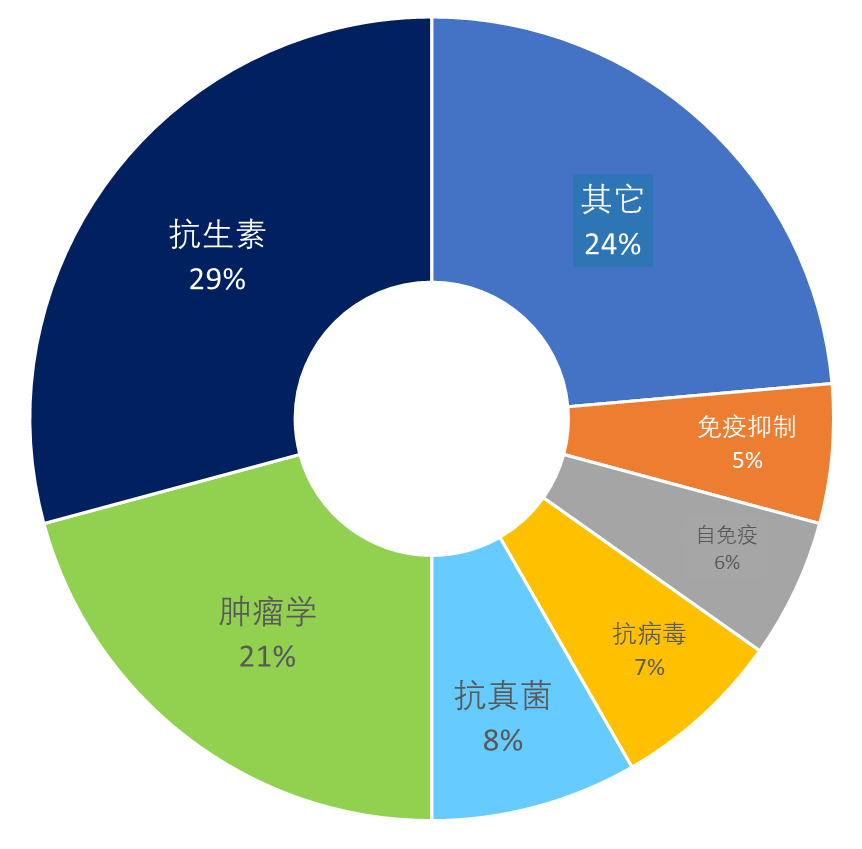
对于新出现的疾病和未被满足临床需求的治疗领域,医药同仁们一直在积极寻找创新方法。大环小分子药物、环肽、蛋白水解靶向嵌合体 (PROTAC) 和寡核苷酸是药物新模态的突出例子,它们很多都没有遵循Lipinski五规则的“理想”口服制剂的标准。 近日,J. Med. Chem. 最新发表的文章 Macrocycles in Drug Discovery-Learning from the Past for the Future,分析了 FDA 批准的大环化合物药物的特点。 图1. 从 PubMed (16) 检索到的文章数量:(A) 使用 “大环”作为关键词和 (B)“大环和药物发现”作为关键词(截止2022 年 5 月); 部分天然产物来源的大环药物(杆菌肽、放线菌素、两性霉素 B 和环孢菌素)以及一些通过从头设计获得的药物(simeprevir 和 lorlatinib)例子、治疗适应症以及在文献中首次报道的年份 图片来源:J. Med. Chem 大环通常定义为含有至少 12 个重原子(重原子指的是除H之外的原子)的闭环有机分子。1970年代末,不同科学领域对大环化合物的普遍兴趣开始增长,并从 1990 年代开始激增(图1)。在药物发现领域,快速增长阶段始于世纪之交(图 1)。 大环化合物的好处在于它们可以在半刚性、预先固定的结构中提供功能多样性和立体化学复杂性。 与开环类似物相比,大环化合物有更高的亲和力和选择性,可以结合到难以用传统的小分子药物给药的靶标上。 图2. Cyclosporine A 化学结构 分子量高达1202 Da. 的环孢素(Cyclosporine A,图2)是第一款多肽口服制剂。从历史上看,大环药物大多是自然化合物(例如环孢素), 但从头设计的大环药物现在也逐渐大量获得监管审批。 截至目前,FDA共批准了 67 种大环化合物作为药物(表 1),其中26 种大环药物 (占比39%) 是口服给药、 41 种是肠胃外给药。绝大多数大环药物是天然产物或其衍生物(n = 59, 88%),第一个从头设计(de novo design)的大环药物普乐沙福 (Plerixafor,图3) 直到 2008 年才获得批准。 表1. FDA 批准的大环药物 图3. Plerixafor化学结构 将天然产物细分为原始天然产物 (n = 25) 和天然产物衍生物 (n = 34) 进行分析后可以发现,12种天然产物衍生物源于药代动力学的优化。 在进行PK优化之后,7种抗菌赤霉素和利福霉素衍生物,以及用于肿瘤学和免疫抑制剂的依维莫司,它们的口服生物利用度和半衰期得到改善。其他3种衍生物的化学稳定性、蛋白酶耐受性和溶解度均得到改善。药效学、更广泛的活性,以及减少的副作用,构成了产生7种衍生物的主要原因。有5种衍生物在药效学和药代动力学方面同时得到了优化。 传染病是大环类药物治疗的主要适应症(占所有大环类药物的 44.4%,图 4,表 1)。在这一类别中,大多数用作抗菌剂(29%),但抗病毒剂 (6.9%) 和抗真菌剂 (8.3%) 也很重要。肿瘤(20.8%)、自身免疫性疾病(5.6%)和免疫抑制剂(5.6%)是其后的三个主要适应症。大环类药物用于 13 个其他次要适应症的药物总数占比为 23.6%,适应症包括抗利尿剂、慢性疼痛、遗传性肥胖、心力衰竭等。 图4. 上市大环药物适应症分布 大环药物批准呈现出的趋势: 自 1948 年以来,抗菌药物获得批准的频率相当有规律; 用于治疗丙型肝炎病毒感染的 5 个大环化合物均在 2013 年至 2017 年间获批; 近年来大环化合物在肿瘤学中的应用得到了很大的彰显,2007 年之前总计获批4款药品,而 2007 年之后已有11款药物获批。 从大环化合物药物作用靶点来看,可以发现抗菌大环化合物主要针对一些“传统”目标,例如核糖体和 RNA 聚合酶 (RNAP)。但在肿瘤学中,大环化合物针对大量靶标包括激酶、脱乙酰酶、激素受体和微管蛋白。Pacritinib (图5) 于 2022 年获批,是第一个 Janus 激酶 2 (JAK2) 和 FMS 样受体酪氨酸激酶 3 (FLT3) 的双重抑制剂。值得注意的是,丙型肝炎病毒的 NS3/4A 蛋白酶是唯一受大环药物调节的病毒靶点。 图5. Pacritinib化学结构 除此之外,还有几种大环药物充当分子胶,与蛋白质靶标形成三元复合物。环孢素和沃罗孢素与亲环蛋白 A (CyPA) 和神经钙蛋白 B (CNB) 的结合,用于治疗自身免疫性疾病和用于免疫抑制以防止移植器官排斥。FK506 结合蛋白 FKBP12 与 CNB 或哺乳动物雷帕霉素靶标 (mTOR) 的三元复合物,由子囊霉素和雷帕霉素家族的大环诱导,用于自身免疫性疾病、免疫抑制和肿瘤学。 大环类药物主要用作抗菌药物,肿瘤是第二大适应症。文献调查表明,肿瘤仍将是未来的主要适应症,但大环化合物也有望用于多种新适应症。此外,大环化合物正在进行临床试验或针对大量不同受体进行临床前研究。 检查大环药物-靶标结合复合物 (n = 34) 的结构表明,79% 的大环药物调节那些具有平坦、隧道状或凹槽状结合位点的靶标。在三元复合物中,大环药物充当分子胶,占三个凹槽形结合位点。与一组符合利平斯基五规则标准的药物的比较得出结论,大环化合物可以调节这些难以靶向药物的靶点,因为大环化合物更有可能采用盘状和球状的优势构象。仅有五个临床候选物的靶标披露了晶体结构。这些大环化合物中的三个结合在槽形结合位点中,一个结合在隧道形结合点中。 在大环药物和临床候选药物中,天然产物及其衍生物的数量远远多于从头设计的化合物(比例 > 4:1)。天然物衍生物主要改善药代动力学、药效学,或者在少数情况下两者兼而有之。接近 40% 的大环药物具有口服生物利用度,而临床候选药物中大约有30%具有口服生物利用度。 参考资料: [1] Doak, B. C. et al. Oral Druggable Space beyond the Rule of 5: Insights from Drugs and Clinical Candidates. Chem. Biol. 2014, 21, 1115–1142. [2] Shultz, M. D. Two Decades under the Influence of the Rule of Five and the Changing Properties of Approved Oral Drugs. J. Med. Chem. 2019, 62, 1701–1714. [3] Jimenez, D. G. et al. Macrocycles in Drug Discovery─Learning from the Past for the Future. J. Med. Chem. 2023. doi.org/10.1021/acs.jmedchem.3c00134 [4] Marsault, E. et al. Macrocycles Are Great Cycles: Applications, Opportunities, and Challenges of Synthetic Macrocycles in Drug Discovery. J. Med. Chem. 2011, 54, 1961–2004. [5] Begnini, F. et al. Mining Natural Products for Macrocycles to Drug Difficult Targets. J. Med. Chem. 2021, 64, 1054–1072. [6] DeLorbe, J. E. et al. Thermodynamic and Structural Effects of Macrocyclic Constraints in Protein–Ligand Interactions. ACS Med. Chem. Lett. 2010, 1, 448–452. [7] Giordanetto, F. et al. Macrocyclic Drugs and Clinical Candidates: What Can Medicinal Chemists Learn from Their Properties?. J. Med. Chem. 2014, 57, 278–295. [8] Shawky, A. M. et al. Comprehensive Overview of Globally Approved JAK Inhibitors. Pharmaceutics. 2022, 14, 1001, [9] Schreiber, S. L. The Rise of Molecular Glues. Cell. 2021, 184, 3–9. 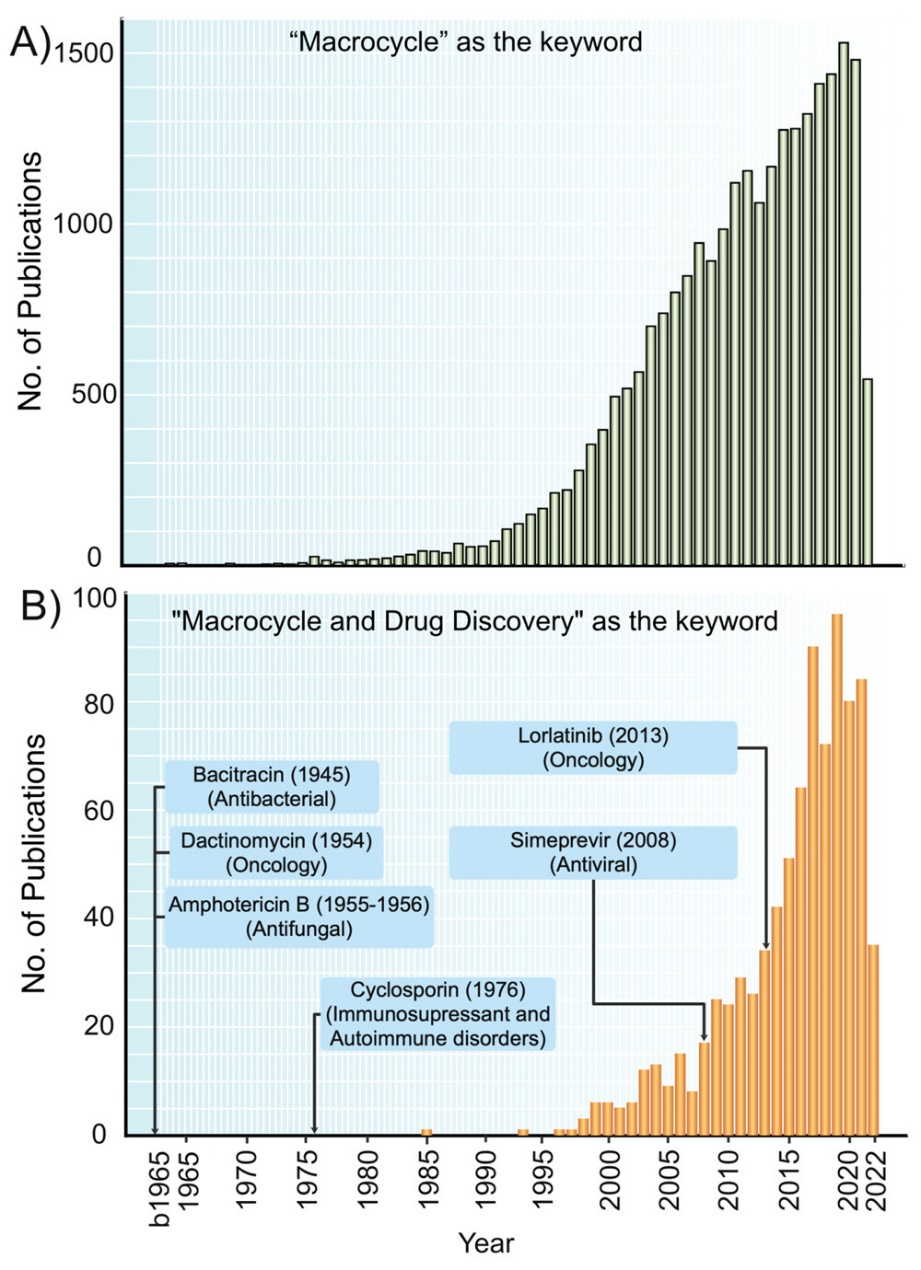

01
FDA 批准的大环药物分析

02
大环药物的适应症和靶点分析

03
结语


