J Hepatol:南方医科大学陈金军等揭示肝硬化急性失代偿期的循环微生物特征
时间:2022-10-30 20:33:41 热度:37.1℃ 作者:网络
肝硬化相关免疫功能障碍(Cirrhosis associated immune dysfunction, CAID)与急性失代偿(acute decompensation, AD)的进展相关,可影响细菌感染的死亡风险。然而CAID的潜在机制尚不清楚,但表明先天免疫系统和适应性免疫系统都受到了广泛的干扰。CAID的严重程度随着肝硬化的严重程度而增加,并可在急性-慢性肝衰竭(acute-on-chronic liver failure, ACLF)晚期患者中表现为免疫瘫痪。
ACLF是一种综合征,其特征是突发事件、多器官衰竭和全身炎症细菌感染是AD患者最常见的诱发事件在约30%的AD患者中,没有发现任何诱发性疾病考虑到肝硬化与CAID相关,有可能是除细菌引起的感染外的其他感染,如病毒感染,作为诱因参与其中。尽管细菌感染对肝硬化的影响已被很好地描述,但非嗜肝病毒(non-hepatotropic virus, NHVs)感染的影响尚不清楚。
2022年10月26日,南方医科大学陈金军与Rajiv Jalan合作在Journal of Hepatology 杂志在线发表题为“Prognostic and therapeutic significance of microbial cell-free DNA in plasma of people with acutely decompensated cirrhosis”的研究论文,该研究利用宏基因组下一代测序(mNGS)对肝硬化急性失代偿患者中循环微生物的基因组片段进行评估,结果表明NHVs可能在AD的复杂化过程中具有致病作用。需要进一步的验证来确定这是否应该纳入AD患者的日常管理。

以前的研究集中在嗜肝病毒作为AD潜在沉淀剂的潜在作用。然而,非嗜肝病毒(NHVs)的感染,如单纯疱疹病毒、人巨细胞病毒、人细小病毒B19和EB病毒,已知会导致急性肝衰竭,其作用尚不清楚。
宏基因组新一代测序(Metagenomic next-generation sequencing, mNGS)是一种重要的不依赖培养的技术,可以同时从临床样本中检测出几乎所有已知的病原体对微生物细胞游离DNA (cell-free DNA, cfDNA)进行测序可以诊断几种感染。mNGS在肝硬化患者中的临床应用相关研究较少本研究的主要目的是通过对血浆微生物cfDNA测序,综合评价急性失代偿肝硬化患者循环微生物基因组片段,并将其与临床结果联系起来。次要目的是验证CMV再激活的潜在作用,一种已知的NHV与现有的抗病毒药物,在确定失代偿肝硬化患者的预后。
在这项研究中,研究人员对129例肝硬化AD患者行血浆mNGS检查。其中10名健康志愿者和20名、39名和81名稳定型肝硬化、严重脓毒症和恶性血液病患者分别作为对照。在一个验证队列(n = 58)中进行了人类巨细胞病毒(cytomegalovirus, CMV)再激活的验证分析,并进行了探索性治疗。结果表明,研究队列中74.4%(96/129)例患者检出188种微生物,包括病毒(58.0%)、细菌(34.1%)、真菌(7.4%)和衣原体(0.5%)。
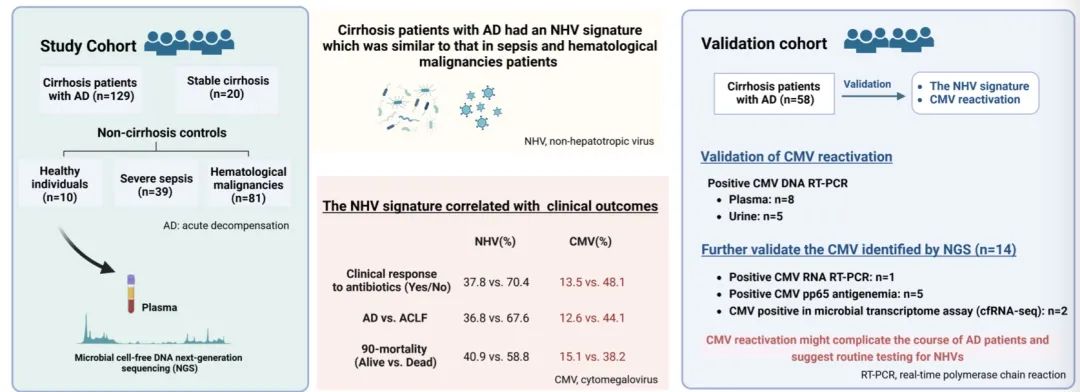
研究概述(图源自Journal of Hepatology )
有趣的是,AD患者具有NHV特征,CMV是最常见的NHV,这与经验抗生素治疗的临床效果、进展为急性-慢性肝衰竭(ACLF)和90天死亡率相关。ACLF患者的NHV特征与脓毒症和恶性血液病患者相似。在验证队列中,有24.1%(14/58)患者检测到可治疗的NHV、CMV。在14例mNGS检测到CMV的病例中,9例通过DNA RT-PCR或pp65抗原血症检测进一步验证。3例巨细胞病毒再激活患者接受更昔洛韦探索性治疗,临床疗效明显。
这项研究的一个重要发现是,在ACLF患者中观察到的NHV特征与脓毒症或血液系统恶性肿瘤患者相似,且NHV特征与临床结果相关。血浆mNGS鉴定出了已知可引起人类慢性感染的NHV的各种基因组片段,如CMV、EBV、TTV和人类细小病毒B19。在这项研究中,CMV病毒血症是最常见的,并与急性失代偿性肝硬化的进展有关。巨细胞病毒可导致胆汁淤积,肝损伤恶化,门静脉血栓形成和肺炎,可增加全因死亡率。由于缺乏肝脏或肠道组织学等特异性组织损伤的数据,目前的研究无法诊断CMV感染是否与CMV疾病相关。
综上所述,该研究使用了针对循环微生物基因组片段的非靶向血浆mNGS方法,并提示AD患者,尤其是ACLF患者具有明显的NHV特征,这可能使AD的病程复杂化,这一观察结果在另一项前瞻性研究中得到了验证。未来还需要进一步的细化和验证来定义测试的临床意义的NHVs AD患者的日常管理。
原文链接:
https://www.journal-of-hepatology.eu/article/S0168-8278(22)03144-0/fulltext#


