PNAS:适当压力,有益健康!
时间:2022-10-13 15:52:51 热度:37.1℃ 作者:网络
随着生活节奏的加快,人们的压力也在变得越来越大。之前的一些研究表明,压力会导致脱发、白发、肥胖等危害。长期压力会导致一系列健康问题,包括心脏病、糖尿病、抑郁和焦虑。不仅如此,压力还会抑制免疫功能,减弱抵御能力,甚至是促进肿瘤生长。
然而,常言道,人无压力轻飘飘,压力并不一定都是坏事,适当的压力可以成为我们前进的动力,迈向人生一个又一个高峰。
近日,美国凯斯西储大学医学和病理学系教授 Fabio Cominelli 领导的研究团队在《美国国家科学院院刊》(PNAS)上发表了题为:Chronic stress induces colonic tertiary lymphoid organ formation and protection against secondary injury through IL-23/IL-22 signaling 的研究论文。
该研究表明,慢性压力对小鼠结肠炎的继发性损伤具有保护作用。这意味着,免疫系统可能会从某种程度的压力中受益。

炎症性肠病(IBD)是一种病因尚未明确的慢性、非特异性肠道炎症性疾病,主要包括溃疡性结肠炎(UC)和克罗恩病(CD)。IBD 高发于18-25岁人群。目前,在东亚国家,IBD 患者人数正在与日俱增。
虽然近几年,科学家们对这种肠道疾病有了更充分的了解,但其明确的发病机制仍难以捉摸。因此,识别环境触发因素和病因对于开发有效预防和治疗的方法至关重要。
目前,心理压力已被确定为炎症性肠病(IBD)的重要风险因素。除此之外,肠系膜三级淋巴器官(TLO)在 IBD 的疾病过程中发挥着重要作用。虽然 TLO 早在几十年前就被认为与 IBD 有关,但其发挥的是保护作用还是致病作用仍存在争议。
TLO 是在出生后形成的,具有密集的 CD4+T 细胞、滤泡树突状细胞和B细胞群,它们是对慢性炎症或损伤做出反应而形成的免疫细胞。虽然 TLO 的形成途径仍是未知的,但科学家们普遍认为 TLO 的形成最终取决于白细胞介素-23(IL-23)介导的趋化因子 CXC配体13 (CXCL13)的上调。但心理压力是否影响 TLO 的形成尚未有定论。
在这项研究中,研究团队研究了克罗恩病(CD)样回肠炎小鼠模型(SAMP)。他们在连续56天对小鼠进行约束性刺激以诱导慢性心理压力后,SAMP 小鼠表现出自发性和持续性的 CD 样回肠炎,但没有出现结肠炎。与对照组小鼠相比,SAMP 小鼠的结肠中类似 TLO 的结构数量明显增加。
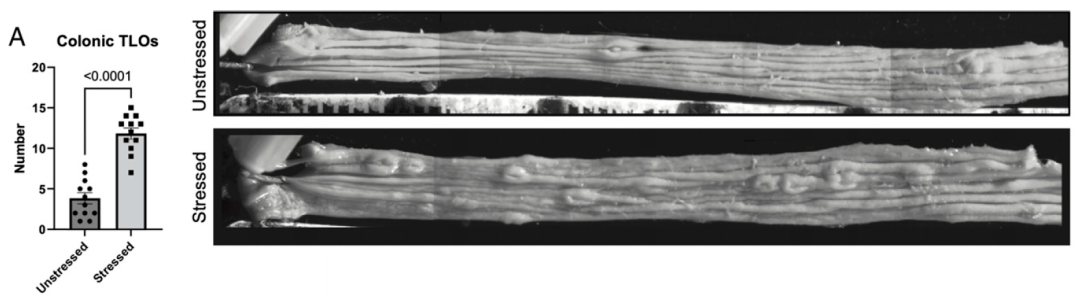
此外,压力没有显着增加 SAMP 小鼠小肠或大肠炎症,也没有改变小鼠肠道微生物组的组成。
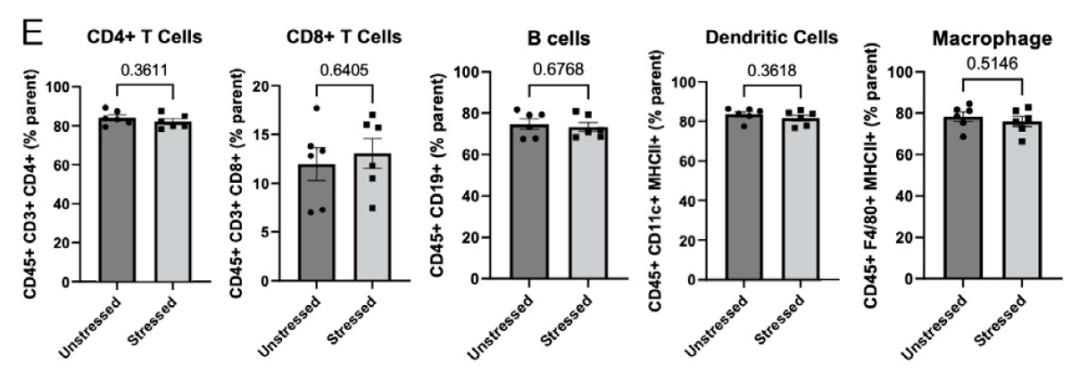
由于测量微生物组的方法存在固有的缺陷,研究团队随后进行了粪便微生物组移植。他们发现,虽然接受 SAMP 小鼠微生物组的受体小鼠表现出与供体小鼠相同的行为表型,但粪菌移植并没有增加 TLO 的形成。相反,压力增加了细胞因子 IL-23 和 IL-22 的产生,并随后上调了抗菌肽。IL-23 已被认为是 TLO 形成途径的一部分。IL-22 在伤口愈合和组织再生中发挥着保护作用,并具有抗炎和促炎反应。
随后,研究团队敲除了 SAMP 小鼠的 IL-23 受体。他们发现,压力增加了 IL-23 水平,但没有增加 IL-22 的水平,也没有增加 TLO 的形成。当给小鼠给予重组 IL-22 时,这种作用被逆转, TLO 的形成增加。这表明,心理压力通过增加 IL-23 的产生诱导 TLO 的形成。

值得注意的是,在用葡萄糖硫酸钠诱导继发性结肠损伤后,与对照组小鼠相比,承受压力的 SAMP 小鼠的结肠炎在组织学和结肠镜检查中均显着改善。压力的保护作用可以用 IL-22 信号的增加来解释。已知 IL-22 能诱导 AMP 的产生,AMP 是肠腔内微生物的调节因子。
通常情况下,压力与更严重的炎症有关。然而,并不是所有经历压力的患者病情都更严重。因此,这项研究具有转化意义,因为它证明了在一些情况下,压力具有有益的影响。
该论文的通讯作者 Fabio Cominelli 教授表示,持续六周的慢性压力对预防“二次伤害”(继发性肠炎)是有益的。我们发现,它能刺激免疫系统,从而防止肠道炎症;但需要进一步研究的是,这是否会转化为其他疾病或伤害。
总之,该研究表明,慢性心理压力通过 IL-23 信号传导的内在改变诱导结肠 TLO 形成,而不是通过微生物组的影响。此外,慢性压力对结肠炎的继发性损伤具有保护作用,这表明 TLO 可能起到改善粘膜屏障的作用。
最后,Fabio Cominelli 教授表示,我们是否需要压力,这完全取决于对压力的定义,其实,用“刺激”一词形容更好。因为在生活中,有一点压力是好的,但要以正确的方式来承受它。
原始出处:
Chronic stress induces colonic tertiary lymphoid organ formation and protection against secondary injury through IL-23/IL-22 signaling. PNAS, 2022.


